氯水成分与性质的探究[上学期]
图片预览






文档简介
课件22张PPT。氯水的成分与性质探究长兴中学 王强 氯气能溶解于水,
在常温下,1体积的水能
够溶解约2体积的氯气。
氯气的水溶液叫做氯水。
氯水的漂白性实验(实验) 为什么干燥的氯气无漂白性, 而潮湿的氯气有漂白性呢?探究1探究2 新制氯水中含有哪些微粒?
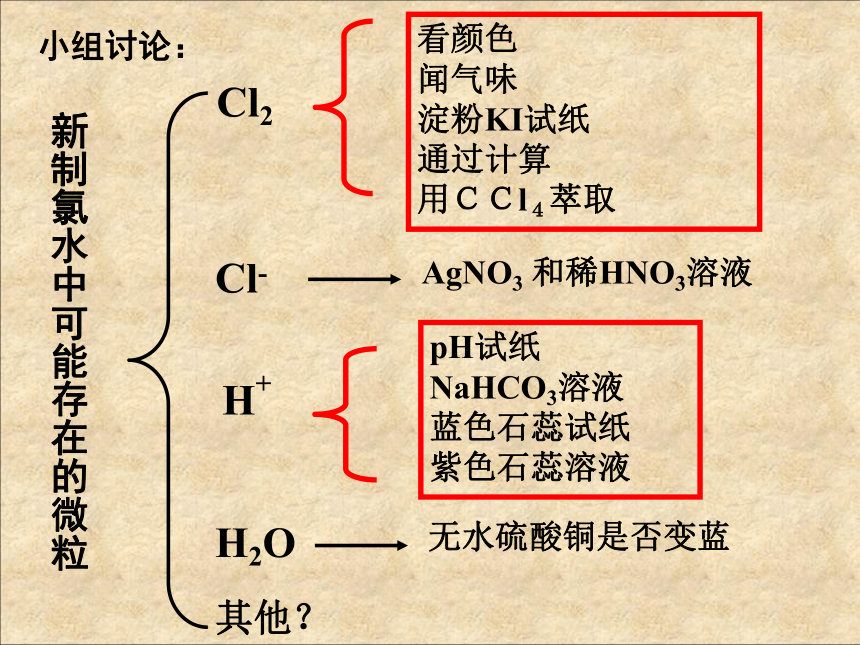
如何证明这些微粒的存在?新制氯水中可能存在的微粒Cl2H+小组讨论:Cl-其他?H2O 观察集气瓶中氯气的颜色,向集气瓶中
加入少量的蒸馏水,观察集气瓶中颜色
变化,再用PH试纸测量新制的氯水的PH
值,将PH试纸放置片刻,比较前后的颜色。实验现象:氯气是黄绿色气体,加入蒸馏水后颜色变浅,
水溶液也呈现浅绿色,pH试纸先变红,而
后红色又褪去 结论: 在洁净的试管中加入少量的碳酸氢钠粉末,
再加入2mL的氯水,振荡试管,观察现象。实验现象:结论:固体溶解,试管中产生气泡 氯水中含有H+实验现象:结论:在洁净的试管中加入2mL的氯水,再向
其中加入两滴红墨水,观察现象。红墨水的颜色褪去 氯水有漂白性 在洁净的试管中加入2mL的氯水,再向
其中加入几滴硝酸银和稀硝酸,观察
实验现象。 实验现象:结论:氯水中含有Cl-试管中有不溶于稀硝酸的白色沉淀产生 在洁净的试管中加入2mL氯化亚铁溶液,
再加入几滴新制的氯水,观察现象。实验现象:结论:Fe2+被氯气氧化 溶液颜色由浅绿色变为黄色 1、氯气与水的反应可逆反应:在相同条件下既能向正反应方向进行,
又能向逆方向进行的反应。
特点:1)相同条件下 2)同时 3)两个相反方向[思考1] 如果在紫色的石蕊溶液中加入氯气,会有什
么现象,解释原因?[思考2] 次氯酸的漂白性和我们初中所学的活性碳的
漂白性原理相同么?2、新制的氯水中的成分 分子: Cl2 HClO H2O
离子: H+ OH- Cl- ClO-疑问:为什么久置的氯水没有漂白性?次氯酸见光分解3、新制氯水的性质
具有氯气的性质(氧化性)具有强酸的性质(H+的性质)具有漂白性 (HClO的性质)具有Cl-的性质具有不稳定性:
2HClO = 2HCl+O2↑(条件:光照)[思考3] 新制的氯水和久置的氯水成分上相同么?
请同学设计实验探究探究记录:1.蓝色石蕊试纸只变红,
没有褪色1.说明不存在次氯酸3.pH试纸测得酸性增强3.说明H+的浓度增加2.无色2.说明没有氯分子【对 比】Cl2Cl2、H2O、HClOH2O无H+、Cl-、ClO-、
OH-(极少量)H+、Cl-、
OH-(极少量)淡黄绿色无色酸性、漂白性酸性(比新制氯水强)Cl2 + H2O == HCl + HClO你能否根据氯气与水的反应,
推测氯气与石灰乳的产物?2Cl2 + 2Ca(OH)2 == CaCl2 + Ca(ClO)2+ 2H2OCa(ClO)2 + H2O + CO2 == CaCO3↓ + 2HClO工业制漂白粉: CaCl2 、Ca(ClO)2的混合物巩固练习:1.下列关于氯水的说法正确的是( )
A.新制的氯水只含有氯气分子和水分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.光照氯水有气泡逸出,该气体主要是氯气
D.新制氯水久置后酸性增强,几乎无漂白性 BD巩固练习:2.下列物质中含有Cl-的是( )
A.液氯 B.氯水
C.KClO溶液 D.CuCl2溶液
E.KClO3溶液 BD巩固练习:3.用自来水养鱼时,将氯水注入鱼缸前需在阳光 下曝晒一段时间,主要目的是( )
A.起杀菌作用 B.使水中的HClO分解
C.提高水温 D.增加水中O2的含量B巩固练习:4.漂白粉制取原理的反应方程式是 ;
漂白粉的成分是 ;有效成分是 ;漂白粉放置在空气中失效的方程是 。Ca(ClO)2+CO2+H2O====CaCO3↓+2HClO2Cl2+2Ca(OH)2=====CaCl2+Ca(ClO)2+2H2OCaCl2和Ca(ClO)2Ca(ClO)2研究性课题:
某些地区自来水消毒采用的是氯气
消毒,请问氯气消毒的缺点?
??? 有的地区采用ClO2消毒,请问ClO2消
毒的优缺点?
???请浏览下面网站: http://www.xiaodu.net/clo2-bd/clo2-bd2.htm
谢谢观赏,再见!
在常温下,1体积的水能
够溶解约2体积的氯气。
氯气的水溶液叫做氯水。
氯水的漂白性实验(实验) 为什么干燥的氯气无漂白性, 而潮湿的氯气有漂白性呢?探究1探究2 新制氯水中含有哪些微粒?
如何证明这些微粒的存在?新制氯水中可能存在的微粒Cl2H+小组讨论:Cl-其他?H2O 观察集气瓶中氯气的颜色,向集气瓶中
加入少量的蒸馏水,观察集气瓶中颜色
变化,再用PH试纸测量新制的氯水的PH
值,将PH试纸放置片刻,比较前后的颜色。实验现象:氯气是黄绿色气体,加入蒸馏水后颜色变浅,
水溶液也呈现浅绿色,pH试纸先变红,而
后红色又褪去 结论: 在洁净的试管中加入少量的碳酸氢钠粉末,
再加入2mL的氯水,振荡试管,观察现象。实验现象:结论:固体溶解,试管中产生气泡 氯水中含有H+实验现象:结论:在洁净的试管中加入2mL的氯水,再向
其中加入两滴红墨水,观察现象。红墨水的颜色褪去 氯水有漂白性 在洁净的试管中加入2mL的氯水,再向
其中加入几滴硝酸银和稀硝酸,观察
实验现象。 实验现象:结论:氯水中含有Cl-试管中有不溶于稀硝酸的白色沉淀产生 在洁净的试管中加入2mL氯化亚铁溶液,
再加入几滴新制的氯水,观察现象。实验现象:结论:Fe2+被氯气氧化 溶液颜色由浅绿色变为黄色 1、氯气与水的反应可逆反应:在相同条件下既能向正反应方向进行,
又能向逆方向进行的反应。
特点:1)相同条件下 2)同时 3)两个相反方向[思考1] 如果在紫色的石蕊溶液中加入氯气,会有什
么现象,解释原因?[思考2] 次氯酸的漂白性和我们初中所学的活性碳的
漂白性原理相同么?2、新制的氯水中的成分 分子: Cl2 HClO H2O
离子: H+ OH- Cl- ClO-疑问:为什么久置的氯水没有漂白性?次氯酸见光分解3、新制氯水的性质
具有氯气的性质(氧化性)具有强酸的性质(H+的性质)具有漂白性 (HClO的性质)具有Cl-的性质具有不稳定性:
2HClO = 2HCl+O2↑(条件:光照)[思考3] 新制的氯水和久置的氯水成分上相同么?
请同学设计实验探究探究记录:1.蓝色石蕊试纸只变红,
没有褪色1.说明不存在次氯酸3.pH试纸测得酸性增强3.说明H+的浓度增加2.无色2.说明没有氯分子【对 比】Cl2Cl2、H2O、HClOH2O无H+、Cl-、ClO-、
OH-(极少量)H+、Cl-、
OH-(极少量)淡黄绿色无色酸性、漂白性酸性(比新制氯水强)Cl2 + H2O == HCl + HClO你能否根据氯气与水的反应,
推测氯气与石灰乳的产物?2Cl2 + 2Ca(OH)2 == CaCl2 + Ca(ClO)2+ 2H2OCa(ClO)2 + H2O + CO2 == CaCO3↓ + 2HClO工业制漂白粉: CaCl2 、Ca(ClO)2的混合物巩固练习:1.下列关于氯水的说法正确的是( )
A.新制的氯水只含有氯气分子和水分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.光照氯水有气泡逸出,该气体主要是氯气
D.新制氯水久置后酸性增强,几乎无漂白性 BD巩固练习:2.下列物质中含有Cl-的是( )
A.液氯 B.氯水
C.KClO溶液 D.CuCl2溶液
E.KClO3溶液 BD巩固练习:3.用自来水养鱼时,将氯水注入鱼缸前需在阳光 下曝晒一段时间,主要目的是( )
A.起杀菌作用 B.使水中的HClO分解
C.提高水温 D.增加水中O2的含量B巩固练习:4.漂白粉制取原理的反应方程式是 ;
漂白粉的成分是 ;有效成分是 ;漂白粉放置在空气中失效的方程是 。Ca(ClO)2+CO2+H2O====CaCO3↓+2HClO2Cl2+2Ca(OH)2=====CaCl2+Ca(ClO)2+2H2OCaCl2和Ca(ClO)2Ca(ClO)2研究性课题:
某些地区自来水消毒采用的是氯气
消毒,请问氯气消毒的缺点?
??? 有的地区采用ClO2消毒,请问ClO2消
毒的优缺点?
???请浏览下面网站: http://www.xiaodu.net/clo2-bd/clo2-bd2.htm
谢谢观赏,再见!
