铝的性质[上学期]
图片预览






文档简介
课件27张PPT。我们今天是桃李芬芳,明天是社会的栋梁!2019-2-28金属铝的性质与用途江苏省宿迁中学高一化学组2019-2-28铝 的 性 质 导 课 实验探究 小 结 练 习 2019-2-28回忆金属的化学性质化学性质特点是均易 最外层电子,表现 性,
且 电子的能力越强,则金属性越强。
主要表现:与非金属、酸、盐、氧化物等反应,
在这些反应中,金属单质均作 剂。失去还原失去还原2019-2-28氧
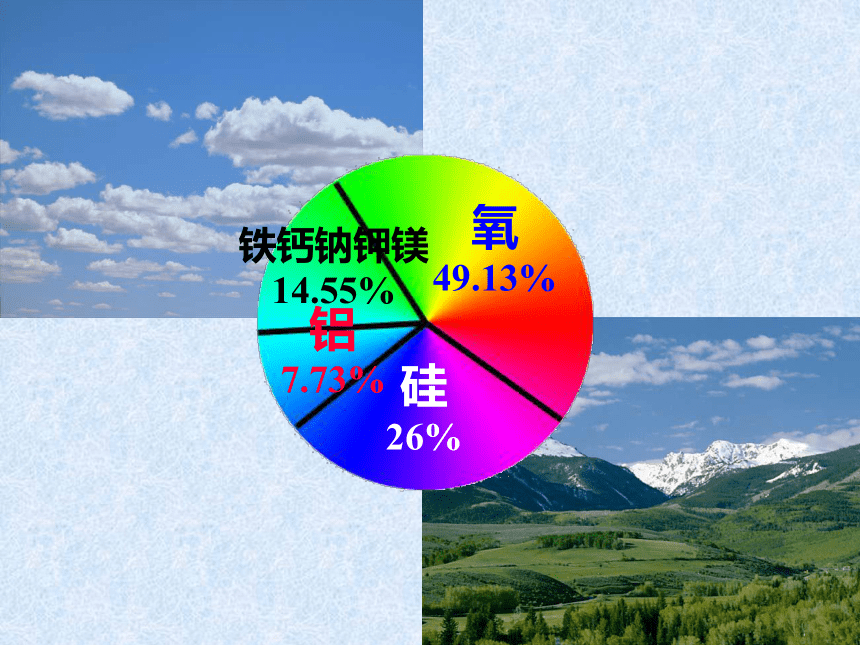
49.13%硅
26%铝
7.73%铁钙钠钾镁
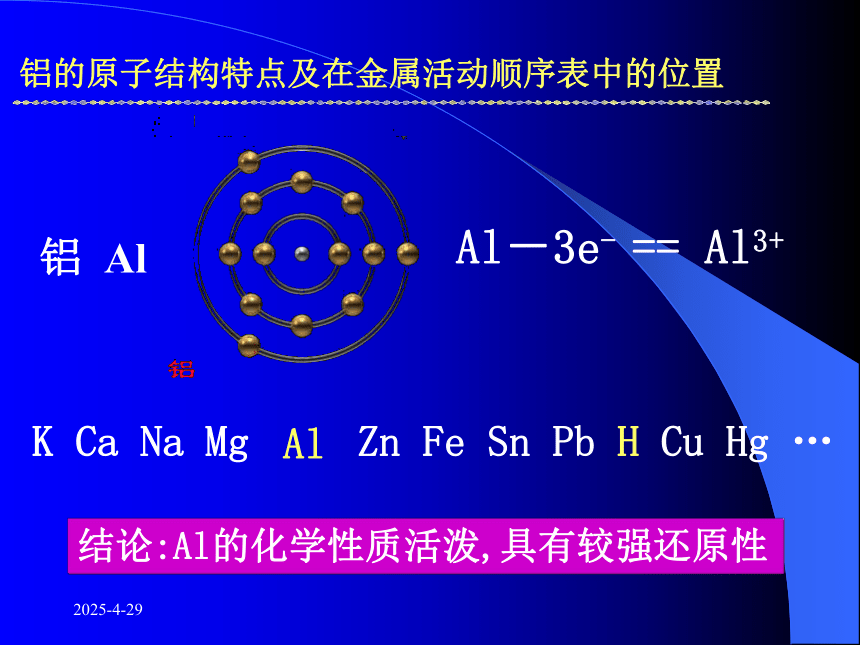
14.55%生活生产中的铝制品2019-2-28导热性能好导电性能较好铝的物理性质和用途2019-2-28铝的原子结构特点及在金属活动顺序表中的位置 Al-3e- == Al3+K Ca Na Mg Zn Fe Sn Pb H Cu Hg … Al结论:Al的化学性质活泼,具有较强还原性铝 Al2019-2-28① Al与氧气反应② Al与酸反应③ Al与NaOH溶液反应④ Al与Fe2O3反应观察.思考.探究2019-2-28铝与氧气反应剧烈燃烧,
放出大量的热和耀眼的白光现象:化学方程式:1.铝与非金属反应2019-2-28问题探究(1)铝锅为什么可以用来煮饭?(2)能写出Al和S、Cl2反应的化学方程式吗?铝具有导热性。常温下铝的表面被氧化,生成一层致密氧化物薄膜而具有抗腐蚀性。2019-2-282、铝与酸反应铝能将非氧化性酸中的H+置换成H2冷的浓硝酸,浓硫酸使铝表面钝化!把铝分别加入浓硝酸、浓硫酸、盐酸中2019-2-28铝与NaOH反应现象:铝与NaOH反应,有氢气产生。化学方程式:2Al + 2NaOH + 2H2O == 2NaAlO2 + 3H2↑3、铝与碱反应2019-2-286e-Al(OH)3+NaOH=NaAlO2+2H2O2019-2-28问题探究1.为什么铝制餐具不宜蒸煮或长期存放有酸性或碱性的食物? 2.Al与氨水反应能生成H2吗?Al能与酸或碱起反应不能! Al与强碱反应才能生成H2 2019-2-28现象:化学方程式:发出耀眼的光芒,有熔融物生成铝热剂4、铝热反应2019-2-28定向爆破上海成功实施定向爆破 未影响黄浦江防汛墙(图) ⅠⅡⅢ爆破前起爆瞬间爆破后2019-2-28问题探究1.铝热反应的原理?2.能写出下列方程式吗?Al的还原性强,且反应能放出大量的热,将生成物熔化。Al与V2O5 Al与Cr2O32019-2-28铝的用途性质→用途1.制造导线和电缆;
2.包装食品和饮料;制造日常用品;
3.加入其他元素,制造合金,用于飞机、汽车等部件;
4.可用铝制容器储运浓硫酸或浓硝酸;
5.用来焊接钢轨、冶炼难熔的金属,如:钒、铬、锰等。2019-2-28小结:铝的物理性质和用途铝的化学性质与氧化性单质反应与氧化物反应与酸、碱反应还原性2019-2-28开 心 辞 典这里有五个问题,你想回答哪一个?幻灯片 4222幻灯片 42幻灯片 19幻灯片 193幻灯片 424幻灯片 铝的性质1252019-2-281.下列关于铝的叙述中,不正确的是:
A.铝属于金属单质,不与任何碱反应
B.铝是地壳中含量最多的金属
C.在常温下,铝不能与氧气反应
D.铝既能与酸反应,也能与强碱反应A C2019-2-282.相等质量的两块铝,分别和足量的稀H2SO4和NaOH反应,产生气体在相同条件下的体积比:A.2:3 B.3:2 C.2:1 D.1:1D.1:12019-2-283.铝具有较强的抗腐蚀性,主要因为:
A.铝不活泼??? B.具有两性??
C.铝与氧气在常温下不反应
D.铝表面在常温下能形成一层致密的氧化物薄膜D2019-2-284.在加入铝粉能放出H2的溶液中,一定能大量 共存的离子组是:A.K+、Na+、CO32-、SO42- B.NH4+、Na+、Cl-、NO3-
C.K+、Na+、Cl-、SO42- D.K+、HCO3-、Cl- 、SO42-C2019-2-285.将一个用金属铝做的易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口。经过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起来。
(1)罐壁内凹而瘪的原因是_____;
(2)罐再鼓起的原因是______。2019-2-28再见谢谢同学们的合作2019-2-28
且 电子的能力越强,则金属性越强。
主要表现:与非金属、酸、盐、氧化物等反应,
在这些反应中,金属单质均作 剂。失去还原失去还原2019-2-28氧
49.13%硅
26%铝
7.73%铁钙钠钾镁
14.55%生活生产中的铝制品2019-2-28导热性能好导电性能较好铝的物理性质和用途2019-2-28铝的原子结构特点及在金属活动顺序表中的位置 Al-3e- == Al3+K Ca Na Mg Zn Fe Sn Pb H Cu Hg … Al结论:Al的化学性质活泼,具有较强还原性铝 Al2019-2-28① Al与氧气反应② Al与酸反应③ Al与NaOH溶液反应④ Al与Fe2O3反应观察.思考.探究2019-2-28铝与氧气反应剧烈燃烧,
放出大量的热和耀眼的白光现象:化学方程式:1.铝与非金属反应2019-2-28问题探究(1)铝锅为什么可以用来煮饭?(2)能写出Al和S、Cl2反应的化学方程式吗?铝具有导热性。常温下铝的表面被氧化,生成一层致密氧化物薄膜而具有抗腐蚀性。2019-2-282、铝与酸反应铝能将非氧化性酸中的H+置换成H2冷的浓硝酸,浓硫酸使铝表面钝化!把铝分别加入浓硝酸、浓硫酸、盐酸中2019-2-28铝与NaOH反应现象:铝与NaOH反应,有氢气产生。化学方程式:2Al + 2NaOH + 2H2O == 2NaAlO2 + 3H2↑3、铝与碱反应2019-2-286e-Al(OH)3+NaOH=NaAlO2+2H2O2019-2-28问题探究1.为什么铝制餐具不宜蒸煮或长期存放有酸性或碱性的食物? 2.Al与氨水反应能生成H2吗?Al能与酸或碱起反应不能! Al与强碱反应才能生成H2 2019-2-28现象:化学方程式:发出耀眼的光芒,有熔融物生成铝热剂4、铝热反应2019-2-28定向爆破上海成功实施定向爆破 未影响黄浦江防汛墙(图) ⅠⅡⅢ爆破前起爆瞬间爆破后2019-2-28问题探究1.铝热反应的原理?2.能写出下列方程式吗?Al的还原性强,且反应能放出大量的热,将生成物熔化。Al与V2O5 Al与Cr2O32019-2-28铝的用途性质→用途1.制造导线和电缆;
2.包装食品和饮料;制造日常用品;
3.加入其他元素,制造合金,用于飞机、汽车等部件;
4.可用铝制容器储运浓硫酸或浓硝酸;
5.用来焊接钢轨、冶炼难熔的金属,如:钒、铬、锰等。2019-2-28小结:铝的物理性质和用途铝的化学性质与氧化性单质反应与氧化物反应与酸、碱反应还原性2019-2-28开 心 辞 典这里有五个问题,你想回答哪一个?幻灯片 4222幻灯片 42幻灯片 19幻灯片 193幻灯片 424幻灯片 铝的性质1252019-2-281.下列关于铝的叙述中,不正确的是:
A.铝属于金属单质,不与任何碱反应
B.铝是地壳中含量最多的金属
C.在常温下,铝不能与氧气反应
D.铝既能与酸反应,也能与强碱反应A C2019-2-282.相等质量的两块铝,分别和足量的稀H2SO4和NaOH反应,产生气体在相同条件下的体积比:A.2:3 B.3:2 C.2:1 D.1:1D.1:12019-2-283.铝具有较强的抗腐蚀性,主要因为:
A.铝不活泼??? B.具有两性??
C.铝与氧气在常温下不反应
D.铝表面在常温下能形成一层致密的氧化物薄膜D2019-2-284.在加入铝粉能放出H2的溶液中,一定能大量 共存的离子组是:A.K+、Na+、CO32-、SO42- B.NH4+、Na+、Cl-、NO3-
C.K+、Na+、Cl-、SO42- D.K+、HCO3-、Cl- 、SO42-C2019-2-285.将一个用金属铝做的易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口。经过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起来。
(1)罐壁内凹而瘪的原因是_____;
(2)罐再鼓起的原因是______。2019-2-28再见谢谢同学们的合作2019-2-28
