胶体的性质及应用[上学期]
图片预览






文档简介
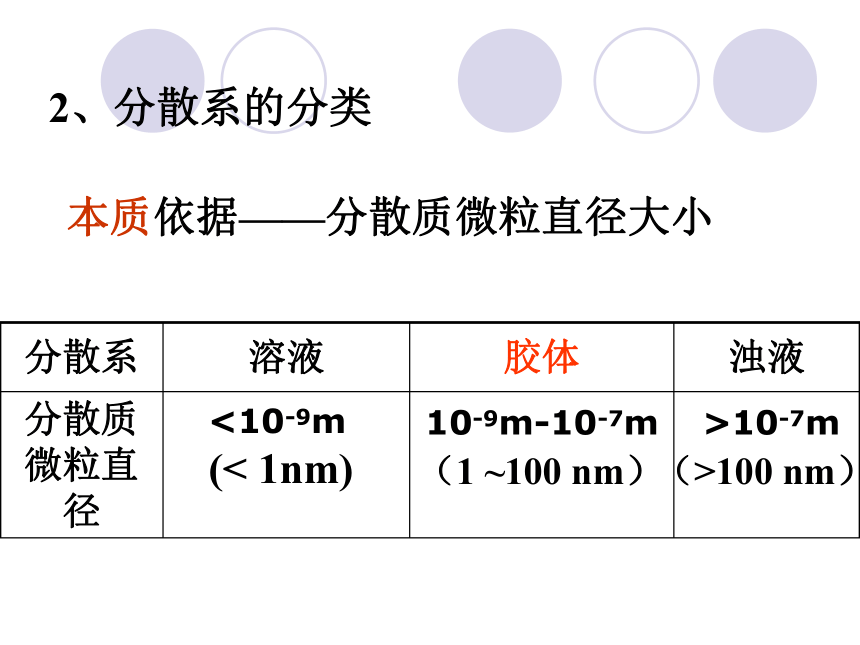
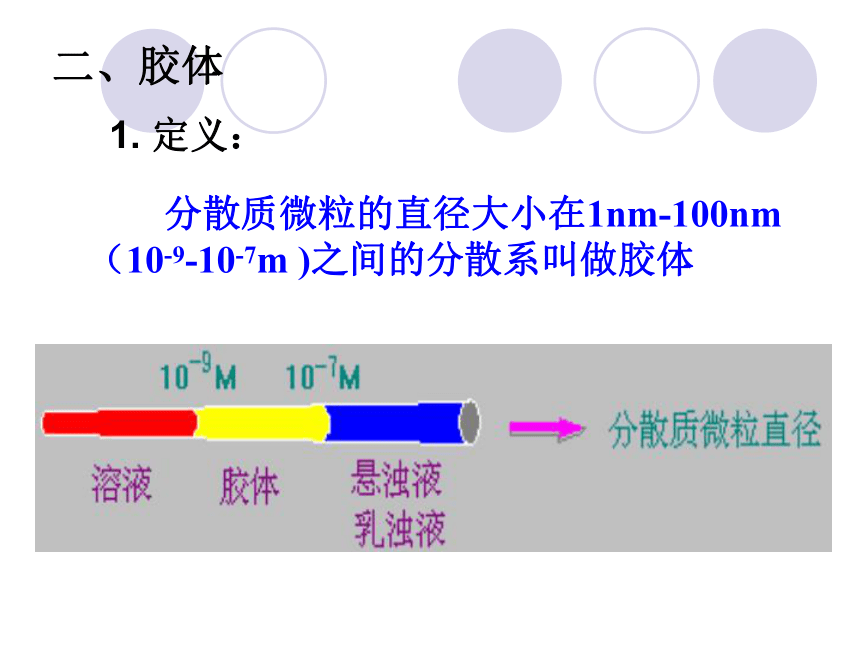
课件28张PPT。物质的分散系高一化学备课组 陈 健1、定义:一种或一种以上的物质分散到 另一种物质中所得到的混合物 分散质:被分散的物质 分散剂:能分散分散质的物质 一、分散系溶液、悬(乳)浊液、胶体(其中分散成微粒的物质)(微粒分散在其中的物质)2、分散系的分类本质依据——分散质微粒直径大小<10-9m(< 1nm) 10-9m-10-7m(1 ~100 nm) >10-7m(>100 nm) 二、胶体 分散质微粒的直径大小在1nm-100nm(10-9-10-7m )之间的分散系叫做胶体1. 定义:胶体制备的方法:胶体中
分散质 悬浮颗粒 分子、原子和离子 分散法 凝聚法 将悬浊液或乳浊液中的分散质分散;如:磨墨
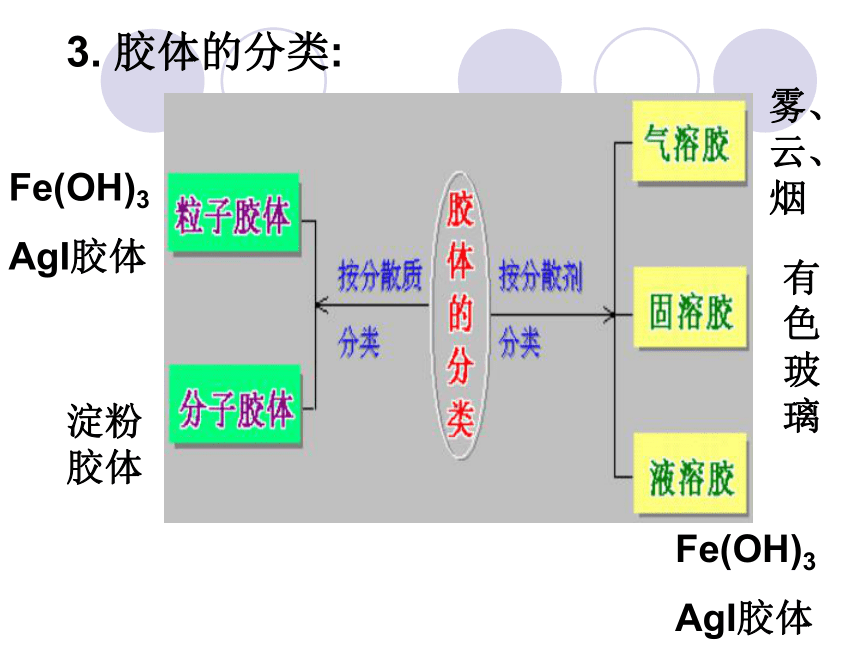
常见的胶体有:墨汁、碳素墨水、淀粉溶液等2、胶体的制备原理:使分散质粒子大小在1nm ~ 100nm之间物理方法化学方法①水解法注意:不能过度加热,以免出现Fe(OH)3胶体凝聚。红褐色 FeCl3溶液中存在微弱的水解,生成极少量的Fe(OH)3 ,加热, 加大水解程度, 使Fe(OH)3聚集成较大颗粒 ——胶体 条件:饱和FeCl3溶液、沸水②复分解法AgNO3+KI=AgI(胶体)+KNO3 注意:浓度控制,浓度过大会生成沉淀,逐滴滴加,同时要不断振荡。 胶体较为稳定,但是长时间放置之后也会出现沉淀。所以胶体通常现配现用。浅黄色3. 胶体的分类:Fe(OH)3
AgI胶体淀粉胶体雾、云、烟有色玻璃Fe(OH)3
AgI胶体注:胶体不是一类物质,而是几乎任何物质都可能形成的一种分散状态。如:NaCl溶于水形成溶液,如果分散在酒精中则可形成胶体。练习:(2000·上海)用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子直径和这种粒子具有相同数量级的是 ( )
A、溶液 B、悬浊液 C、胶体 D、乳浊液
c4、渗析利用半透膜把胶体中混有的离子或分子从胶体溶液里分离的操作,叫做渗析。
其原理为胶体微粒不能透过半透膜,而溶液中的分子和离子能透过半透膜。 应用:
胶体净化、提纯使胶体和溶液分离< 1nm 1 ~100 nm >100 nm 单个分子或离子 许多分子集合体 大量分子集合体 能 能 不能 能 不能 不能 稳定 较稳定 不稳定 【小结】:三种分散系的比较(胶体)(溶液)三、胶体的性质 1、丁达尔现象(光学性质)
实验:光束分别通过Fe(OH)3胶体和CuSO4溶液,观察现象。现象:一束光通过胶体时,从侧面可观察到胶体里产生一条光亮的“通路”。丁达尔现象(光学性质)原因:胶粒直径大小与光的波长相近,胶粒对
光有散射作用;而溶液分散质的粒子太
小,不发生散射。应用:鉴别溶胶和溶液。 练习:不能发生丁达尔现象的分散系是( )
A、碘酒 B、无水酒精
C、蛋白质溶液 D、钴玻璃A B普遍存在的现象 2、 布朗运动(动力学性质) 在超显微镜下观察胶体溶液可以看到胶体颗粒不断地作无规则的运动。原因:溶剂分子不均匀地撞击胶体粒子,使其发生不断改变方向、改变速率的布朗运动。胶体微粒作布朗运动是胶体稳定的原因之一。练习:胶体粒子能作布朗运动的原因是 ( )
①水分子对胶体粒子的撞击 ②胶体粒子有
吸附能力 ③胶体粒子带电 ④胶体粒子质
量很小,所受重力小
A、①② B、①③ C、①④ D、②④
c在外加电场作用下, 胶体粒子在分散剂里向电极 (阴极或阳极) 作定向移动的现象, 叫做电泳Fe(OH)3胶体向阴极
移动——带正电荷 3、 电泳现象(电学性质)原因:粒子胶体微粒带同种电荷,当胶粒带正
电荷时向阴极运动,当胶粒带负电荷时
向阳极运动。应用:①静电除尘;②电泳电镀,利用电泳将油漆、
乳胶、橡胶等粒子均匀地沉积在镀件上。胶体的胶粒有的带电,有电泳现象;有的不带电,没有电泳现象。Q:可否用电泳现象净化或检验胶体?重要胶粒带电的一般规律: 胶粒带同种电荷,相互间产生排斥作用,不易结合成更大的沉淀微粒,这是胶体具有稳定性的主要因素。 在陶瓷工业上常遇到因陶土里混有Fe2O3而影响产品质量的问题。解决方法之一是把这些陶土和水放在一起搅拌,使粒子大小在1nm~100nm之间,然后插入两根电极,接通直流电源,这时阳极聚积 ,
阴极聚积 ,理由
是 。
例题带负电荷的胶粒(粒子陶土) 带正电荷的胶粒(Fe2O3) 含有杂质的陶土和水形成了胶体,利用电泳将
陶土和杂质分离除杂 例题:已知土壤胶体中的粒子带负电荷,又有很大的表面积,因而具有选择吸附能力。 有下列阴阳离子,NH4+、K+、H+、NO3-、H2PO4 -、PO43- ,哪些易被吸附?在土壤里施用含氮量相同的下列肥料,肥效较差的是
(NH4)2SO4 、 NH4HCO3 、 NH4NO3 、 NH4Cl 土壤胶粒一般带负电荷,容易再吸附阳离子如NH4+、K+、H+,而难以吸附阴离子如NO3-、H2PO4 -、PO43-,据此,我们可以得到如下有关施用化肥与土壤胶体关系的常识:①铵态氮肥、钾肥容易被土壤吸收,此类化肥可以直接进行表面施用。②磷肥不易被土壤吸收,易随雨水流失,因此,磷肥必须深施在土壤里层,以保证有效利用。③施用硝酸盐氮肥肥料不如施用铵态氮肥好,如NH4NO3虽含氮量高,但NO3-的利用率低,多雨季节不宜使用。④酸雨和长期施用酸性化肥容易导致土壤胶粒吸附H+,而使土壤酸化,影响植物生长,也影响铵态氮肥和钾肥的有效利用。 4、胶体的聚沉 要使胶体凝聚成沉淀,就要减少或消除胶体微粒表面吸附的电荷,使之减弱或失去电性排斥力作用,从而使胶粒在运动中碰撞结合成更大的颗粒。Q1:胶体为什么能够稳定存在?
胶粒带电、布朗运动Q2:如何破坏胶体的稳定状态? 使胶体微粒凝聚成更大的颗粒,形成沉淀,从分散剂里析出的过程叫胶体的聚沉。实例:
①浑浊的井水中加入少量石灰能使水变澄清;
②豆浆里加盐卤(MgCl2·6H2O)或石膏(CaSO4·2H2O)溶液使之凝聚成豆腐;
③水泥里加石膏能调节水泥浆的硬化速率;
④在江河与海的交汇处形成的沙洲。(1)加入电解质(2)加入胶粒带相反电荷的胶体带不同电荷的胶体微粒相互吸引发生电性中和,从而在胶粒碰撞时发生凝聚,形成沉淀或凝胶。实验:将Fe(OH)3胶体溶液与硅酸胶体溶液
现象:形成大量的沉淀.
结论:Fe(OH)3胶粒与H2SiO3胶粒带相反电荷.实例:①用明矾、氯化铁等净水;②不同种类的墨水混合使用时有沉淀产生,使墨水失效。(3)加热 温度升高,胶粒的吸附能力减弱,减少了胶粒所吸引的阴离子或阳离子数量,胶粒所带的电荷数减少,胶粒间的斥力作用减弱,使得胶粒在碰撞时容易结合成大颗粒,形成沉淀或凝胶。实例:淀粉溶液加热后凝聚成了浆糊凝胶,蛋清加热后凝聚成了白色胶状物(同时发生变性)。 练习:氯化铁溶液与氢氧化铁胶体具有的共同性
质是 ( )
A、分散质颗粒直径都在1nm~100nm之间
B、能透过半透膜
C、加热蒸干、灼烧后都有氧化铁生成
D、呈红褐色C 练习:下列事实:①用盐卤点豆腐 ②用明矾净水 ③ 河海交汇处可沉积沙洲 ④钢笔使用两种不同颜色的蓝墨水,易出现堵塞 ⑤血液透析。其中与胶体知识有关的是 ( )
A、①②③ B、③④⑤
C、①③⑤ D、全部都是D土壤的性质 化学工业 食品 建筑材料
分散质 悬浮颗粒 分子、原子和离子 分散法 凝聚法 将悬浊液或乳浊液中的分散质分散;如:磨墨
常见的胶体有:墨汁、碳素墨水、淀粉溶液等2、胶体的制备原理:使分散质粒子大小在1nm ~ 100nm之间物理方法化学方法①水解法注意:不能过度加热,以免出现Fe(OH)3胶体凝聚。红褐色 FeCl3溶液中存在微弱的水解,生成极少量的Fe(OH)3 ,加热, 加大水解程度, 使Fe(OH)3聚集成较大颗粒 ——胶体 条件:饱和FeCl3溶液、沸水②复分解法AgNO3+KI=AgI(胶体)+KNO3 注意:浓度控制,浓度过大会生成沉淀,逐滴滴加,同时要不断振荡。 胶体较为稳定,但是长时间放置之后也会出现沉淀。所以胶体通常现配现用。浅黄色3. 胶体的分类:Fe(OH)3
AgI胶体淀粉胶体雾、云、烟有色玻璃Fe(OH)3
AgI胶体注:胶体不是一类物质,而是几乎任何物质都可能形成的一种分散状态。如:NaCl溶于水形成溶液,如果分散在酒精中则可形成胶体。练习:(2000·上海)用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子直径和这种粒子具有相同数量级的是 ( )
A、溶液 B、悬浊液 C、胶体 D、乳浊液
c4、渗析利用半透膜把胶体中混有的离子或分子从胶体溶液里分离的操作,叫做渗析。
其原理为胶体微粒不能透过半透膜,而溶液中的分子和离子能透过半透膜。 应用:
胶体净化、提纯使胶体和溶液分离< 1nm 1 ~100 nm >100 nm 单个分子或离子 许多分子集合体 大量分子集合体 能 能 不能 能 不能 不能 稳定 较稳定 不稳定 【小结】:三种分散系的比较(胶体)(溶液)三、胶体的性质 1、丁达尔现象(光学性质)
实验:光束分别通过Fe(OH)3胶体和CuSO4溶液,观察现象。现象:一束光通过胶体时,从侧面可观察到胶体里产生一条光亮的“通路”。丁达尔现象(光学性质)原因:胶粒直径大小与光的波长相近,胶粒对
光有散射作用;而溶液分散质的粒子太
小,不发生散射。应用:鉴别溶胶和溶液。 练习:不能发生丁达尔现象的分散系是( )
A、碘酒 B、无水酒精
C、蛋白质溶液 D、钴玻璃A B普遍存在的现象 2、 布朗运动(动力学性质) 在超显微镜下观察胶体溶液可以看到胶体颗粒不断地作无规则的运动。原因:溶剂分子不均匀地撞击胶体粒子,使其发生不断改变方向、改变速率的布朗运动。胶体微粒作布朗运动是胶体稳定的原因之一。练习:胶体粒子能作布朗运动的原因是 ( )
①水分子对胶体粒子的撞击 ②胶体粒子有
吸附能力 ③胶体粒子带电 ④胶体粒子质
量很小,所受重力小
A、①② B、①③ C、①④ D、②④
c在外加电场作用下, 胶体粒子在分散剂里向电极 (阴极或阳极) 作定向移动的现象, 叫做电泳Fe(OH)3胶体向阴极
移动——带正电荷 3、 电泳现象(电学性质)原因:粒子胶体微粒带同种电荷,当胶粒带正
电荷时向阴极运动,当胶粒带负电荷时
向阳极运动。应用:①静电除尘;②电泳电镀,利用电泳将油漆、
乳胶、橡胶等粒子均匀地沉积在镀件上。胶体的胶粒有的带电,有电泳现象;有的不带电,没有电泳现象。Q:可否用电泳现象净化或检验胶体?重要胶粒带电的一般规律: 胶粒带同种电荷,相互间产生排斥作用,不易结合成更大的沉淀微粒,这是胶体具有稳定性的主要因素。 在陶瓷工业上常遇到因陶土里混有Fe2O3而影响产品质量的问题。解决方法之一是把这些陶土和水放在一起搅拌,使粒子大小在1nm~100nm之间,然后插入两根电极,接通直流电源,这时阳极聚积 ,
阴极聚积 ,理由
是 。
例题带负电荷的胶粒(粒子陶土) 带正电荷的胶粒(Fe2O3) 含有杂质的陶土和水形成了胶体,利用电泳将
陶土和杂质分离除杂 例题:已知土壤胶体中的粒子带负电荷,又有很大的表面积,因而具有选择吸附能力。 有下列阴阳离子,NH4+、K+、H+、NO3-、H2PO4 -、PO43- ,哪些易被吸附?在土壤里施用含氮量相同的下列肥料,肥效较差的是
(NH4)2SO4 、 NH4HCO3 、 NH4NO3 、 NH4Cl 土壤胶粒一般带负电荷,容易再吸附阳离子如NH4+、K+、H+,而难以吸附阴离子如NO3-、H2PO4 -、PO43-,据此,我们可以得到如下有关施用化肥与土壤胶体关系的常识:①铵态氮肥、钾肥容易被土壤吸收,此类化肥可以直接进行表面施用。②磷肥不易被土壤吸收,易随雨水流失,因此,磷肥必须深施在土壤里层,以保证有效利用。③施用硝酸盐氮肥肥料不如施用铵态氮肥好,如NH4NO3虽含氮量高,但NO3-的利用率低,多雨季节不宜使用。④酸雨和长期施用酸性化肥容易导致土壤胶粒吸附H+,而使土壤酸化,影响植物生长,也影响铵态氮肥和钾肥的有效利用。 4、胶体的聚沉 要使胶体凝聚成沉淀,就要减少或消除胶体微粒表面吸附的电荷,使之减弱或失去电性排斥力作用,从而使胶粒在运动中碰撞结合成更大的颗粒。Q1:胶体为什么能够稳定存在?
胶粒带电、布朗运动Q2:如何破坏胶体的稳定状态? 使胶体微粒凝聚成更大的颗粒,形成沉淀,从分散剂里析出的过程叫胶体的聚沉。实例:
①浑浊的井水中加入少量石灰能使水变澄清;
②豆浆里加盐卤(MgCl2·6H2O)或石膏(CaSO4·2H2O)溶液使之凝聚成豆腐;
③水泥里加石膏能调节水泥浆的硬化速率;
④在江河与海的交汇处形成的沙洲。(1)加入电解质(2)加入胶粒带相反电荷的胶体带不同电荷的胶体微粒相互吸引发生电性中和,从而在胶粒碰撞时发生凝聚,形成沉淀或凝胶。实验:将Fe(OH)3胶体溶液与硅酸胶体溶液
现象:形成大量的沉淀.
结论:Fe(OH)3胶粒与H2SiO3胶粒带相反电荷.实例:①用明矾、氯化铁等净水;②不同种类的墨水混合使用时有沉淀产生,使墨水失效。(3)加热 温度升高,胶粒的吸附能力减弱,减少了胶粒所吸引的阴离子或阳离子数量,胶粒所带的电荷数减少,胶粒间的斥力作用减弱,使得胶粒在碰撞时容易结合成大颗粒,形成沉淀或凝胶。实例:淀粉溶液加热后凝聚成了浆糊凝胶,蛋清加热后凝聚成了白色胶状物(同时发生变性)。 练习:氯化铁溶液与氢氧化铁胶体具有的共同性
质是 ( )
A、分散质颗粒直径都在1nm~100nm之间
B、能透过半透膜
C、加热蒸干、灼烧后都有氧化铁生成
D、呈红褐色C 练习:下列事实:①用盐卤点豆腐 ②用明矾净水 ③ 河海交汇处可沉积沙洲 ④钢笔使用两种不同颜色的蓝墨水,易出现堵塞 ⑤血液透析。其中与胶体知识有关的是 ( )
A、①②③ B、③④⑤
C、①③⑤ D、全部都是D土壤的性质 化学工业 食品 建筑材料
