原子核外电子排布[下学期]
图片预览






文档简介
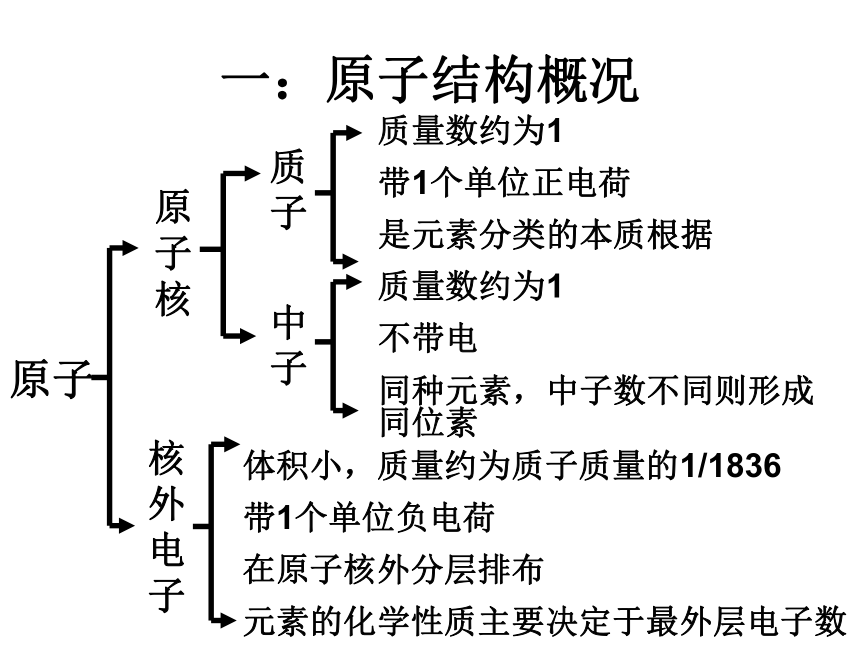
课件17张PPT。§1:原子核外电子的排布 根据你对原子的理解,给“原子”这个词造一个句子?一:原子结构概况原子核核外电子质子中子质量数约为1
带1个单位正电荷
是元素分类的本质根据质量数约为1
不带电
同种元素,中子数不同则形成同位素体积小,质量约为质子质量的1/1836
带1个单位负电荷
在原子核外分层排布
元素的化学性质主要决定于最外层电子数训练 b Xn 说一说 中a、b、c+、c-、+d、 -d、n的化学涵义? a---代表质量数;
b---代表核电荷数;
c---代表离子所带的电荷数;
d---代表元素的化合价;
n---代表微粒中所含的原子数。二:原子中的重要关系质子数(Z)+中子数(N)==质量数(A)≈
≈原子的相对原子质量;在原子中:质子数(Z)==核外电子数
==核电荷数=原子序数;在阴离子中:质子数(Z)==核外电子数-电荷数;在阳离子中:质子数(Z)==核外电子数+电荷数;提问1: 观察图1-1、1-2所示的元素原子结构示意图。你能发现随着元素核电荷数的递增,元素原子核外电子的排布有什么规律吗?小结:电子层数: 1、 2、 3、 4、 5、 6、 7
电子层符号:K、L、 M、N、O、P、Q
提问2: 观察分析表1-1所示稀有气体元素的原子核外电子排布,与同学讨论下列问题:
1、从稀有气体元素的原子核外电子排布可知,K、L、M、N电子层最多能容纳的电子数依次是多少?请由此推出原子核外各电子层最多能容纳的电子数和电子层序数n的关系。
2、各稀有气体元素原子中最外电子层最多容纳的电子数是多少?次外电子层最多容纳的电子数是多少?
小结:电子层数: 1、 2、 3、 4……
电子层符号: K、 L、 M、N……
最多容纳的电子数:2、 8、18、32……2n2
离核远近或能量高低:K2、最外层电子数不超过8个,K层作最外层时不超过2个;
3、次外层电子数不超过18个,倒数第三层电子数不超过32个;
4、电子总是尽先排布在能量在低的电子层,然后由里往外,依次排布在能量逐步升高的电子层里;即先排K层,排满K层再排L层,排满L层再排M层。练习1:画出下列微粒的结构示意图:
S、 Al、 C、 Ne、 S2-、F-、 Mg2+。练习2: 能用结构示意图 表示的原子是________,阳离子有_______________,阴离子有_____________.NeNa+、Mg2+、Al3+F-、O2-、N3-交流与讨论 根据图1-2、稀有气体性质稳定及钠原子和氯原子形成氯化钠的过程,讨论元素的性质与原子核外电子排布的关系?结论1:1、最外层电子数少于等于3个的原子一般是金属元素的原子,在化学反应中容易失去最外层电子,使次外层变成最外层,达到8电子稳定结构。
2、最外层电子数多于等于4个的原子一般是非金属元素的原子,在化学反应中容易得到电子,使最外层达到8电子稳定结构。
3、具有K电子层2个电子,其它电子层8个电子的结构,称为稳定结构,不易发生化学反应。
4、因此说:元素的性质,特别是化学性质,主要决定于原子的最外层电子数。练习3: Na、Mg、Al等活泼金属单质与F2、O2、Cl2等活泼非金属单质发生反应生成的化合物中,金属元素和非金属元素的化合价与其在反应中失去或得到电子的数目存在一定的关系。请与同学共同探究下列问题。
1、金属单质Na、Mg能分别与非金属单质O2、Cl2反应生成氧化物和氯化物,请写出这些氧化物和氯化物的化学式。_____________________________________.Na2O、Na2O2、NaCl、MgO、MgCl2。结论2: 在活泼金属元素和活泼非金属元素形成的化合物(离子化合物)中;元素化合价数值与该元素的一个原子得失电子数目相等,得到电子带负电为负价,失去电子带正电为正价。反思与收获 今天我们学会了什么知识?
带1个单位正电荷
是元素分类的本质根据质量数约为1
不带电
同种元素,中子数不同则形成同位素体积小,质量约为质子质量的1/1836
带1个单位负电荷
在原子核外分层排布
元素的化学性质主要决定于最外层电子数训练 b Xn 说一说 中a、b、c+、c-、+d、 -d、n的化学涵义? a---代表质量数;
b---代表核电荷数;
c---代表离子所带的电荷数;
d---代表元素的化合价;
n---代表微粒中所含的原子数。二:原子中的重要关系质子数(Z)+中子数(N)==质量数(A)≈
≈原子的相对原子质量;在原子中:质子数(Z)==核外电子数
==核电荷数=原子序数;在阴离子中:质子数(Z)==核外电子数-电荷数;在阳离子中:质子数(Z)==核外电子数+电荷数;提问1: 观察图1-1、1-2所示的元素原子结构示意图。你能发现随着元素核电荷数的递增,元素原子核外电子的排布有什么规律吗?小结:电子层数: 1、 2、 3、 4、 5、 6、 7
电子层符号:K、L、 M、N、O、P、Q
提问2: 观察分析表1-1所示稀有气体元素的原子核外电子排布,与同学讨论下列问题:
1、从稀有气体元素的原子核外电子排布可知,K、L、M、N电子层最多能容纳的电子数依次是多少?请由此推出原子核外各电子层最多能容纳的电子数和电子层序数n的关系。
2、各稀有气体元素原子中最外电子层最多容纳的电子数是多少?次外电子层最多容纳的电子数是多少?
小结:电子层数: 1、 2、 3、 4……
电子层符号: K、 L、 M、N……
最多容纳的电子数:2、 8、18、32……2n2
离核远近或能量高低:K
3、次外层电子数不超过18个,倒数第三层电子数不超过32个;
4、电子总是尽先排布在能量在低的电子层,然后由里往外,依次排布在能量逐步升高的电子层里;即先排K层,排满K层再排L层,排满L层再排M层。练习1:画出下列微粒的结构示意图:
S、 Al、 C、 Ne、 S2-、F-、 Mg2+。练习2: 能用结构示意图 表示的原子是________,阳离子有_______________,阴离子有_____________.NeNa+、Mg2+、Al3+F-、O2-、N3-交流与讨论 根据图1-2、稀有气体性质稳定及钠原子和氯原子形成氯化钠的过程,讨论元素的性质与原子核外电子排布的关系?结论1:1、最外层电子数少于等于3个的原子一般是金属元素的原子,在化学反应中容易失去最外层电子,使次外层变成最外层,达到8电子稳定结构。
2、最外层电子数多于等于4个的原子一般是非金属元素的原子,在化学反应中容易得到电子,使最外层达到8电子稳定结构。
3、具有K电子层2个电子,其它电子层8个电子的结构,称为稳定结构,不易发生化学反应。
4、因此说:元素的性质,特别是化学性质,主要决定于原子的最外层电子数。练习3: Na、Mg、Al等活泼金属单质与F2、O2、Cl2等活泼非金属单质发生反应生成的化合物中,金属元素和非金属元素的化合价与其在反应中失去或得到电子的数目存在一定的关系。请与同学共同探究下列问题。
1、金属单质Na、Mg能分别与非金属单质O2、Cl2反应生成氧化物和氯化物,请写出这些氧化物和氯化物的化学式。_____________________________________.Na2O、Na2O2、NaCl、MgO、MgCl2。结论2: 在活泼金属元素和活泼非金属元素形成的化合物(离子化合物)中;元素化合价数值与该元素的一个原子得失电子数目相等,得到电子带负电为负价,失去电子带正电为正价。反思与收获 今天我们学会了什么知识?
