人教版高中化学选修四 3.4.1 沉淀溶解平衡与溶度积教学课件(31张)
文档属性
| 名称 | 人教版高中化学选修四 3.4.1 沉淀溶解平衡与溶度积教学课件(31张) |

|
|
| 格式 | zip | ||
| 文件大小 | 722.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-11-19 00:00:00 | ||
图片预览










文档简介
课件31张PPT。第1课时 沉淀溶解平衡与溶度积第三章 第四节学习目标定位
1.知道沉淀溶解平衡的概念及其影响因素。
2.明确溶度积和离子积的关系,并由此学会判断反应进行的方向。一 难溶电解质的溶解平衡达标检测 提升技能内容索引二 溶度积常数一 难溶电解质的溶解平衡下列物质,属于易溶物质的是 ,属于微溶物质的是 ,属于难溶物质的是 。
①NaCl、②NaOH、③H2SO4、④MgCO3、⑤CaSO4、⑥Ca(OH)2、
⑦CaCO3、⑧BaSO4、⑨Mg(OH)21.不同的固体物质在水中的溶解度不同,有的很大,有的很小,但无论大小,都有一定的溶解度。在20 ℃时,物质的溶解度与溶解性的关系如下:难溶微溶可溶新知导学易溶①②③④⑤⑥⑦⑧⑨2.固体物质的溶解是可逆过程
固体溶质 溶液中的溶质
(1)v溶解 v沉淀 固体溶解
(2)v溶解 v沉淀 溶解平衡
(3)v溶解 v沉淀 析出晶体
3.在一定温度下,当 时,即建立了动态平衡,叫做沉淀 。如AgCl溶于水的溶解平衡表示为
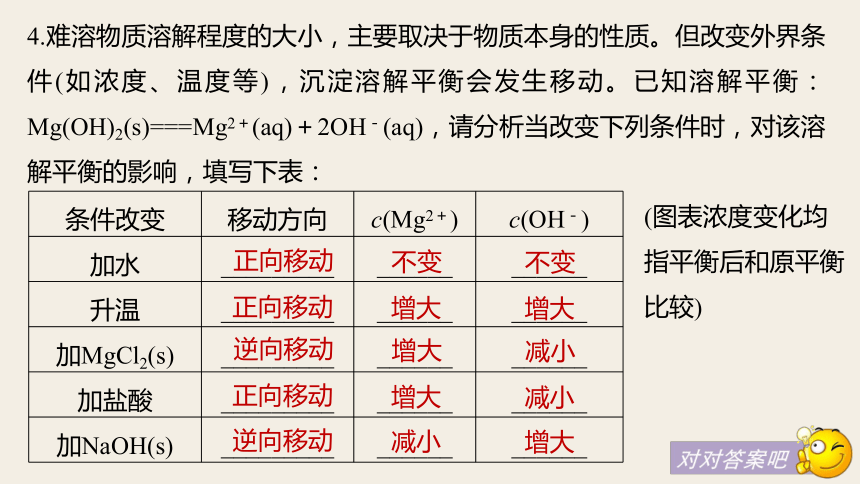
AgCl(s) Ag+(aq)+Cl-(aq)。>=<沉淀溶解和生成的速率相等溶解平衡4.难溶物质溶解程度的大小,主要取决于物质本身的性质。但改变外界条件(如浓度、温度等),沉淀溶解平衡会发生移动。已知溶解平衡:Mg(OH)2(s)===Mg2+(aq)+2OH-(aq),请分析当改变下列条件时,对该溶解平衡的影响,填写下表:正向移动正向移动逆向移动正向移动逆向移动不变增大增大增大减小不变增大减小减小增大(图表浓度变化均
指平衡后和原平衡
比较)1.难溶电解质的沉淀溶解平衡
(1)溶解度(S)
在一定温度下,某固态物质在100 g溶剂中达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂中的溶解度,用S表示。
(2)AgCl(s)===Ag+(aq)+Cl-(aq)和AgCl===Ag++Cl-表示的意义
不同:前者表示AgCl的溶解平衡,后者表示AgCl在水中完全电离(是指溶解的那一部分)。(3)沉淀溶解平衡状态的特征
①动态平衡v溶解=v沉淀≠0。
②达到平衡时,溶液中离子的 。
③当改变外界条件时,溶解平衡将 ,达到新的平衡。浓度保持不变发生移动2.外界条件对溶解平衡的影响
(1)温度升高,多数溶解平衡向溶解的方向移动。
(2)加水稀释,浓度减小,溶解平衡向溶解方向移动,但平衡后因仍存在溶解平衡,故离子浓度保持不变。
(3)加入与难溶电解质构成微粒相同的物质,溶解平衡向生成沉淀的方向移动。
(4)加入与难溶电解质溶解所得的离子反应的物质,溶解平衡向溶解的方向移动。 1.把氢氧化钙放入蒸馏水中,一段时间后达到如下平衡:
Ca(OH)2(s)===Ca2+(aq)+2OH-(aq),加入以下物质,可使Ca(OH)2减少的是
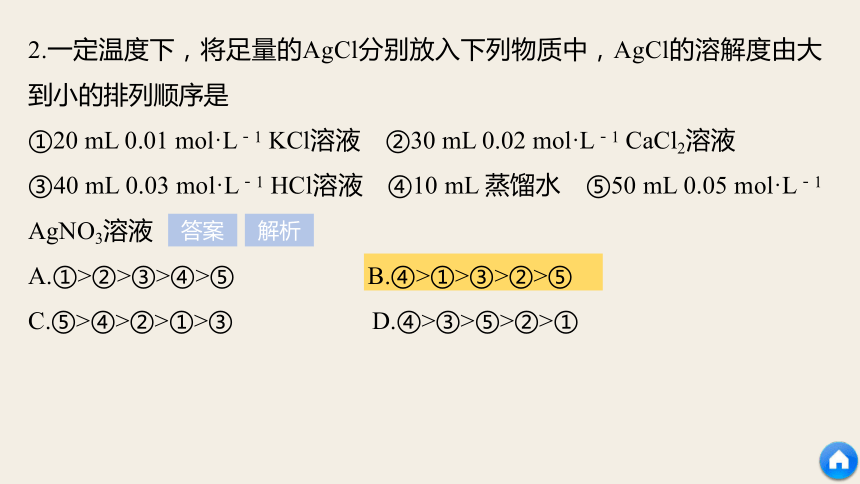
A.Na2S B.AlCl3 C.NaOH D.CaCl2活学活用 答案 解析Na2S水解显碱性,增大了溶液中OH-的浓度;NaOH会提供大量OH-;CaCl2会增大Ca2+的浓度,所以A、C、D选项都会使溶解平衡向生成沉淀的方向移动使Ca(OH)2增多。AlCl3中的Al3+可与OH-发生反应生成Al(OH)3沉淀,使平衡向溶解的方向移动,促进Ca(OH)2的溶解。 2.一定温度下,将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①20 mL 0.01 mol·L-1 KCl溶液 ②30 mL 0.02 mol·L-1 CaCl2溶液
③40 mL 0.03 mol·L-1 HCl溶液 ④10 mL 蒸馏水 ⑤50 mL 0.05 mol·L-1 AgNO3溶液
A.①>②>③>④>⑤ B.④>①>③>②>⑤
C.⑤>④>②>①>③ D.④>③>⑤>②>① 答案 解析AgCl(s)===Ag+(aq)+Cl-(aq),c(Cl-)或c(Ag+)越大,对AgCl的溶解抑制作用越大,AgCl的溶解度就越小。注意AgCl的溶解度大小只与溶液中Ag+或Cl-的浓度有关,而与溶液体积无关。①c(Cl-)=0.01 mol·L-1;
②c(Cl-)=0.04 mol·L-1;③c(Cl-)=0.03 mol·L-1;④c(Cl-)=0 mol·L-1;⑤c(Ag+)=0.05 mol·L-1。Ag+或Cl-浓度由小到大的顺序为④<①<③<②<⑤,故AgCl的溶解度由大到小的排列顺序为④>①>③>②>⑤。二 溶度积常数1.在一定温度下,沉淀达溶解平衡后的溶液为 溶液,其离子浓度
,溶液中各离子浓度幂之积为常数,叫做 (简称 ),用 表示。
2.写出下列沉淀溶解平衡的溶度积常数的表达式
(1)AgCl(s)===Ag+(aq)+Cl-(aq)
Ksp= ;
(2)Fe(OH)3(s)===Fe3+(aq)+3OH-(aq)
Ksp= ;
(3)AmBn(s)===mAn+(aq)+nBm-(aq)
Ksp= 。新知导学饱和不再发生变化溶度积常数溶度积c(Ag+)·c(Cl-)c(Fe3+)·c3(OH-)cm(An+)·cn(Bm-)Ksp3.通过比较溶度积与溶液中有关离子浓度幂的乘积——离子积Qc的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解:
(1)Qc>Ksp,溶液过饱和,有 析出,直至溶液 ,达到新的平衡。
(2)Qc=Ksp,溶液饱和,沉淀与溶解处于 。
(3)Qc(1)溶度积的意义
①溶度积Ksp值的大小只与难溶电解质本身的性质和温度有关,与浓度无关。
②Ksp大小反映难溶电解质的溶解能力,Ksp越小,说明难溶物越难溶解。
③相同类型的电解质,溶度积越小,其溶解度越小。
④不同类型的电解质,溶度积小的电解质的溶解度不一定比溶度积大的溶解度小。(2)根据溶度积能计算出饱和溶液中离子浓度,由溶液体积可计算出溶解的溶质的物质的量,Ksp与S换算时,S的单位必须用物质的量浓度(mol·L-1
或mol·dm-3)。 3.已知25 ℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大
B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
C.温度一定时,当溶液中c(Ag+)·c(Cl-)=Ksp时,此溶液中必有AgCl的沉
淀析出
D.Ksp(AgI)B项混合后可能Ag+或Cl-有剩余,但不一定有c(Ag+)=c(Cl-);
C项Qc=Ksp时达到溶解平衡,没有AgCl沉淀析出;
D项比较物质的溶解度大小时,要注意物质的类型相同且化学式中阴阳离子的个数比相同,溶度积越小,其溶解度也越小。如果不同,则不能直接利用溶度积的大小来比较其溶解性,需转化为溶解度进行比较,否则容易误判。4.向含有AgI的饱和溶液中:
(1)加入AgCl固体,则c(I-)________(填“变大”“变小”或“不变”,下同)。
(2)若改加更多的AgI,则c(Ag+)将________。
(3)若改加AgBr固体,则c(I-)________,而c(Ag+)________。变小不变变小变大 答案沉淀溶解平衡影响平衡移动因素溶度积常数Ksp达标检测 提升技能1.下列有关AgCl沉淀的溶解平衡状态的说法中,正确的是
A.AgCl沉淀的生成和溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl的溶解度不变
D.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变 答案 解析√12345AgCl固体在溶液中存在溶解平衡,所以溶液中有Ag+和Cl-,B错;
升高温度,AgCl溶解度增大,C错;
向平衡体系中加入NaCl固体,增大了c(Cl-),溶解平衡左移,AgCl溶解度减小,D错。2.下列说法正确的是
A.在一定温度下的饱和AgCl水溶液中,Ag+与Cl-的浓度积是一个常数
B.已知AgCl的Ksp=1.8×10-10,则在任何含AgCl固体的溶液中,c(Ag+)
=c(Cl-),且Ag+与Cl-浓度的乘积等于1.8×10-10
C.Ksp数值越大的难溶电解质在水中的溶解能力越强
D.难溶电解质的溶解度很小,故外界条件改变,对它的溶解度没有影响 答案 解析√12345由溶度积常数定义可知,一定温度下Ksp=c(Ag+)·c(Cl-)为一常数,A项正确;
若在含AgCl固体的溶液中溶有NaCl,则c(Ag+)当化学式所表示的组成中阴、阳离子个数比相同时,Ksp越大的难溶电解质在水中的溶解能力越强,C项错误;
难溶电解质的溶解度仍然受外界条件的影响,D项错误。123453.下列说法中,正确的是
A.两种难溶盐电解质,其中Ksp小的溶解度一定小
B.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定
先生成沉淀
C.难溶盐电解质的Ksp与温度有关
D.同离子效应使难溶盐电解质的溶解度变小,也使Ksp变小 答案 解析√Ksp只与难溶电解质的性质和温度有关。123454.已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和CrO ,浓度均为 0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
A.Cl-、Br-、CrO B.CrO 、Br-、Cl-
C.Br-、Cl-、CrO D.Br-、CrO 、Cl- 答案 解析√12345123455.在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=___________ mol·L-1
(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1 mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是____ mol·L-1。 答案 解析123452.2×10-80.2pH=8时,c(OH-)=10-6 mol·L-1,由硫酸铜的沉淀溶解平衡常数可知:Ksp=2.2×10-20=10-12×c(Cu2+),得c(Cu2+)=2.2×10-8 mol·L-1;使Cu2+沉淀完全,已知c(Cu2+)=0.1 mol·L-1,根据反应关系式:Cu2+~2H+得c(H+)=0.2 mol·L-1。本课结束
1.知道沉淀溶解平衡的概念及其影响因素。
2.明确溶度积和离子积的关系,并由此学会判断反应进行的方向。一 难溶电解质的溶解平衡达标检测 提升技能内容索引二 溶度积常数一 难溶电解质的溶解平衡下列物质,属于易溶物质的是 ,属于微溶物质的是 ,属于难溶物质的是 。
①NaCl、②NaOH、③H2SO4、④MgCO3、⑤CaSO4、⑥Ca(OH)2、
⑦CaCO3、⑧BaSO4、⑨Mg(OH)21.不同的固体物质在水中的溶解度不同,有的很大,有的很小,但无论大小,都有一定的溶解度。在20 ℃时,物质的溶解度与溶解性的关系如下:难溶微溶可溶新知导学易溶①②③④⑤⑥⑦⑧⑨2.固体物质的溶解是可逆过程
固体溶质 溶液中的溶质
(1)v溶解 v沉淀 固体溶解
(2)v溶解 v沉淀 溶解平衡
(3)v溶解 v沉淀 析出晶体
3.在一定温度下,当 时,即建立了动态平衡,叫做沉淀 。如AgCl溶于水的溶解平衡表示为
AgCl(s) Ag+(aq)+Cl-(aq)。>=<沉淀溶解和生成的速率相等溶解平衡4.难溶物质溶解程度的大小,主要取决于物质本身的性质。但改变外界条件(如浓度、温度等),沉淀溶解平衡会发生移动。已知溶解平衡:Mg(OH)2(s)===Mg2+(aq)+2OH-(aq),请分析当改变下列条件时,对该溶解平衡的影响,填写下表:正向移动正向移动逆向移动正向移动逆向移动不变增大增大增大减小不变增大减小减小增大(图表浓度变化均
指平衡后和原平衡
比较)1.难溶电解质的沉淀溶解平衡
(1)溶解度(S)
在一定温度下,某固态物质在100 g溶剂中达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂中的溶解度,用S表示。
(2)AgCl(s)===Ag+(aq)+Cl-(aq)和AgCl===Ag++Cl-表示的意义
不同:前者表示AgCl的溶解平衡,后者表示AgCl在水中完全电离(是指溶解的那一部分)。(3)沉淀溶解平衡状态的特征
①动态平衡v溶解=v沉淀≠0。
②达到平衡时,溶液中离子的 。
③当改变外界条件时,溶解平衡将 ,达到新的平衡。浓度保持不变发生移动2.外界条件对溶解平衡的影响
(1)温度升高,多数溶解平衡向溶解的方向移动。
(2)加水稀释,浓度减小,溶解平衡向溶解方向移动,但平衡后因仍存在溶解平衡,故离子浓度保持不变。
(3)加入与难溶电解质构成微粒相同的物质,溶解平衡向生成沉淀的方向移动。
(4)加入与难溶电解质溶解所得的离子反应的物质,溶解平衡向溶解的方向移动。 1.把氢氧化钙放入蒸馏水中,一段时间后达到如下平衡:
Ca(OH)2(s)===Ca2+(aq)+2OH-(aq),加入以下物质,可使Ca(OH)2减少的是
A.Na2S B.AlCl3 C.NaOH D.CaCl2活学活用 答案 解析Na2S水解显碱性,增大了溶液中OH-的浓度;NaOH会提供大量OH-;CaCl2会增大Ca2+的浓度,所以A、C、D选项都会使溶解平衡向生成沉淀的方向移动使Ca(OH)2增多。AlCl3中的Al3+可与OH-发生反应生成Al(OH)3沉淀,使平衡向溶解的方向移动,促进Ca(OH)2的溶解。 2.一定温度下,将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①20 mL 0.01 mol·L-1 KCl溶液 ②30 mL 0.02 mol·L-1 CaCl2溶液
③40 mL 0.03 mol·L-1 HCl溶液 ④10 mL 蒸馏水 ⑤50 mL 0.05 mol·L-1 AgNO3溶液
A.①>②>③>④>⑤ B.④>①>③>②>⑤
C.⑤>④>②>①>③ D.④>③>⑤>②>① 答案 解析AgCl(s)===Ag+(aq)+Cl-(aq),c(Cl-)或c(Ag+)越大,对AgCl的溶解抑制作用越大,AgCl的溶解度就越小。注意AgCl的溶解度大小只与溶液中Ag+或Cl-的浓度有关,而与溶液体积无关。①c(Cl-)=0.01 mol·L-1;
②c(Cl-)=0.04 mol·L-1;③c(Cl-)=0.03 mol·L-1;④c(Cl-)=0 mol·L-1;⑤c(Ag+)=0.05 mol·L-1。Ag+或Cl-浓度由小到大的顺序为④<①<③<②<⑤,故AgCl的溶解度由大到小的排列顺序为④>①>③>②>⑤。二 溶度积常数1.在一定温度下,沉淀达溶解平衡后的溶液为 溶液,其离子浓度
,溶液中各离子浓度幂之积为常数,叫做 (简称 ),用 表示。
2.写出下列沉淀溶解平衡的溶度积常数的表达式
(1)AgCl(s)===Ag+(aq)+Cl-(aq)
Ksp= ;
(2)Fe(OH)3(s)===Fe3+(aq)+3OH-(aq)
Ksp= ;
(3)AmBn(s)===mAn+(aq)+nBm-(aq)
Ksp= 。新知导学饱和不再发生变化溶度积常数溶度积c(Ag+)·c(Cl-)c(Fe3+)·c3(OH-)cm(An+)·cn(Bm-)Ksp3.通过比较溶度积与溶液中有关离子浓度幂的乘积——离子积Qc的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解:
(1)Qc>Ksp,溶液过饱和,有 析出,直至溶液 ,达到新的平衡。
(2)Qc=Ksp,溶液饱和,沉淀与溶解处于 。
(3)Qc
①溶度积Ksp值的大小只与难溶电解质本身的性质和温度有关,与浓度无关。
②Ksp大小反映难溶电解质的溶解能力,Ksp越小,说明难溶物越难溶解。
③相同类型的电解质,溶度积越小,其溶解度越小。
④不同类型的电解质,溶度积小的电解质的溶解度不一定比溶度积大的溶解度小。(2)根据溶度积能计算出饱和溶液中离子浓度,由溶液体积可计算出溶解的溶质的物质的量,Ksp与S换算时,S的单位必须用物质的量浓度(mol·L-1
或mol·dm-3)。 3.已知25 ℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大
B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
C.温度一定时,当溶液中c(Ag+)·c(Cl-)=Ksp时,此溶液中必有AgCl的沉
淀析出
D.Ksp(AgI)
C项Qc=Ksp时达到溶解平衡,没有AgCl沉淀析出;
D项比较物质的溶解度大小时,要注意物质的类型相同且化学式中阴阳离子的个数比相同,溶度积越小,其溶解度也越小。如果不同,则不能直接利用溶度积的大小来比较其溶解性,需转化为溶解度进行比较,否则容易误判。4.向含有AgI的饱和溶液中:
(1)加入AgCl固体,则c(I-)________(填“变大”“变小”或“不变”,下同)。
(2)若改加更多的AgI,则c(Ag+)将________。
(3)若改加AgBr固体,则c(I-)________,而c(Ag+)________。变小不变变小变大 答案沉淀溶解平衡影响平衡移动因素溶度积常数Ksp达标检测 提升技能1.下列有关AgCl沉淀的溶解平衡状态的说法中,正确的是
A.AgCl沉淀的生成和溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl的溶解度不变
D.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变 答案 解析√12345AgCl固体在溶液中存在溶解平衡,所以溶液中有Ag+和Cl-,B错;
升高温度,AgCl溶解度增大,C错;
向平衡体系中加入NaCl固体,增大了c(Cl-),溶解平衡左移,AgCl溶解度减小,D错。2.下列说法正确的是
A.在一定温度下的饱和AgCl水溶液中,Ag+与Cl-的浓度积是一个常数
B.已知AgCl的Ksp=1.8×10-10,则在任何含AgCl固体的溶液中,c(Ag+)
=c(Cl-),且Ag+与Cl-浓度的乘积等于1.8×10-10
C.Ksp数值越大的难溶电解质在水中的溶解能力越强
D.难溶电解质的溶解度很小,故外界条件改变,对它的溶解度没有影响 答案 解析√12345由溶度积常数定义可知,一定温度下Ksp=c(Ag+)·c(Cl-)为一常数,A项正确;
若在含AgCl固体的溶液中溶有NaCl,则c(Ag+)
难溶电解质的溶解度仍然受外界条件的影响,D项错误。123453.下列说法中,正确的是
A.两种难溶盐电解质,其中Ksp小的溶解度一定小
B.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定
先生成沉淀
C.难溶盐电解质的Ksp与温度有关
D.同离子效应使难溶盐电解质的溶解度变小,也使Ksp变小 答案 解析√Ksp只与难溶电解质的性质和温度有关。123454.已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和CrO ,浓度均为 0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
A.Cl-、Br-、CrO B.CrO 、Br-、Cl-
C.Br-、Cl-、CrO D.Br-、CrO 、Cl- 答案 解析√12345123455.在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=___________ mol·L-1
(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1 mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是____ mol·L-1。 答案 解析123452.2×10-80.2pH=8时,c(OH-)=10-6 mol·L-1,由硫酸铜的沉淀溶解平衡常数可知:Ksp=2.2×10-20=10-12×c(Cu2+),得c(Cu2+)=2.2×10-8 mol·L-1;使Cu2+沉淀完全,已知c(Cu2+)=0.1 mol·L-1,根据反应关系式:Cu2+~2H+得c(H+)=0.2 mol·L-1。本课结束
