人教版高中化学选修四3.4.2沉淀反应的应用 课件
文档属性
| 名称 | 人教版高中化学选修四3.4.2沉淀反应的应用 课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-11-19 00:00:00 | ||
图片预览











文档简介
课件37张PPT。第2课时 沉淀反应的应用第三章 第四节学习目标定位
1.能用平衡移动原理分析理解沉淀的溶解与生成、沉淀转化的实质。
2.学会用沉淀溶解平衡的移动解决生产、生活中的实际问题。一 沉淀的生成与溶解达标检测 提升技能二 沉淀的转化内容索引一 沉淀的生成与溶解1.某含有CaCO3的悬浊液,改变条件,回答下列问题:
(1)滴加盐酸直至过量,沉淀逐渐溶解。原因是______________________
__________________________________________________________________________________________________________________________。
(2)加入Na2CO3溶液,沉淀 ,c(Ca2+) ,c(CO ) 。新知导学增多减小增大CaCO3在水中存在,2.沉淀生成的应用主要涉及无机制备、提纯工艺的生产、科研、废水处理等领域,常利用生成沉淀达到分离或除去某些离子的目的。常用的方法有:
(1)调节pH法:如工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入氨水调节pH至7~8,可使Fe3+转变为 沉淀而除去。反应如下: 。Fe(OH)3Fe3++3NH3·H2O===Fe(OH)3↓+3NH(2)加沉淀剂法:如以Na2S、H2S等作沉淀剂,使某些金属离子,如Cu2+、Hg2+等生成极难溶的 等沉淀,也是分离、除去杂质常用的方法。
写出下列反应的离子方程式:
①用H2S除去Cu2+: 。
②用Na2S除去Hg2+: 。硫化物CuS、HgSH2S+Cu2+===CuS↓+2H+Hg2++S2-===HgS↓3.根据沉淀溶解平衡,分析回答下列问题:
(1)BaCO3和BaSO4都难溶于水,在医学上常用BaSO4作钡餐透视,而不能用BaCO3的原因是什么? 答案(2)可溶性钡盐(如BaCl2等)当作食盐食用,会造成钡中毒。中毒患者常用5.0%的Na2SO4溶液洗胃的原因是什么? 答案沉淀反应的应用
(1)沉淀的生成和溶解这两个方向相反的过程,控制离子浓度,可以使反应向我们需要的方向转化。
(2)利用生成沉淀除去某种离子,首先要使生成沉淀的反应能够发生,其次沉淀生成的反应进行得越完全越好。
(3)根据平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去溶解平衡体系中的 ,使平衡向 的方向移动,就可以使沉淀溶解。如常用强酸溶解CaCO3、FeS、Al(OH)3、Cu(OH)2等难溶电解质。相应离子沉淀溶解 1.为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入的一种试剂是
A.NH3·H2O B.NaOH
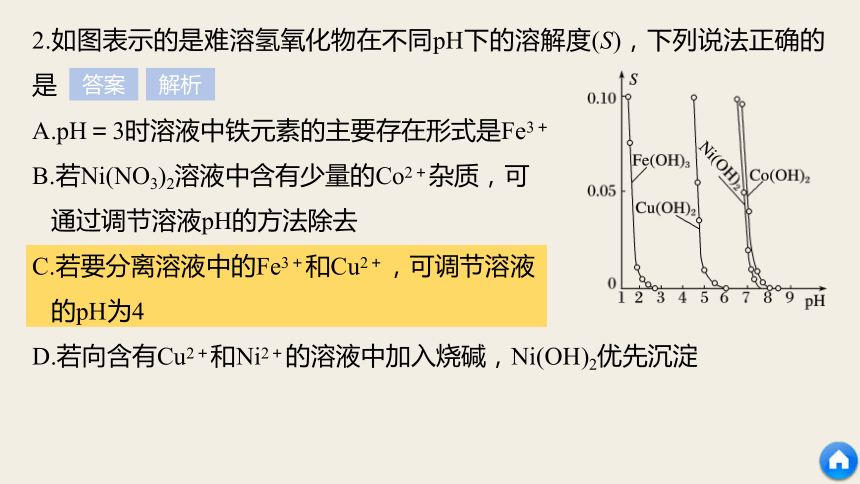
C.Na2CO3 D.MgCO3活学活用 答案 解析Fe3++3H2O??Fe(OH)3+3H+,调节pH,可使Fe3+转化为Fe(OH)3沉淀后除去。在不引入新杂质,Mg2+不沉淀的条件下,选用MgCO3,过量的MgCO3可一起过滤除去。也可选用MgO、Mg(OH)2等试剂。 2.如图表示的是难溶氢氧化物在不同pH下的溶解度(S),下列说法正确的是
A.pH=3时溶液中铁元素的主要存在形式是Fe3+
B.若Ni(NO3)2溶液中含有少量的Co2+杂质,可
通过调节溶液pH的方法除去
C.若要分离溶液中的Fe3+和Cu2+,可调节溶液
的pH为4
D.若向含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀 答案 解析当pH=3时,Fe3+已沉淀完全,A项错误;
由于Ni2+和Co2+完全沉淀时的pH相差不大,故不宜通过调节溶液pH的方法除去,B项错误;
根据图可知向含有Cu2+和Ni2+的溶液中加入烧碱,Cu(OH)2优先沉淀,D项错误。二 沉淀的转化(1)写出各步反应的离子方程式:
① ;
② ;
③ 。
(2)由上述实验得出的结论是
。1.根据下列图示完成实验,将观察到的现象填在空格内:Ag++Cl-===AgCl↓AgCl(s)+I-(aq)===AgI(s)+Cl-(aq)新知探究2AgI(s)+S2-(aq)===Ag2S↓(s)+2I-(aq)溶解能力小的沉淀能转化为溶解能力更小白色
沉淀黄色
沉淀黑色
沉淀的沉淀2.沉淀转化在生活中的应用
(1)工业废水处理过程中,重金属离子可利用沉淀转化原理用FeS等难溶物转化为HgS、Ag2S、PbS等沉淀。写出用FeS除去Hg2+的离子方程式:
。FeS(s)+Hg2+(aq)===HgS(s)+Fe2+(aq)(2)硬水煮沸形成的水垢主要成分是CaCO3和Mg(OH)2,说明它形成的原因(用离子方程式表示)。
,
,
。(3)锅炉形成的水垢中常含有CaSO4,除去方法是CaSO4(s) CaCO3(s)
Ca2+(aq),写出有关反应的化学方程式:_____________________
。
(4)原生铜硫化物的转化如下:
原生铜硫化物 CuSO4(溶液) CuS(铜蓝)。写出CuSO4转化为铜蓝的化学方程式: 。 CuSO4(aq)+ZnS(s)===CuS(s)+ZnSO4(aq),CuSO4(aq)+PbS(s)===CuS(s)+PbSO4(s) CaSO4(s)+Na2CO3(aq) ===
CaCO3(s)+Na2SO4(aq),CaCO3+2HCl===CaCl2+H2O+CO2↑沉淀的转化
(1)沉淀转化的实质就是 。
(2)一般说来,溶解度小的沉淀转化为溶解度更小的沉淀容易实现;两者差别越大,沉淀转化越容易。
(3)组成类型相同的难溶电解质,Ksp较大的难溶电解质能转化为Ksp较小的难溶电解质。
(4)Ksp相差不大的难溶电解质,Ksp较小的难溶电解质在一定条件下可以转化为Ksp较大的难溶电解质。沉淀溶解平衡的移动 3.25 ℃时,三种难溶银盐的Ksp与颜色如下表,下列说法正确的是活学活用A.AgCl、Ag2CrO4、AgI饱和溶液中c(Ag+)依次减小
B.Ag2CrO4饱和溶液中c(Ag+)约为1.0×10-6 mol·L-1
C.向AgCl悬浊液中加入足量KI溶液,沉淀将由白色转化为黄色
D.向等浓度的KCl与K2CrO4的混合溶液中滴加少量AgNO3溶液,将生成
砖红色沉淀 答案 解析
溶解度小的沉淀可转化为溶解度更小的沉淀,所以向AgCl悬浊液中加入足量KI溶液,会有黄色沉淀产生,C正确。4.已知25 ℃:某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,实验步骤如下:
①向0.1 mol·L-1的CaCl2溶液100 mL中加入0.1 mol·L-1的Na2SO4溶液100 mL,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3 g,搅拌,静置沉淀后弃去上层清液。
③再加入蒸馏水搅拌,静置后再弃去上层清液。
④___________________________________________________________。(1)由题中信息Ksp越大,表示电解质的溶解度越______(填“大”或“小”)。大(2)写出第②步发生的化学反应方程式:____________________________
_______________________。Na2CO3(aq)+CaSO4(s)===CaCO3(s)+Na2SO4(aq)(3)设计第③步的目的是_______________________。(4)请补充第④步操作及发生的现象:______________________________
________________________________。向沉淀中加入足量的盐酸,沉淀完全溶解,并放出无色无味的气体(5)请写出该原理在实际生活、生产中的一个应用: _________________
________________________________。 将锅炉水垢中的
CaSO4转化为CaCO3,再用盐酸除去 答案 解析Ksp越大,表示电解质的溶解度越大,溶解度大的沉淀会向溶解度小的沉淀转化,要证明CaSO4完全转化为CaCO3,可以加入盐酸,因为CaSO4不和盐酸反应,而CaCO3可完全溶于盐酸。在实际生活、生产中利用此反应可以将锅炉水垢中的CaSO4转化为CaCO3再用盐酸除去。达标检测 提升技能1.已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16。下列说法错误的是
A.AgCl不溶于水,不能转化为AgI
B.在含有浓度均为0.001 mol·L-1的Cl-、I-的溶液中缓慢加入AgNO3稀
溶液,首先析出AgI沉淀
C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不
低于 ×10-11 mol·L-1 答案 解析√1234组成结构相似的物质,溶度积越小,其溶解度越小,越易先形成沉淀,B项正确;
溶解度小的沉淀转化成溶解度更小的沉淀容易实现,所以A项错、C项正确;12342.已知如下物质的溶度积常数:Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36。下列说法正确的是
A.同温度下,CuS的溶解度大于FeS的溶解度
B.同温度下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)变小
C.向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,
最先出现的沉淀是FeS
D.除去工业废水中的Cu2+和Hg2+,可以选用FeS作沉淀剂 答案 解析√1234A项,由于FeS的Ksp大,且FeS与CuS的Ksp表达式是相同类型的,因此FeS的溶解度比CuS的大;
B项,Ksp不随浓度变化而变化,它只与温度有关;
C项,先达到CuS的Ksp,先出现CuS沉淀;
D项,向含有Cu2+的工业废水中加入FeS,FeS会转化为更难溶的CuS和HgS,可以用FeS作沉淀剂。12343.实验:①0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1NaCl溶液等体积混合得到悬浊液a,过滤得到滤液b和白色沉淀c;②向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为黄色。
下列说法不正确的是
A.悬浊液a中存在沉淀溶解平衡:AgCl(s)===Ag+(aq)+Cl-(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶 答案 解析√1234在悬浊液a中,存在AgCl的沉淀溶解平衡,即在滤液b中,仍含有少量Ag+,故在b中生成了AgI沉淀,A正确,B错误;
向白色沉淀AgCl中滴加KI溶液生成黄色AgI,由此可说明AgI比AgCl更难溶,C项和D项都正确。1234已知Cu2+、Fe2+在pH为4~5时不水解,而Fe3+却几乎完全水解而沉淀。请回答下列问题:
(1)X是什么物质?______。其反应的离子方程式是
_________________________。4.工业上制取纯净的CuCl2·2H2O的主要过程是①将粗氧化铜(含少量Fe)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;②对①所得滤液按下列步骤进行操作: 答案 解析Cl2Cl2+2Fe2+===2Fe3++2Cl-1234根据框图,加入氧化剂X可把Fe2+氧化为Fe3+,而没有增加新杂质,所以X为Cl2。1234(2)加入Y物质的作用是_________________________________________,
生产中Y可选________________。 答案 解析调节溶液pH,使pH为4~5,且不引进新杂质CuO或Cu(OH)2结合提示,调节pH至4~5,使Fe3+全部沉淀,同样不引进新杂质,所以Y最好为CuO或Cu(OH)2。1234(3)溶液乙在蒸发结晶时应注意_____________________________________
_________。 答案 解析通入HCl气体(或加入盐酸),并不断搅拌且不能蒸干CuCl2溶液在蒸发结晶过程中发生水解,为抑制其水解,根据Cu2++2H2O===Cu(OH)2+2H+,加入盐酸可抑制其水解,在蒸发过程中要不断搅拌且不能蒸干。1234本课结束
1.能用平衡移动原理分析理解沉淀的溶解与生成、沉淀转化的实质。
2.学会用沉淀溶解平衡的移动解决生产、生活中的实际问题。一 沉淀的生成与溶解达标检测 提升技能二 沉淀的转化内容索引一 沉淀的生成与溶解1.某含有CaCO3的悬浊液,改变条件,回答下列问题:
(1)滴加盐酸直至过量,沉淀逐渐溶解。原因是______________________
__________________________________________________________________________________________________________________________。
(2)加入Na2CO3溶液,沉淀 ,c(Ca2+) ,c(CO ) 。新知导学增多减小增大CaCO3在水中存在,2.沉淀生成的应用主要涉及无机制备、提纯工艺的生产、科研、废水处理等领域,常利用生成沉淀达到分离或除去某些离子的目的。常用的方法有:
(1)调节pH法:如工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入氨水调节pH至7~8,可使Fe3+转变为 沉淀而除去。反应如下: 。Fe(OH)3Fe3++3NH3·H2O===Fe(OH)3↓+3NH(2)加沉淀剂法:如以Na2S、H2S等作沉淀剂,使某些金属离子,如Cu2+、Hg2+等生成极难溶的 等沉淀,也是分离、除去杂质常用的方法。
写出下列反应的离子方程式:
①用H2S除去Cu2+: 。
②用Na2S除去Hg2+: 。硫化物CuS、HgSH2S+Cu2+===CuS↓+2H+Hg2++S2-===HgS↓3.根据沉淀溶解平衡,分析回答下列问题:
(1)BaCO3和BaSO4都难溶于水,在医学上常用BaSO4作钡餐透视,而不能用BaCO3的原因是什么? 答案(2)可溶性钡盐(如BaCl2等)当作食盐食用,会造成钡中毒。中毒患者常用5.0%的Na2SO4溶液洗胃的原因是什么? 答案沉淀反应的应用
(1)沉淀的生成和溶解这两个方向相反的过程,控制离子浓度,可以使反应向我们需要的方向转化。
(2)利用生成沉淀除去某种离子,首先要使生成沉淀的反应能够发生,其次沉淀生成的反应进行得越完全越好。
(3)根据平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去溶解平衡体系中的 ,使平衡向 的方向移动,就可以使沉淀溶解。如常用强酸溶解CaCO3、FeS、Al(OH)3、Cu(OH)2等难溶电解质。相应离子沉淀溶解 1.为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入的一种试剂是
A.NH3·H2O B.NaOH
C.Na2CO3 D.MgCO3活学活用 答案 解析Fe3++3H2O??Fe(OH)3+3H+,调节pH,可使Fe3+转化为Fe(OH)3沉淀后除去。在不引入新杂质,Mg2+不沉淀的条件下,选用MgCO3,过量的MgCO3可一起过滤除去。也可选用MgO、Mg(OH)2等试剂。 2.如图表示的是难溶氢氧化物在不同pH下的溶解度(S),下列说法正确的是
A.pH=3时溶液中铁元素的主要存在形式是Fe3+
B.若Ni(NO3)2溶液中含有少量的Co2+杂质,可
通过调节溶液pH的方法除去
C.若要分离溶液中的Fe3+和Cu2+,可调节溶液
的pH为4
D.若向含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀 答案 解析当pH=3时,Fe3+已沉淀完全,A项错误;
由于Ni2+和Co2+完全沉淀时的pH相差不大,故不宜通过调节溶液pH的方法除去,B项错误;
根据图可知向含有Cu2+和Ni2+的溶液中加入烧碱,Cu(OH)2优先沉淀,D项错误。二 沉淀的转化(1)写出各步反应的离子方程式:
① ;
② ;
③ 。
(2)由上述实验得出的结论是
。1.根据下列图示完成实验,将观察到的现象填在空格内:Ag++Cl-===AgCl↓AgCl(s)+I-(aq)===AgI(s)+Cl-(aq)新知探究2AgI(s)+S2-(aq)===Ag2S↓(s)+2I-(aq)溶解能力小的沉淀能转化为溶解能力更小白色
沉淀黄色
沉淀黑色
沉淀的沉淀2.沉淀转化在生活中的应用
(1)工业废水处理过程中,重金属离子可利用沉淀转化原理用FeS等难溶物转化为HgS、Ag2S、PbS等沉淀。写出用FeS除去Hg2+的离子方程式:
。FeS(s)+Hg2+(aq)===HgS(s)+Fe2+(aq)(2)硬水煮沸形成的水垢主要成分是CaCO3和Mg(OH)2,说明它形成的原因(用离子方程式表示)。
,
,
。(3)锅炉形成的水垢中常含有CaSO4,除去方法是CaSO4(s) CaCO3(s)
Ca2+(aq),写出有关反应的化学方程式:_____________________
。
(4)原生铜硫化物的转化如下:
原生铜硫化物 CuSO4(溶液) CuS(铜蓝)。写出CuSO4转化为铜蓝的化学方程式: 。 CuSO4(aq)+ZnS(s)===CuS(s)+ZnSO4(aq),CuSO4(aq)+PbS(s)===CuS(s)+PbSO4(s) CaSO4(s)+Na2CO3(aq) ===
CaCO3(s)+Na2SO4(aq),CaCO3+2HCl===CaCl2+H2O+CO2↑沉淀的转化
(1)沉淀转化的实质就是 。
(2)一般说来,溶解度小的沉淀转化为溶解度更小的沉淀容易实现;两者差别越大,沉淀转化越容易。
(3)组成类型相同的难溶电解质,Ksp较大的难溶电解质能转化为Ksp较小的难溶电解质。
(4)Ksp相差不大的难溶电解质,Ksp较小的难溶电解质在一定条件下可以转化为Ksp较大的难溶电解质。沉淀溶解平衡的移动 3.25 ℃时,三种难溶银盐的Ksp与颜色如下表,下列说法正确的是活学活用A.AgCl、Ag2CrO4、AgI饱和溶液中c(Ag+)依次减小
B.Ag2CrO4饱和溶液中c(Ag+)约为1.0×10-6 mol·L-1
C.向AgCl悬浊液中加入足量KI溶液,沉淀将由白色转化为黄色
D.向等浓度的KCl与K2CrO4的混合溶液中滴加少量AgNO3溶液,将生成
砖红色沉淀 答案 解析
溶解度小的沉淀可转化为溶解度更小的沉淀,所以向AgCl悬浊液中加入足量KI溶液,会有黄色沉淀产生,C正确。4.已知25 ℃:某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,实验步骤如下:
①向0.1 mol·L-1的CaCl2溶液100 mL中加入0.1 mol·L-1的Na2SO4溶液100 mL,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3 g,搅拌,静置沉淀后弃去上层清液。
③再加入蒸馏水搅拌,静置后再弃去上层清液。
④___________________________________________________________。(1)由题中信息Ksp越大,表示电解质的溶解度越______(填“大”或“小”)。大(2)写出第②步发生的化学反应方程式:____________________________
_______________________。Na2CO3(aq)+CaSO4(s)===CaCO3(s)+Na2SO4(aq)(3)设计第③步的目的是_______________________。(4)请补充第④步操作及发生的现象:______________________________
________________________________。向沉淀中加入足量的盐酸,沉淀完全溶解,并放出无色无味的气体(5)请写出该原理在实际生活、生产中的一个应用: _________________
________________________________。 将锅炉水垢中的
CaSO4转化为CaCO3,再用盐酸除去 答案 解析Ksp越大,表示电解质的溶解度越大,溶解度大的沉淀会向溶解度小的沉淀转化,要证明CaSO4完全转化为CaCO3,可以加入盐酸,因为CaSO4不和盐酸反应,而CaCO3可完全溶于盐酸。在实际生活、生产中利用此反应可以将锅炉水垢中的CaSO4转化为CaCO3再用盐酸除去。达标检测 提升技能1.已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16。下列说法错误的是
A.AgCl不溶于水,不能转化为AgI
B.在含有浓度均为0.001 mol·L-1的Cl-、I-的溶液中缓慢加入AgNO3稀
溶液,首先析出AgI沉淀
C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不
低于 ×10-11 mol·L-1 答案 解析√1234组成结构相似的物质,溶度积越小,其溶解度越小,越易先形成沉淀,B项正确;
溶解度小的沉淀转化成溶解度更小的沉淀容易实现,所以A项错、C项正确;12342.已知如下物质的溶度积常数:Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36。下列说法正确的是
A.同温度下,CuS的溶解度大于FeS的溶解度
B.同温度下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)变小
C.向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,
最先出现的沉淀是FeS
D.除去工业废水中的Cu2+和Hg2+,可以选用FeS作沉淀剂 答案 解析√1234A项,由于FeS的Ksp大,且FeS与CuS的Ksp表达式是相同类型的,因此FeS的溶解度比CuS的大;
B项,Ksp不随浓度变化而变化,它只与温度有关;
C项,先达到CuS的Ksp,先出现CuS沉淀;
D项,向含有Cu2+的工业废水中加入FeS,FeS会转化为更难溶的CuS和HgS,可以用FeS作沉淀剂。12343.实验:①0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1NaCl溶液等体积混合得到悬浊液a,过滤得到滤液b和白色沉淀c;②向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为黄色。
下列说法不正确的是
A.悬浊液a中存在沉淀溶解平衡:AgCl(s)===Ag+(aq)+Cl-(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶 答案 解析√1234在悬浊液a中,存在AgCl的沉淀溶解平衡,即在滤液b中,仍含有少量Ag+,故在b中生成了AgI沉淀,A正确,B错误;
向白色沉淀AgCl中滴加KI溶液生成黄色AgI,由此可说明AgI比AgCl更难溶,C项和D项都正确。1234已知Cu2+、Fe2+在pH为4~5时不水解,而Fe3+却几乎完全水解而沉淀。请回答下列问题:
(1)X是什么物质?______。其反应的离子方程式是
_________________________。4.工业上制取纯净的CuCl2·2H2O的主要过程是①将粗氧化铜(含少量Fe)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;②对①所得滤液按下列步骤进行操作: 答案 解析Cl2Cl2+2Fe2+===2Fe3++2Cl-1234根据框图,加入氧化剂X可把Fe2+氧化为Fe3+,而没有增加新杂质,所以X为Cl2。1234(2)加入Y物质的作用是_________________________________________,
生产中Y可选________________。 答案 解析调节溶液pH,使pH为4~5,且不引进新杂质CuO或Cu(OH)2结合提示,调节pH至4~5,使Fe3+全部沉淀,同样不引进新杂质,所以Y最好为CuO或Cu(OH)2。1234(3)溶液乙在蒸发结晶时应注意_____________________________________
_________。 答案 解析通入HCl气体(或加入盐酸),并不断搅拌且不能蒸干CuCl2溶液在蒸发结晶过程中发生水解,为抑制其水解,根据Cu2++2H2O===Cu(OH)2+2H+,加入盐酸可抑制其水解,在蒸发过程中要不断搅拌且不能蒸干。1234本课结束
