物质的聚集状态[上学期]
图片预览



文档简介
课件15张PPT。 物质的聚集状态洪家中学 黄颖 固态、液态和气态结构与性质分析 微观结构
运动方式
宏观性质
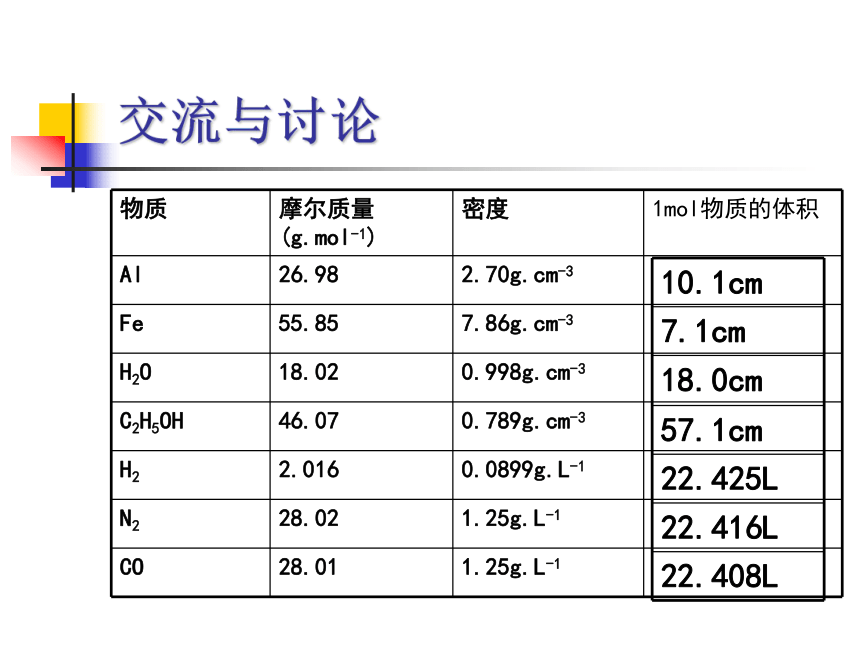
不同聚集状态的物质在微观结构上的差异,导致了物质性质上的不同交流与讨论小结:1:相同条件下,1mol的不同物质的体积是不同的
V(固)2:相同条件下,1mol气体所占的体积是近似相等的
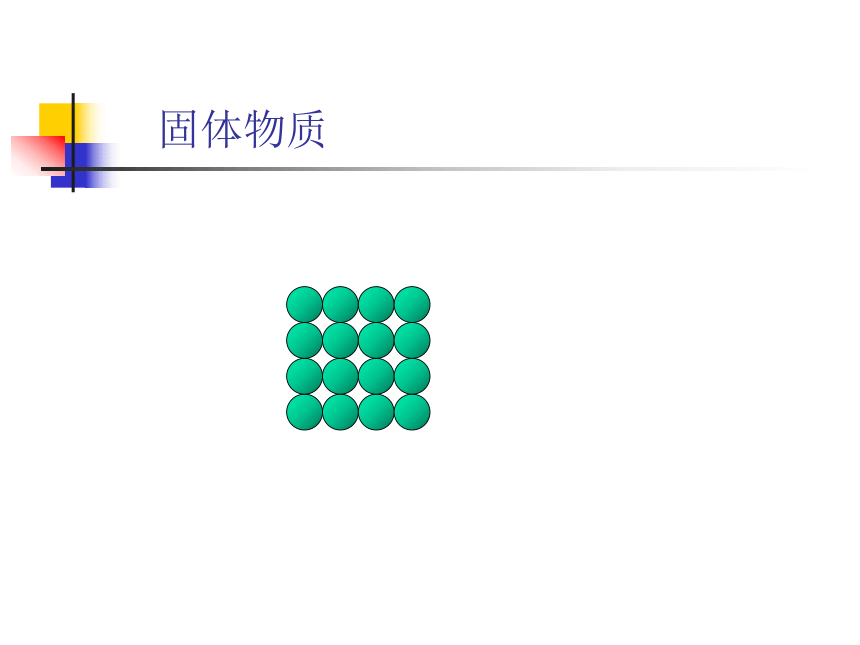
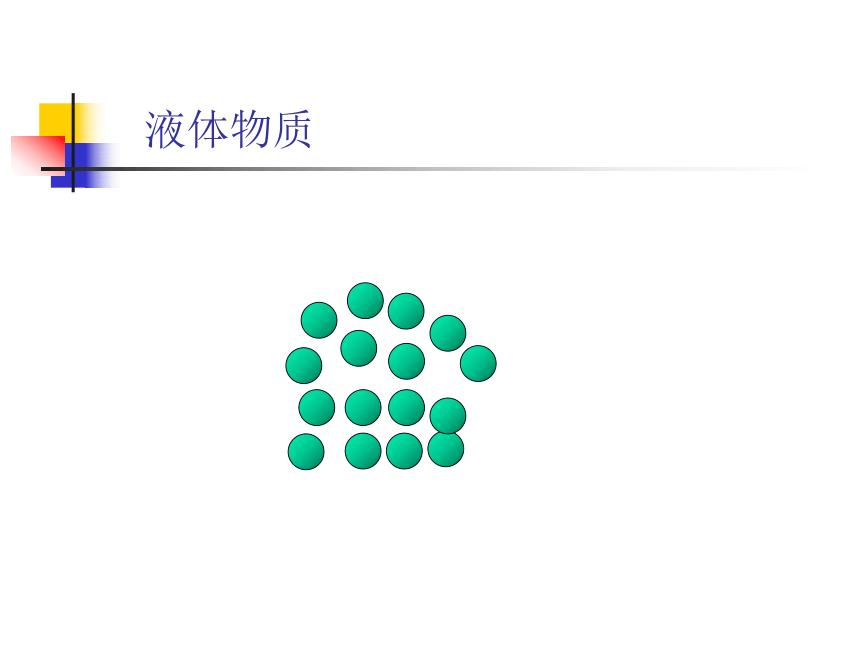
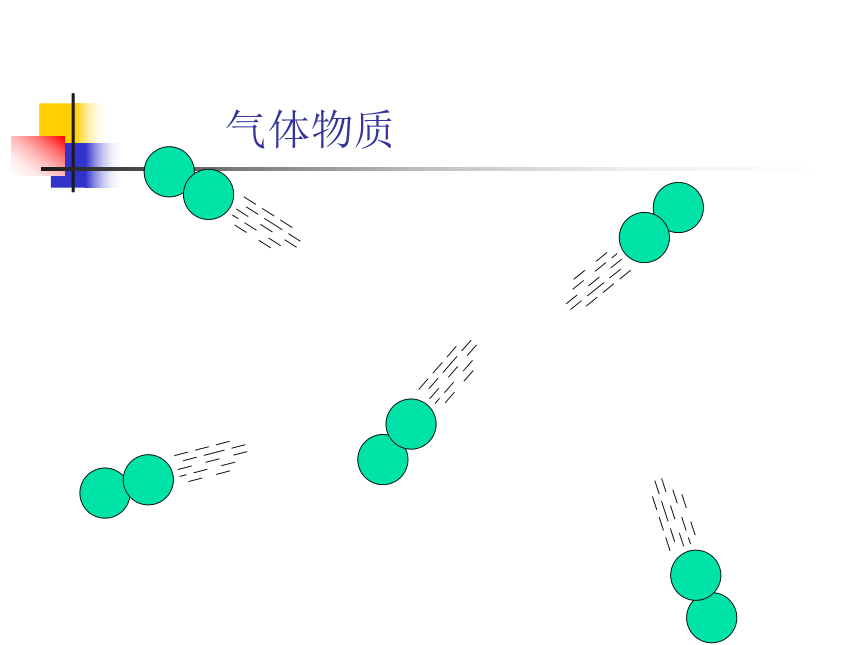
为什么? 固体物质 液体物质 气体物质问题探究:相同条件下,影响物质体积的主要因素微粒本身的大小
微粒数目
微粒间的平均距离固体和液体气 体思考:
为什么要强调,在相同条件下,1mol气体所占的体积才是近似相等的?
温度、压强这两个条件又受什么因素影响?对气体分子间平均距离(或气体体积)产生怎样影响?压强增大使得分子间距离减小,而使气体体积缩小温度升高,分子间距离增大,而使气体体积膨胀气体的摩尔体积(Vm)1、定义:单位物质的量的气体所占的体积
2、单位:L·mol-1或m3·mol-1
3、影响因素:
? ①温度越高,体积越大
? ②压强越大,体积越小
在标准状况( 273K 、 101 kPa)时,1 mol任何气体的体积都约是 22.4 L 课堂练习判断下列叙述是否正确
A .标况下,1mol任何物质的体积都约为 22.4 L
B . 1mol气体的体积约为22.4 L
C. 1mol氖气和1mol氧气体积相同
D.标准状况下, 1mol氧气和氮气混合气(任意比)的体积约为22.4 L
E.22.4 L气体所含分子数一定大于11.2 L气体所含分子数
F. 只有在标况下,气体的摩尔体积才能是22.4 L注意下列几个问题:(1)22.4 L是1 mol任何气体(可以是混合气体)在标准状况下的体积,因此在非标准状况时一般不使用22.4 L·mol-1。
(2)只适用于气态物质,对于固态物质和液态物质来讲是不适用的。
(3) 22.4 L·mol-1这个数值是特定条件下的气体摩尔体积,但不仅仅是标准状况下的气体摩尔体积。 气体摩尔体积的表达式:Vm = V / n气体物质的量 n 气体的质量m
÷M×M×NA÷NA气体的体积V×Vm÷Vm气体分子数 N
运动方式
宏观性质
不同聚集状态的物质在微观结构上的差异,导致了物质性质上的不同交流与讨论小结:1:相同条件下,1mol的不同物质的体积是不同的
V(固)
为什么? 固体物质 液体物质 气体物质问题探究:相同条件下,影响物质体积的主要因素微粒本身的大小
微粒数目
微粒间的平均距离固体和液体气 体思考:
为什么要强调,在相同条件下,1mol气体所占的体积才是近似相等的?
温度、压强这两个条件又受什么因素影响?对气体分子间平均距离(或气体体积)产生怎样影响?压强增大使得分子间距离减小,而使气体体积缩小温度升高,分子间距离增大,而使气体体积膨胀气体的摩尔体积(Vm)1、定义:单位物质的量的气体所占的体积
2、单位:L·mol-1或m3·mol-1
3、影响因素:
? ①温度越高,体积越大
? ②压强越大,体积越小
在标准状况( 273K 、 101 kPa)时,1 mol任何气体的体积都约是 22.4 L 课堂练习判断下列叙述是否正确
A .标况下,1mol任何物质的体积都约为 22.4 L
B . 1mol气体的体积约为22.4 L
C. 1mol氖气和1mol氧气体积相同
D.标准状况下, 1mol氧气和氮气混合气(任意比)的体积约为22.4 L
E.22.4 L气体所含分子数一定大于11.2 L气体所含分子数
F. 只有在标况下,气体的摩尔体积才能是22.4 L注意下列几个问题:(1)22.4 L是1 mol任何气体(可以是混合气体)在标准状况下的体积,因此在非标准状况时一般不使用22.4 L·mol-1。
(2)只适用于气态物质,对于固态物质和液态物质来讲是不适用的。
(3) 22.4 L·mol-1这个数值是特定条件下的气体摩尔体积,但不仅仅是标准状况下的气体摩尔体积。 气体摩尔体积的表达式:Vm = V / n气体物质的量 n 气体的质量m
÷M×M×NA÷NA气体的体积V×Vm÷Vm气体分子数 N
