物质的检验[上学期]
图片预览








文档简介
课件26张PPT。常 见 物 质 的 检 验问题:如何检验某物质中是否含有碳酸盐?我们检验物质的依据是什么?问题:氯化铵、硫酸铵、氯化钾、硫酸钾均可用作化肥,请写出上述盐在溶液中电离的方程式。 活动与探究:完成实验1、实验2、实验3 请同学们:规范操作、注意安全1、对液体加热时,先均匀加热, 且试管口不准对着人
2、湿润的红色石蕊试纸不要接触到试管口
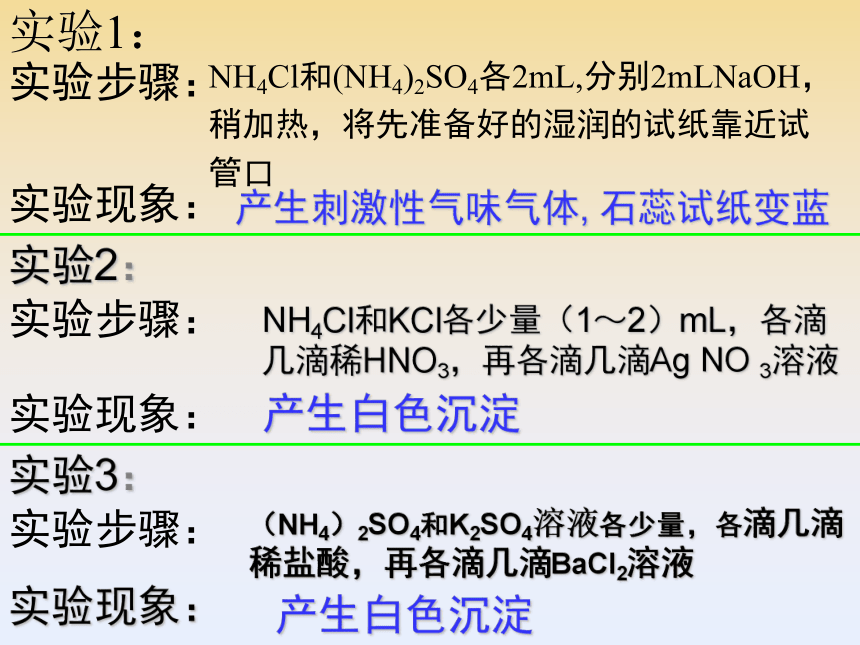
3、所加试剂的量要适量,不可浪费。4、结束时把废液到在废液缸(塑料烧杯中)。实验1:NH4Cl和(NH4)2SO4各2mL,分别2mLNaOH,
稍加热,将先准备好的湿润的试纸靠近试
管口实验步骤:实验现象:实验2:实验步骤:NH4Cl和KCl各少量(1~2)mL,各滴几滴稀HNO3,再各滴几滴Ag NO 3溶液实验现象:实验3:实验步骤:(NH4)2SO4和K2SO4溶液各少量,各滴几滴稀盐酸,再各滴几滴BaCl2溶液实验现象:产生刺激性气味气体, 石蕊试纸变蓝产生白色沉淀产生白色沉淀 取样(少量放在试管中)与碱混合加热,若有刺激性气味的气体产生,且该气使湿润的红色石蕊试纸变蓝,证明该试样中含有NH4+。
1、NH4+的检验(铵盐)
方法:实验原理:
蓝取样并向内加稀HNO3和AgNO3溶液,若生成白色沉淀,证明该试样中含有Cl- 。
2、Cl-的检验(盐酸盐或称氯化物)
方法:实验原理KCl+AgNO3=AgCl↓+KNO3稀硝酸的作用是什么?排除CO32-等的干扰
取样并向内加稀HCl、BaCl2溶液,若生成白色沉淀,证明该试样中含有SO42- 。3、SO42-的检验(硫酸盐)
方法:思考:
稀盐酸的作用?除去CO32-等的干扰实验原理Na2SO4+BaCl2=BaSO4↓+2NaCl如何检验刚才的蓝色溶液是否为CuCl2 ?
4. K+ 、 Na+的检验Na 为黄色 K为紫色焰色反应(许多金属或它们的化合物在灼烧时都会使火焰呈现出特殊的颜色,这叫做焰色反应)P20表1-5 一些物质的检验有烧焦羽毛的气味灼烧丝绸制品变蓝与碘水反应淀粉紫色石蕊变蓝;PH试纸变色PH>7
用紫色石蕊试液;用PH试纸碱
(OH-)紫色石蕊变红;PH试纸变色PH<7用紫色石蕊试液;用PH试纸酸
(H+)有气体产生,澄清石灰水变浑浊与盐酸反应,产生气体通入澄清石灰水碳酸盐
(CO32-)现象检验方法待检物质用红外光谱仪来确定:物质中是否含有某些有机基团用元素分析仪测定:物质中是否含C、H、O、N、S等元素5. 仪器分析法:课本P21用原子吸收光谱确定:物质中是否含有哪些金属元素1、人人都会出汗,汗液中含有NaCl,请设计实验加以证明。练习2、能用来区别BaCl2、NaCl、Na2CO3三种物质的
试剂是( )
A. AgNO3 B. 稀硫酸
C. 稀盐酸 D. 稀硝酸3、在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁和硫酸铁溶液,这种试剂是( )
A.NaOH? ????????? B.Na2CO3
C.AgNO3? ???????? D.BaCl2 BA4、某溶液中含有大量的Cl-、SO42-、OH-三种离子,如果只取一次就能够将3种阴离子依次检验出来,下列实验操作顺序正确的是:
① 滴加Mg(NO3)2溶液 ② 过滤
③ 滴加Ba(NO3)2 ④滴加AgNO3
①②③②④或 ③②①②④
● 某白色晶体可能是硫酸铵,怎样证明?
A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B. 某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO42-
C.某无色溶液滴入紫色石蕊试液显红色,该溶液一定是酸溶液
D.验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl-5、对下列实验过程的评价,正确的是√作业:课本 P25 2 、31、以下是对某水溶液进行离子检验的方法和结论,其中正确的是( )
A、先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀,溶液中一定含有大量SO
B、加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定含有大量 的CO
C、加入足量浓NaOH溶液,产生了带有强烈刺激性气味的气体。溶液中一定含有大量的NH
D、先加适量的盐酸将溶液酸化,再加入AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl-+42-32-4C课堂训练实验现象:实验药品:实验结论:有刺激性气味气体产生,且该气体能使湿润的红石蕊试纸变蓝NH4Cl和(NH4)2SO4中含有NH4+
实验1.NH4Cl、 (NH4)2SO4 、NaOH实验2实验药品:NH4Cl、KCl、稀HNO3和Ag NO 3
实验现象:实验结论:问题稀硝酸的作用是什么?排除CO32-等的干扰反应生成不溶于稀硝酸的白色沉淀NH4Cl和KCl 中含有 Cl-实验3实验药品:(NH4)2SO4、K2SO4、稀HCl 和BaCl2实验现象:反应生成不溶于稀盐酸的白色沉淀实验结论:硫酸铵、硫酸钾中含有SO42-问题稀盐酸的作用是什么?排除CO32-和SO32-的干扰除杂不用稀硝酸实验3实验药品:(NH4)2SO4、K2SO4、稀HCl 和BaCl2实验现象:反应生成不溶于稀盐酸的白色沉淀实验结论:硫酸铵、硫酸钾中含有SO42-问题稀盐酸的作用是什么?排除CO32-和SO32-的干扰除杂不用稀硝酸含有K+透过蓝色钴玻璃观察到紫色在酒精灯火焰上灼烧K+(钾盐)含有SO42-生成白色沉淀、不溶解。加BaCl2溶液,再加稀HClSO42- (硫酸盐)有Cl-生成白色沉淀、不溶解。滴加AgNO3,再加稀硝酸Cl- (盐酸盐)含有NH4+。试纸变蓝。加浓的氢氧化钠、加热,用湿润的红色石蕊试纸放在 试管口NH4+ (铵盐)结论现象检验方法待检物质归纳:一、离子特征反应检验法
2、湿润的红色石蕊试纸不要接触到试管口
3、所加试剂的量要适量,不可浪费。4、结束时把废液到在废液缸(塑料烧杯中)。实验1:NH4Cl和(NH4)2SO4各2mL,分别2mLNaOH,
稍加热,将先准备好的湿润的试纸靠近试
管口实验步骤:实验现象:实验2:实验步骤:NH4Cl和KCl各少量(1~2)mL,各滴几滴稀HNO3,再各滴几滴Ag NO 3溶液实验现象:实验3:实验步骤:(NH4)2SO4和K2SO4溶液各少量,各滴几滴稀盐酸,再各滴几滴BaCl2溶液实验现象:产生刺激性气味气体, 石蕊试纸变蓝产生白色沉淀产生白色沉淀 取样(少量放在试管中)与碱混合加热,若有刺激性气味的气体产生,且该气使湿润的红色石蕊试纸变蓝,证明该试样中含有NH4+。
1、NH4+的检验(铵盐)
方法:实验原理:
蓝取样并向内加稀HNO3和AgNO3溶液,若生成白色沉淀,证明该试样中含有Cl- 。
2、Cl-的检验(盐酸盐或称氯化物)
方法:实验原理KCl+AgNO3=AgCl↓+KNO3稀硝酸的作用是什么?排除CO32-等的干扰
取样并向内加稀HCl、BaCl2溶液,若生成白色沉淀,证明该试样中含有SO42- 。3、SO42-的检验(硫酸盐)
方法:思考:
稀盐酸的作用?除去CO32-等的干扰实验原理Na2SO4+BaCl2=BaSO4↓+2NaCl如何检验刚才的蓝色溶液是否为CuCl2 ?
4. K+ 、 Na+的检验Na 为黄色 K为紫色焰色反应(许多金属或它们的化合物在灼烧时都会使火焰呈现出特殊的颜色,这叫做焰色反应)P20表1-5 一些物质的检验有烧焦羽毛的气味灼烧丝绸制品变蓝与碘水反应淀粉紫色石蕊变蓝;PH试纸变色PH>7
用紫色石蕊试液;用PH试纸碱
(OH-)紫色石蕊变红;PH试纸变色PH<7用紫色石蕊试液;用PH试纸酸
(H+)有气体产生,澄清石灰水变浑浊与盐酸反应,产生气体通入澄清石灰水碳酸盐
(CO32-)现象检验方法待检物质用红外光谱仪来确定:物质中是否含有某些有机基团用元素分析仪测定:物质中是否含C、H、O、N、S等元素5. 仪器分析法:课本P21用原子吸收光谱确定:物质中是否含有哪些金属元素1、人人都会出汗,汗液中含有NaCl,请设计实验加以证明。练习2、能用来区别BaCl2、NaCl、Na2CO3三种物质的
试剂是( )
A. AgNO3 B. 稀硫酸
C. 稀盐酸 D. 稀硝酸3、在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁和硫酸铁溶液,这种试剂是( )
A.NaOH? ????????? B.Na2CO3
C.AgNO3? ???????? D.BaCl2 BA4、某溶液中含有大量的Cl-、SO42-、OH-三种离子,如果只取一次就能够将3种阴离子依次检验出来,下列实验操作顺序正确的是:
① 滴加Mg(NO3)2溶液 ② 过滤
③ 滴加Ba(NO3)2 ④滴加AgNO3
①②③②④或 ③②①②④
● 某白色晶体可能是硫酸铵,怎样证明?
A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B. 某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO42-
C.某无色溶液滴入紫色石蕊试液显红色,该溶液一定是酸溶液
D.验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl-5、对下列实验过程的评价,正确的是√作业:课本 P25 2 、31、以下是对某水溶液进行离子检验的方法和结论,其中正确的是( )
A、先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀,溶液中一定含有大量SO
B、加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定含有大量 的CO
C、加入足量浓NaOH溶液,产生了带有强烈刺激性气味的气体。溶液中一定含有大量的NH
D、先加适量的盐酸将溶液酸化,再加入AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl-+42-32-4C课堂训练实验现象:实验药品:实验结论:有刺激性气味气体产生,且该气体能使湿润的红石蕊试纸变蓝NH4Cl和(NH4)2SO4中含有NH4+
实验1.NH4Cl、 (NH4)2SO4 、NaOH实验2实验药品:NH4Cl、KCl、稀HNO3和Ag NO 3
实验现象:实验结论:问题稀硝酸的作用是什么?排除CO32-等的干扰反应生成不溶于稀硝酸的白色沉淀NH4Cl和KCl 中含有 Cl-实验3实验药品:(NH4)2SO4、K2SO4、稀HCl 和BaCl2实验现象:反应生成不溶于稀盐酸的白色沉淀实验结论:硫酸铵、硫酸钾中含有SO42-问题稀盐酸的作用是什么?排除CO32-和SO32-的干扰除杂不用稀硝酸实验3实验药品:(NH4)2SO4、K2SO4、稀HCl 和BaCl2实验现象:反应生成不溶于稀盐酸的白色沉淀实验结论:硫酸铵、硫酸钾中含有SO42-问题稀盐酸的作用是什么?排除CO32-和SO32-的干扰除杂不用稀硝酸含有K+透过蓝色钴玻璃观察到紫色在酒精灯火焰上灼烧K+(钾盐)含有SO42-生成白色沉淀、不溶解。加BaCl2溶液,再加稀HClSO42- (硫酸盐)有Cl-生成白色沉淀、不溶解。滴加AgNO3,再加稀硝酸Cl- (盐酸盐)含有NH4+。试纸变蓝。加浓的氢氧化钠、加热,用湿润的红色石蕊试纸放在 试管口NH4+ (铵盐)结论现象检验方法待检物质归纳:一、离子特征反应检验法
