化学电源[下学期]
图片预览



文档简介
课件10张PPT。 知识回忆 1、从能量角度定义:把化学能转换成电能的装置 2、从反应本质定义: 自发进行的氧化还原反应,其氧化反应和还原
反应分别在分开的两极上进行,在连接两极
的导线中形成持续的电流.正极反应 负极反应 1、有自发的氧化还原反应
2、两个导体做电极
(一般为活泼性不同的两种金属
或金属与非金属,如石墨)
3、电极需插入电解质溶液中
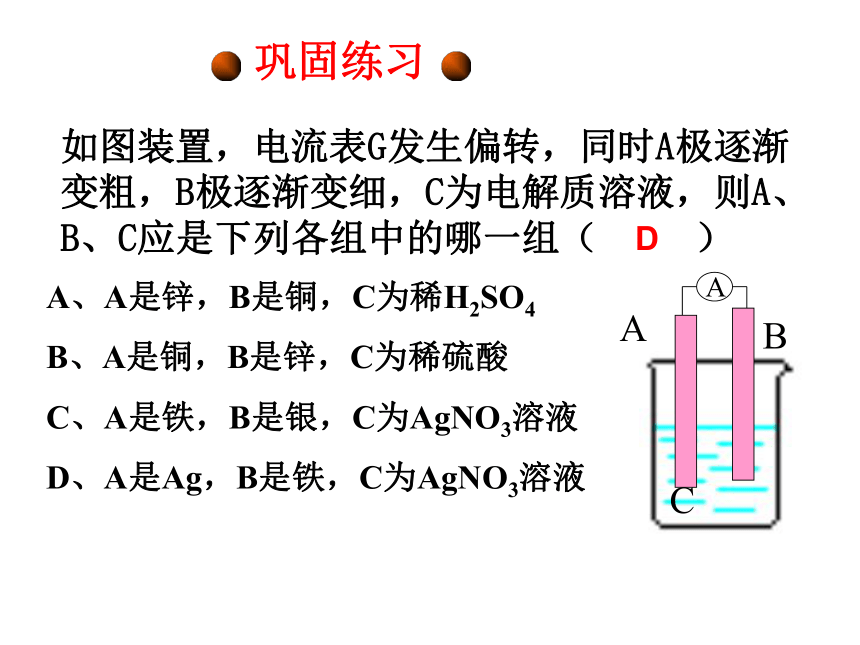
4、产生电流,需要形成回路构成原电池的条件 化学能转化成电能的条件巩固练习如图装置,电流表G发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的哪一组( ) A、A是锌,B是铜,C为稀H2SO4
B、A是铜,B是锌,C为稀硫酸
C、A是铁,B是银,C为AgNO3溶液
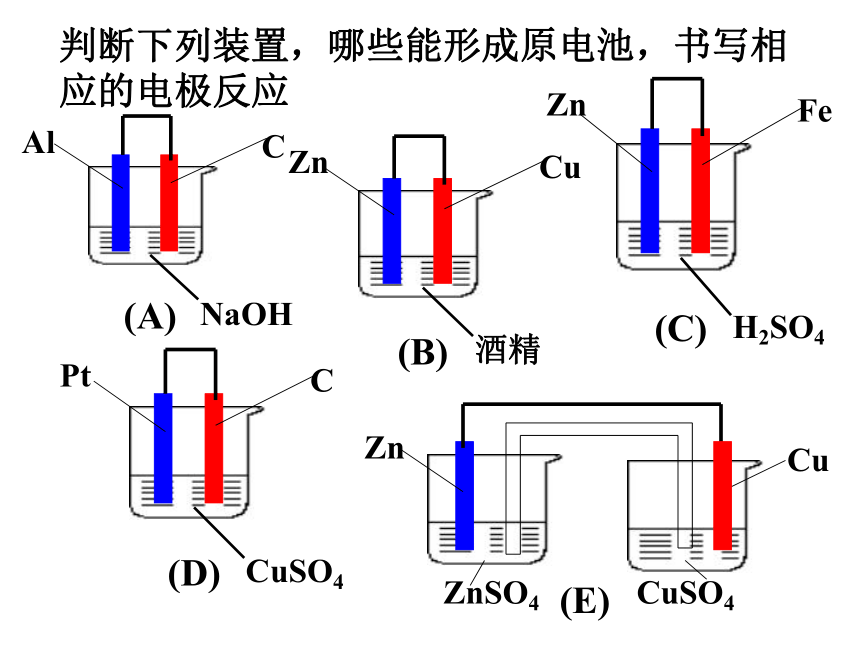
D、A是Ag,B是铁,C为AgNO3溶液 D判断下列装置,哪些能形成原电池,书写相应的电极反应在体积相同、浓度都是4.0mol/L的盐酸中,
一份加入纯锌,另一份加入含有杂质铜的
金属锌,发现后者产生的氢气速率快?
你能解释原因吗? 含有杂质铜的金属锌跟盐酸反应速率快,这是
由于Cu、Zn构成原电池的正极和负极,
其电极反应式为:
负极? ??Zn-2e- = Zn2+
正极 2H++2e- = H2 ↑注意:在相同条件下,
电化学反应比化学反应的反应速率快得多巩固与提高把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,d电极逐渐溶解,则四种金属的活动性顺序由强到弱的为( )
A.a > b > c > d B.a > c > d > b
C.c > a > b > d D.b > d > c > a B阅读课文P39化学电源内容,了解常见的化学电源(燃料电池)宇宙飞船上的氢氧燃料电池,
其电池反应为:2H2+O2=2H2O,
试写出电解质溶液为KOH时的电极反应式,
并指出各电极和电解质溶液的pH值变化。若电解质溶液为盐酸时又如何?
反应分别在分开的两极上进行,在连接两极
的导线中形成持续的电流.正极反应 负极反应 1、有自发的氧化还原反应
2、两个导体做电极
(一般为活泼性不同的两种金属
或金属与非金属,如石墨)
3、电极需插入电解质溶液中
4、产生电流,需要形成回路构成原电池的条件 化学能转化成电能的条件巩固练习如图装置,电流表G发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的哪一组( ) A、A是锌,B是铜,C为稀H2SO4
B、A是铜,B是锌,C为稀硫酸
C、A是铁,B是银,C为AgNO3溶液
D、A是Ag,B是铁,C为AgNO3溶液 D判断下列装置,哪些能形成原电池,书写相应的电极反应在体积相同、浓度都是4.0mol/L的盐酸中,
一份加入纯锌,另一份加入含有杂质铜的
金属锌,发现后者产生的氢气速率快?
你能解释原因吗? 含有杂质铜的金属锌跟盐酸反应速率快,这是
由于Cu、Zn构成原电池的正极和负极,
其电极反应式为:
负极? ??Zn-2e- = Zn2+
正极 2H++2e- = H2 ↑注意:在相同条件下,
电化学反应比化学反应的反应速率快得多巩固与提高把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,d电极逐渐溶解,则四种金属的活动性顺序由强到弱的为( )
A.a > b > c > d B.a > c > d > b
C.c > a > b > d D.b > d > c > a B阅读课文P39化学电源内容,了解常见的化学电源(燃料电池)宇宙飞船上的氢氧燃料电池,
其电池反应为:2H2+O2=2H2O,
试写出电解质溶液为KOH时的电极反应式,
并指出各电极和电解质溶液的pH值变化。若电解质溶液为盐酸时又如何?
