溴、碘的提取[上学期]
图片预览


文档简介
溴、碘的提取
大田中学 周萍娟
2006年7月
教学目标
知识技能:了解溴、碘的物理性质;了解海水中提取溴和碘的原理及过程;掌握氯、溴、碘单质之间的置换关系;掌握氯、溴、碘三种离子的检验方法;了解几种卤化物的性质、用途
能力培养:学会由事物的表象分析事物的本质、变化,进一步培养学生综合运用知识、解决问题的能力;通过人人动手实验,规范学生的操作,培养、提高学生的的实验能力、观察能力和对实验现象的分析能力。
科学思想:运用辨证唯物主义指导学习,培养学生的科学思维和正确的认识事物;培育环境保护意识。
科学品质:在发现总结规律的过程中启发学生分析、探究,激发学习兴趣。
科学方法:通过实验、观察、分析、对比等方法,使学生进一步学会综合运用知识解决问题。
重点:溴、碘的性质
难点:氯、溴、碘的性质比较及规律
课时安排 1课时
教学过程设计
教 师 活 动 学 生 活 动 设 计 意 图
[复习提问]上一节课我们学习了氯气的性质,请回忆氯气的重要化学性质并写出代表反应的化学方程式。 写出氯气与氢气、铁、水、氢氧化钠(钙)的化学方程式 复习旧知识,训练正确书写重要化学方程式
[引入]氯元素以氯化钠形式广泛的存在于海洋,但被称为“海洋元素”的却是溴,并且碘在海洋中也非常丰富。今天的课我们要学习溴、碘的单质及化合物与氯气及氯化物性质之间的异同;怎样从海洋中提取到溴和碘。 让学生明确本节课的学习重点
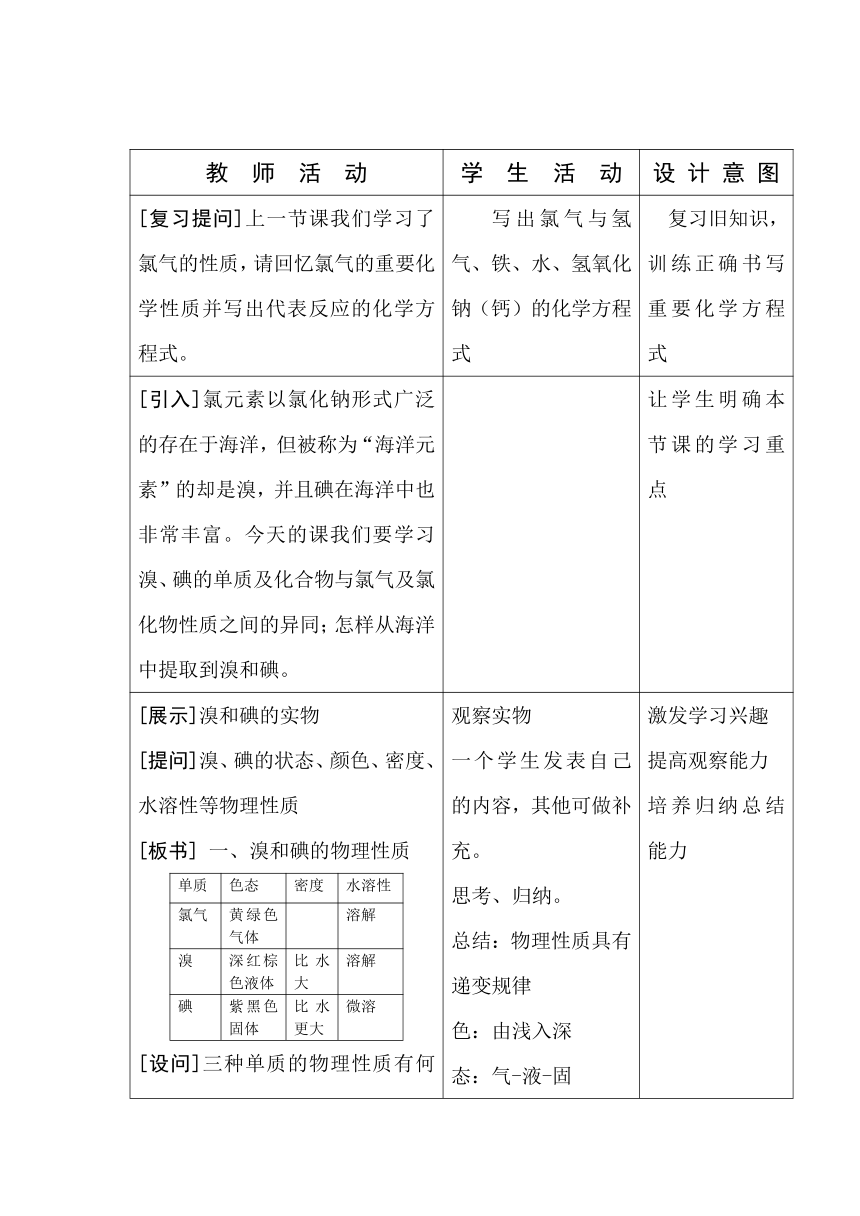
[展示]溴和碘的实物[提问]溴、碘的状态、颜色、密度、水溶性等物理性质[板书] 一、溴和碘的物理性质单质色态密度水溶性氯气黄绿色气体溶解溴深红棕色液体比水大溶解碘紫黑色固体比水更大微溶[设问]三种单质的物理性质有何关系? 观察实物一个学生发表自己的内容,其他可做补充。思考、归纳。总结:物理性质具有递变规律色:由浅入深态:气-液-固密度:变大水溶性:下降 激发学习兴趣提高观察能力培养归纳总结能力
[提问]观察贮存溴的试剂瓶的结构特点,溴还有什么物理性质? 试剂瓶内的物质明显分三层:底为深红棕色液体,中为红棕色溶液,上为红棕色气体总结:溴易挥发 提高学生解决问题的能力
[设问]碘呢?[演示实验]碘的升华,遇淀粉(马铃薯)显兰色[板书] 溴易挥发 碘易升华 遇淀粉显兰色引导学生阅读溴、碘的性质,划出重点信息。 疑问,动手实验、观察,得出结论阅读,记忆 利用实验释疑培养阅读自学能力
[讲述] 溴和碘的化学性质与氯气十分相似。请写出溴和碘分别与氢气、铁、水反应的化学方程式[板书]二、溴和碘的化学性质1、与氢气、铁、水等反应选择个别学生的方程式进行讲解:性质相似并不是完全相同,溴与氢气反应须要加热;碘与氢气则持续500℃并且碘化氢也会分解,是可逆反应;碘与铁则生成亚铁,这些不同是因为卤原子的结构决定的。 联系已学知识,明白动手写方程式 概括总结,形成规律性认识
[投影]活动与探究实验一:在一只试管中加入2-3mlNaBr,滴加少量新制氯水,再滴加少量CCl4,充分振荡,静置,观察实验现象。实验二:在两只试管中加入2-3mlKI,分别滴加溴水和新置氯水,再分别滴加少量CCl4,充分振荡,静置,观察实验现象。 四人一组进行实验记录现象并填写表2-4每个实验由一个学生代表总结:实验一:水层原为黄色,加入CCl4(下层)后,CCl4层出现了橙色。实验二:水层原为黄色,加入CCl4后,CCl4层出现了紫色。结论:根据水层与CCl4层的颜色变化,说明卤素单质之间发生了反应 利用实验的直观性,培养学生的感性思维。描述实验现象的语言表达能力,书写化学用语的能力。学会用表格处理资料,提高记忆
[提问]卤素单质之间的反应属于哪类反应类型?[设疑]氯能置换出溴和碘,溴能置换出碘,而碘却不能[板书]2、置换反应Cl2+NaBr==NaCl+Br2Cl2+KI==KCl+I2Br2+KI==KBr+I2 置换反应
[提问]你所熟悉的置换反应发生在哪些物质之间,为什么?此类置换又说明什么? [板书]非金属性Cl2>Br2>I2 排在氢前的金属与酸反应产生氢气;活泼金属置换出不活泼金属。是非金属性强的置换出非金属性较弱的非金属单质 温故引新,引导学生思考、比较、归纳
[讲述]:海水中提取溴和碘遵循的也是这一规律和原理,请翻阅书本P44[投影]例1、工业上从海水中提取溴采用下列方法:(1)向海水中通入氯气使NaBr氧化,反应式为________________(2)向所得溶液中鼓入空气,将Br2吹出用纯碱吸收生成NaBr、NaBrO3反应式________________(3)将(2)所得的溶液用硫酸酸化,使NaBr、NaBrO3转化成单质溴(4)这样制得的溴含少量Cl2,除Cl2的方法是________________ 自学 培养学生的自学能力把知识点分解发散,既能达到良好的学习效果,又适当的降低难度
[过渡]下面我们再来认识几种卤化物,卤化物中卤元素以离子形式存在,卤离子如何检验?[投影]卤离子检验取三只试管分别加入2-3mlNaCl、NaBr、KI三种溶液,分别滴加少量的AgNO3,再滴加稀硝酸,观察实验现象[板书]三、卤化物卤离子的检验滴加AgNO3再加稀硝酸[投影练习]有一包白色粉末,可能含有Na2CO3,NaCl中的一种或两种,如何确定? 四人一组进行实验记录现象 用实验解决问题,培养学生的动手操作能力现学现用,加深记忆。
[讲述]AgCl、AgBr、AgI对光都不稳定,易分解,具感光性,常用于感光材料,如照相用的胶卷和相纸上涂有一层药膜主要成分是溴化银,碘化银又可用于人工降雨[提问]你觉得卤素单质和他的化合物还有哪些重要的用途? 思考,发表意见卤素是人类身体不可缺少的元素,尤其是碘元素,如果缺碘人将患上大脖子病,影响人类的健康 联系自身,增加学习兴趣,扩展知识层面
[讲述]对,碘缺乏病给人类智力、健康带来极大的危害对婴幼儿的危害更大,患儿身体矮小、智力低下、发育不全,甚至痴呆。为了防止碘缺乏症,我国政府在居民的食盐中加入了一定量的碘盐。[设问]你知道加的是什么碘盐?展示食盐包装袋 学生非常好奇,猜想原来是碘酸钾 联系生活,联系实际,体现化学的实用性
随堂检测:
1、 将少量氯气通入无色的饱和碘化钾溶液中,溶液变_______色,反应式_______________向此溶液中加入四氯化碳,振荡后静止,则溶液分为两层,上层是______,颜色为_____色,下层是____,颜色为_____色。
2、 欲将NaCl、沙子、I2三者的固体混合物分开,最好的操作顺序
A、溶解 过滤 萃取 B、加热 溶解 过滤
C、升华 萃取 蒸馏 D、分液 结晶 分液
大田中学 周萍娟
2006年7月
教学目标
知识技能:了解溴、碘的物理性质;了解海水中提取溴和碘的原理及过程;掌握氯、溴、碘单质之间的置换关系;掌握氯、溴、碘三种离子的检验方法;了解几种卤化物的性质、用途
能力培养:学会由事物的表象分析事物的本质、变化,进一步培养学生综合运用知识、解决问题的能力;通过人人动手实验,规范学生的操作,培养、提高学生的的实验能力、观察能力和对实验现象的分析能力。
科学思想:运用辨证唯物主义指导学习,培养学生的科学思维和正确的认识事物;培育环境保护意识。
科学品质:在发现总结规律的过程中启发学生分析、探究,激发学习兴趣。
科学方法:通过实验、观察、分析、对比等方法,使学生进一步学会综合运用知识解决问题。
重点:溴、碘的性质
难点:氯、溴、碘的性质比较及规律
课时安排 1课时
教学过程设计
教 师 活 动 学 生 活 动 设 计 意 图
[复习提问]上一节课我们学习了氯气的性质,请回忆氯气的重要化学性质并写出代表反应的化学方程式。 写出氯气与氢气、铁、水、氢氧化钠(钙)的化学方程式 复习旧知识,训练正确书写重要化学方程式
[引入]氯元素以氯化钠形式广泛的存在于海洋,但被称为“海洋元素”的却是溴,并且碘在海洋中也非常丰富。今天的课我们要学习溴、碘的单质及化合物与氯气及氯化物性质之间的异同;怎样从海洋中提取到溴和碘。 让学生明确本节课的学习重点
[展示]溴和碘的实物[提问]溴、碘的状态、颜色、密度、水溶性等物理性质[板书] 一、溴和碘的物理性质单质色态密度水溶性氯气黄绿色气体溶解溴深红棕色液体比水大溶解碘紫黑色固体比水更大微溶[设问]三种单质的物理性质有何关系? 观察实物一个学生发表自己的内容,其他可做补充。思考、归纳。总结:物理性质具有递变规律色:由浅入深态:气-液-固密度:变大水溶性:下降 激发学习兴趣提高观察能力培养归纳总结能力
[提问]观察贮存溴的试剂瓶的结构特点,溴还有什么物理性质? 试剂瓶内的物质明显分三层:底为深红棕色液体,中为红棕色溶液,上为红棕色气体总结:溴易挥发 提高学生解决问题的能力
[设问]碘呢?[演示实验]碘的升华,遇淀粉(马铃薯)显兰色[板书] 溴易挥发 碘易升华 遇淀粉显兰色引导学生阅读溴、碘的性质,划出重点信息。 疑问,动手实验、观察,得出结论阅读,记忆 利用实验释疑培养阅读自学能力
[讲述] 溴和碘的化学性质与氯气十分相似。请写出溴和碘分别与氢气、铁、水反应的化学方程式[板书]二、溴和碘的化学性质1、与氢气、铁、水等反应选择个别学生的方程式进行讲解:性质相似并不是完全相同,溴与氢气反应须要加热;碘与氢气则持续500℃并且碘化氢也会分解,是可逆反应;碘与铁则生成亚铁,这些不同是因为卤原子的结构决定的。 联系已学知识,明白动手写方程式 概括总结,形成规律性认识
[投影]活动与探究实验一:在一只试管中加入2-3mlNaBr,滴加少量新制氯水,再滴加少量CCl4,充分振荡,静置,观察实验现象。实验二:在两只试管中加入2-3mlKI,分别滴加溴水和新置氯水,再分别滴加少量CCl4,充分振荡,静置,观察实验现象。 四人一组进行实验记录现象并填写表2-4每个实验由一个学生代表总结:实验一:水层原为黄色,加入CCl4(下层)后,CCl4层出现了橙色。实验二:水层原为黄色,加入CCl4后,CCl4层出现了紫色。结论:根据水层与CCl4层的颜色变化,说明卤素单质之间发生了反应 利用实验的直观性,培养学生的感性思维。描述实验现象的语言表达能力,书写化学用语的能力。学会用表格处理资料,提高记忆
[提问]卤素单质之间的反应属于哪类反应类型?[设疑]氯能置换出溴和碘,溴能置换出碘,而碘却不能[板书]2、置换反应Cl2+NaBr==NaCl+Br2Cl2+KI==KCl+I2Br2+KI==KBr+I2 置换反应
[提问]你所熟悉的置换反应发生在哪些物质之间,为什么?此类置换又说明什么? [板书]非金属性Cl2>Br2>I2 排在氢前的金属与酸反应产生氢气;活泼金属置换出不活泼金属。是非金属性强的置换出非金属性较弱的非金属单质 温故引新,引导学生思考、比较、归纳
[讲述]:海水中提取溴和碘遵循的也是这一规律和原理,请翻阅书本P44[投影]例1、工业上从海水中提取溴采用下列方法:(1)向海水中通入氯气使NaBr氧化,反应式为________________(2)向所得溶液中鼓入空气,将Br2吹出用纯碱吸收生成NaBr、NaBrO3反应式________________(3)将(2)所得的溶液用硫酸酸化,使NaBr、NaBrO3转化成单质溴(4)这样制得的溴含少量Cl2,除Cl2的方法是________________ 自学 培养学生的自学能力把知识点分解发散,既能达到良好的学习效果,又适当的降低难度
[过渡]下面我们再来认识几种卤化物,卤化物中卤元素以离子形式存在,卤离子如何检验?[投影]卤离子检验取三只试管分别加入2-3mlNaCl、NaBr、KI三种溶液,分别滴加少量的AgNO3,再滴加稀硝酸,观察实验现象[板书]三、卤化物卤离子的检验滴加AgNO3再加稀硝酸[投影练习]有一包白色粉末,可能含有Na2CO3,NaCl中的一种或两种,如何确定? 四人一组进行实验记录现象 用实验解决问题,培养学生的动手操作能力现学现用,加深记忆。
[讲述]AgCl、AgBr、AgI对光都不稳定,易分解,具感光性,常用于感光材料,如照相用的胶卷和相纸上涂有一层药膜主要成分是溴化银,碘化银又可用于人工降雨[提问]你觉得卤素单质和他的化合物还有哪些重要的用途? 思考,发表意见卤素是人类身体不可缺少的元素,尤其是碘元素,如果缺碘人将患上大脖子病,影响人类的健康 联系自身,增加学习兴趣,扩展知识层面
[讲述]对,碘缺乏病给人类智力、健康带来极大的危害对婴幼儿的危害更大,患儿身体矮小、智力低下、发育不全,甚至痴呆。为了防止碘缺乏症,我国政府在居民的食盐中加入了一定量的碘盐。[设问]你知道加的是什么碘盐?展示食盐包装袋 学生非常好奇,猜想原来是碘酸钾 联系生活,联系实际,体现化学的实用性
随堂检测:
1、 将少量氯气通入无色的饱和碘化钾溶液中,溶液变_______色,反应式_______________向此溶液中加入四氯化碳,振荡后静止,则溶液分为两层,上层是______,颜色为_____色,下层是____,颜色为_____色。
2、 欲将NaCl、沙子、I2三者的固体混合物分开,最好的操作顺序
A、溶解 过滤 萃取 B、加热 溶解 过滤
C、升华 萃取 蒸馏 D、分液 结晶 分液
