化学反应中的能量变化(二课时)[下学期]
文档属性
| 名称 | 化学反应中的能量变化(二课时)[下学期] |  | |
| 格式 | rar | ||
| 文件大小 | 294.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-04-06 21:19:00 | ||
图片预览





文档简介
课件26张PPT。第二单元
化学反应中的热量一.化学反应中的热量变化化学化学变化中除有新物质生成外,必然伴随有能量(热能、光能、电能)的变化。利用化学反应:①是制取物质、②是利用反应中的能量
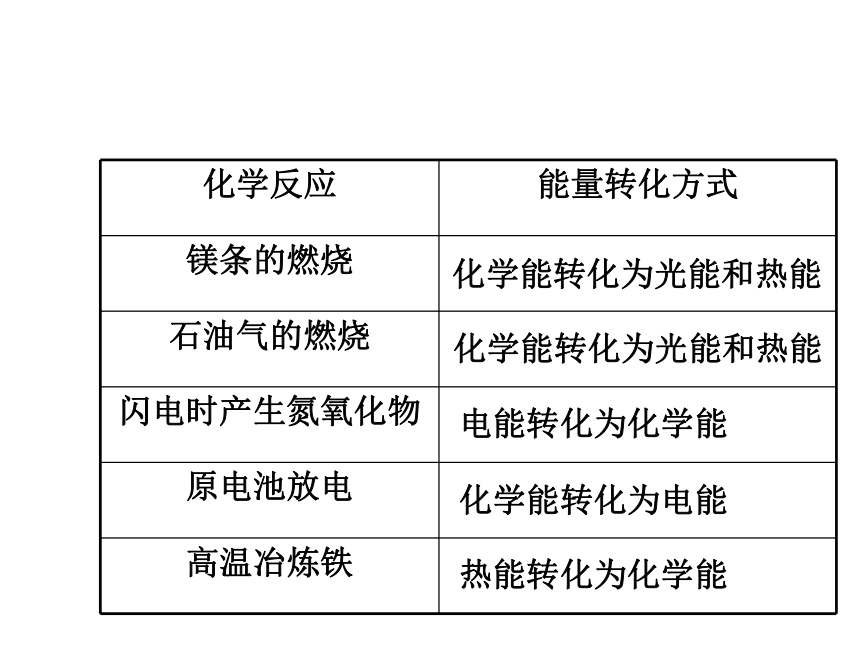
思考:生活中哪些事实说明了在化学反应中伴随着能量的变化?请说出能量转化的方式。化学能转化为光能和热能化学能转化为光能和热能化学能转化为电能电能转化为化学能热能转化为化学能 交流与讨论:问题1:
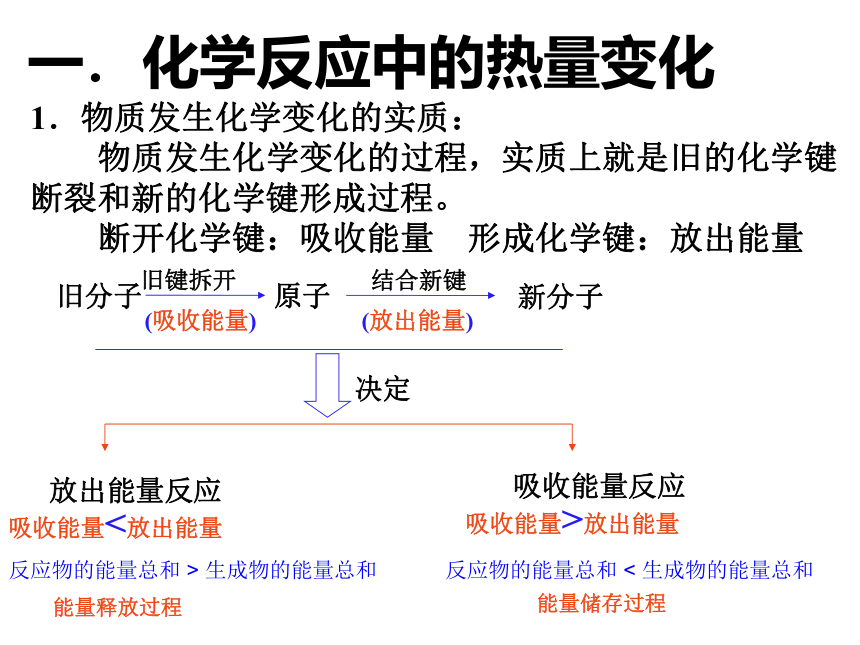
为什么化学反应总会伴随着能量的变化?能量变化的实质是什么?1.物质发生化学变化的实质:
物质发生化学变化的过程,实质上就是旧的化学键断裂和新的化学键形成过程。
断开化学键:吸收能量 形成化学键:放出能量 一.化学反应中的热量变化(吸收能量)旧分子旧键拆开 原子(放出能量)新分子结合新键吸收能量<放出能量吸收能量>放出能量放出能量反应吸收能量反应决定
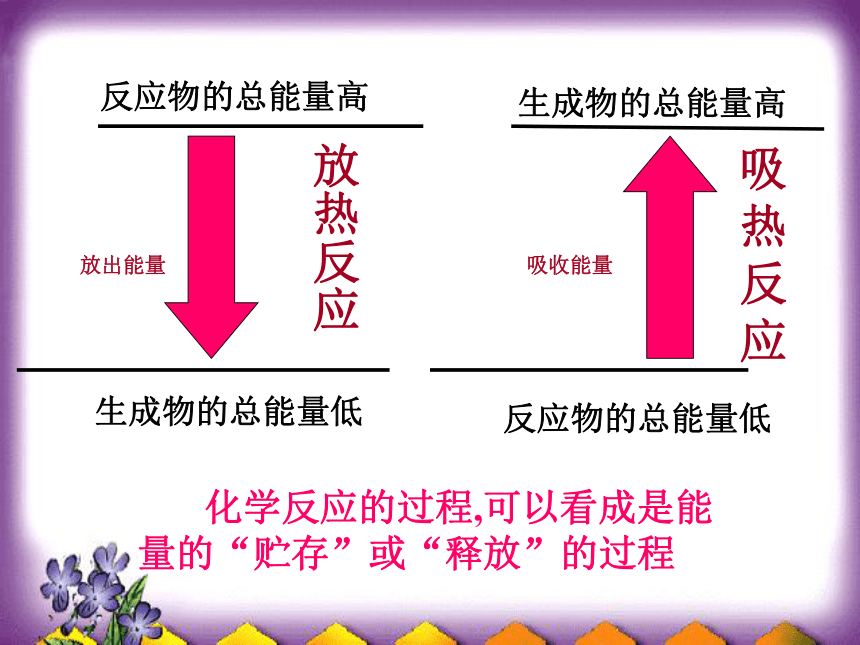
反应物的能量总和 > 生成物的能量总和反应物的能量总和 < 生成物的能量总和能量释放过程能量储存过程反应物的总能量高生成物的总能量低放热反应生成物的总能量高反应物的总能量低吸热反应 化学反应的过程,可以看成是能量的“贮存”或“释放”的过程
吸收能量放出能量1、放热反应:化学上把放出热的化学反应,叫放热反应。
2、吸热反应:化学上把吸收热的化学反应,叫吸热反应。放热反应:反应物的能量总和 > 生成物的能量总和
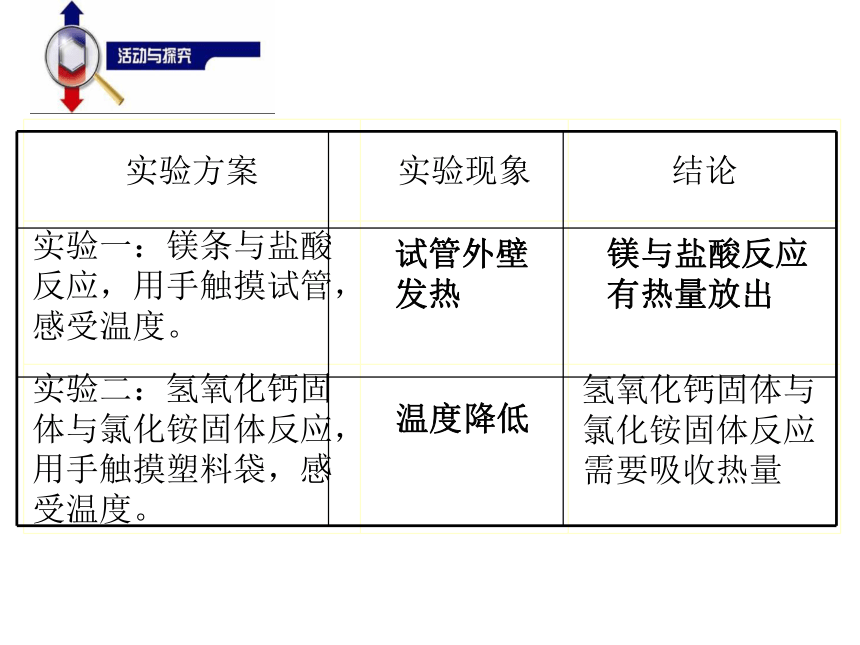
吸热反应:反应物的能量总和 < 生成物的能量总和2.化学反应中的能量变化:通常表现为热量的变化常见的反应那些放热反应、吸热反应呢?试管外壁
发热镁与盐酸反应
有热量放出温度降低氢氧化钙固体与
氯化铵固体反应
需要吸收热量常见的放热反应、吸热反应放热
反应吸热
反应结论:能够自发进行的一般是放热反应,需要持续加热才能进行的一般是吸热反应。问题解决1、判断下列反应是放热反应还是吸热反应的
⑴ :镁条燃烧
⑵ :高温下木炭与二氧化碳反应生成一氧化碳
⑶ C:氧化钙与水
放吸放2、已知断开1molH2中的H-H键需要吸收436.4kJ 能量,断开1molCl2中的Cl-Cl键需要吸收242.7kJ能量,生成1molHCl中的H-Cl键放出431.8kJ能量.试说明反应
2HCl == H2 + Cl2
是放热的还是吸热的?问题解决 1molH2分子中的化学键断裂时需吸收436kJ的能量 1molCl2分子中的化学键断裂时需吸收243kJ的能量2molHCl分子中的化学键形成时释放431kJ/mol×2=862kJ的能量微观解释:
1mol H2中的H-H键断裂时吸收436.4kJ的能量
1molCl2中的Cl-Cl键断裂时吸收242.7kJ的能量
1molHCl中的H-Cl键形成时放出431.8kJ的能量
所以,1molH2和1molCl2反应生成2molHCl时,
放出431.8kJ×2-(436.4kJ+242.7kJ)=184.5kJ的能量。E反应历程△E = kJ吸收436.4 kJ (H2)
吸收242.7 kJ(Cl2)放出2×431.8 kJ
= 863.6 kJ184.5(注:1mol H2和1mol Cl2反应)正反应是放热反应那么逆反应是什么反应吗? ? E184.53.反应热(1)定义:在化学反应中放出或吸收的热量叫反应热。
(2)符号:
(3)单位:△H kJ ?mol-1 H2(g)+Cl2(g) = 2HCl(g);ΔH = -184.6 kJ/mol
负放加吸得了二、热化学方程式:1、定义:
表明反应所放出或吸收的热量的化学方程式,叫做热化学方程式。2H2(g)+ O2(g) = 2H2O(g);ΔH = -483.6kJ/mol2H2(g)+ O2(g) = 2H2O(l);ΔH = -571.6kJ/mol 2.书写步骤:(1)写符合质量守恒的化学方程式(2)注明反应物,生成物聚集状态(s,l,g)(3)用△H表明化学反应放出或吸收的热量 2mol H2(气态) 与1mol O2(气态) 反应, 生成2mol H2O(液态) 放出571.6 kJ的热量,那么生成2mol H2O(气态)呢? 2H2(g)+ O2(g) = 2H2O(l);ΔH = -571.6kJ/mol 问题解决1、2H2(g)+O2(g) === 2H2O(l) △H=- 571.6 kJ/mol ①
H2(g)+1/2O2(g) === H2O(l) △H=- 285.8 kJ/mol ②
H2(g)+1/2O2(g) === H2O(g) △H=- 241.8 kJ/mol ③在上述表示氢气在氧气中燃烧生成水的三个热化学方程式中,方程式①的△H是方程式②的2倍,为什么?方程式③中的△H与方程式②的也有差别,为什么?问题解决2、C、C8H18、CH4、C2H5OH(乙醇)完全燃烧的热化学方程式可以分别表示为:
C(s) + O2(g) == CO2(g) △H= - 393.6kJ/mol
C8H18 (l) + 25/2O2(g) == 8CO2(g)+ 9H2O(l)
△H= - 5473kJ/mol
CH4+ 2O2(g) == CO2(g)+2 H2O(l) △H= - 889.6kJ/mol
C2H5OH + 3O2(g) == 2CO2(g)+3 H2O(l)
△H= - 1366.8kJ/mol
完全燃烧相等质量的上述物质,放出热量大小顺序为
。③②①④÷12÷114÷16÷463、注意事项:①、标聚集状态(g:气、l:液、s:固)不用↑↓②、注意ΔH的“+”与“-”,放热反应为-,吸热反应为“+”④、对于相同物质的反应,当化学计量数不同时,其△H 也不同,即△H 的值与计量数成正比③、热化学方程式中各物质前的化学计量数不表示分子个数,只表示物质的量单位是“摩” ,因此可以是整数或分数。⑤、注明反应的温度和压强(不注明通常指101 kPa和25℃)例1、250C (1.01)(105)Pa下,1g 硫粉在氧气中充分燃烧放出 9.36kJ热量,写出硫燃烧的热化学方程式。1g 硫粉在氧气中充分燃烧放出 9. 36kJ 热量1 mol 硫粉在氧气中充分燃烧放出热量为:
( 32g ) ×( 9.36 kJ /g ) = 299.62 kJ S (s) + O2(g) = SO2(g);?H= – 299.62kJ /mol 分析:练习1:1g H2燃烧,生成液态水并放出142.9 KJ热量,写出该反应的热化学方程式? 练习2:3mol甲烷燃烧时,生成液态水和二氧化碳,同时放出2670.9kJ的热。请写出热化学方程式。2H2(g)+O2(g) === 2H2O(l) △H=- 571.6 kJ/molCH4(g)+ 2O2(g) == CO2(g)+2 H2O(l) △H= - 890.3kJ/mol练习3.已知:X + Y ==M +N 为放热反应,下列关于该反应的说法正确的是 ( )
A:X的能量一定大于M
B:Y的能量一定大于N
C:X和Y的总能量一定高于M和N的总能量
D:因为该反应是放热反应,故不需要加热,反应就可以发生.C练习4:依据事实,写出下列反应的热化学方程式。
14 g N2(气态)与适量H2(气态)起反应,生成 NH3(气态),放出46.1 kJ的热量。
2molN2(气态)与适量O2(气态)起反应,生成NO2(气态),需吸收136 kJ的热量。
适量Cu(固态)与16 g O2(气态)起反应,生成CuO(固体),放出157kJ的热量。
适量C(固态)与适量H2O(气态)起反应,生成28 g CO(气态)和H2(气态),需吸收131.3kJ的热量。
化学反应中的热量一.化学反应中的热量变化化学化学变化中除有新物质生成外,必然伴随有能量(热能、光能、电能)的变化。利用化学反应:①是制取物质、②是利用反应中的能量
思考:生活中哪些事实说明了在化学反应中伴随着能量的变化?请说出能量转化的方式。化学能转化为光能和热能化学能转化为光能和热能化学能转化为电能电能转化为化学能热能转化为化学能 交流与讨论:问题1:
为什么化学反应总会伴随着能量的变化?能量变化的实质是什么?1.物质发生化学变化的实质:
物质发生化学变化的过程,实质上就是旧的化学键断裂和新的化学键形成过程。
断开化学键:吸收能量 形成化学键:放出能量 一.化学反应中的热量变化(吸收能量)旧分子旧键拆开 原子(放出能量)新分子结合新键吸收能量<放出能量吸收能量>放出能量放出能量反应吸收能量反应决定
反应物的能量总和 > 生成物的能量总和反应物的能量总和 < 生成物的能量总和能量释放过程能量储存过程反应物的总能量高生成物的总能量低放热反应生成物的总能量高反应物的总能量低吸热反应 化学反应的过程,可以看成是能量的“贮存”或“释放”的过程
吸收能量放出能量1、放热反应:化学上把放出热的化学反应,叫放热反应。
2、吸热反应:化学上把吸收热的化学反应,叫吸热反应。放热反应:反应物的能量总和 > 生成物的能量总和
吸热反应:反应物的能量总和 < 生成物的能量总和2.化学反应中的能量变化:通常表现为热量的变化常见的反应那些放热反应、吸热反应呢?试管外壁
发热镁与盐酸反应
有热量放出温度降低氢氧化钙固体与
氯化铵固体反应
需要吸收热量常见的放热反应、吸热反应放热
反应吸热
反应结论:能够自发进行的一般是放热反应,需要持续加热才能进行的一般是吸热反应。问题解决1、判断下列反应是放热反应还是吸热反应的
⑴ :镁条燃烧
⑵ :高温下木炭与二氧化碳反应生成一氧化碳
⑶ C:氧化钙与水
放吸放2、已知断开1molH2中的H-H键需要吸收436.4kJ 能量,断开1molCl2中的Cl-Cl键需要吸收242.7kJ能量,生成1molHCl中的H-Cl键放出431.8kJ能量.试说明反应
2HCl == H2 + Cl2
是放热的还是吸热的?问题解决 1molH2分子中的化学键断裂时需吸收436kJ的能量 1molCl2分子中的化学键断裂时需吸收243kJ的能量2molHCl分子中的化学键形成时释放431kJ/mol×2=862kJ的能量微观解释:
1mol H2中的H-H键断裂时吸收436.4kJ的能量
1molCl2中的Cl-Cl键断裂时吸收242.7kJ的能量
1molHCl中的H-Cl键形成时放出431.8kJ的能量
所以,1molH2和1molCl2反应生成2molHCl时,
放出431.8kJ×2-(436.4kJ+242.7kJ)=184.5kJ的能量。E反应历程△E = kJ吸收436.4 kJ (H2)
吸收242.7 kJ(Cl2)放出2×431.8 kJ
= 863.6 kJ184.5(注:1mol H2和1mol Cl2反应)正反应是放热反应那么逆反应是什么反应吗? ? E184.53.反应热(1)定义:在化学反应中放出或吸收的热量叫反应热。
(2)符号:
(3)单位:△H kJ ?mol-1 H2(g)+Cl2(g) = 2HCl(g);ΔH = -184.6 kJ/mol
负放加吸得了二、热化学方程式:1、定义:
表明反应所放出或吸收的热量的化学方程式,叫做热化学方程式。2H2(g)+ O2(g) = 2H2O(g);ΔH = -483.6kJ/mol2H2(g)+ O2(g) = 2H2O(l);ΔH = -571.6kJ/mol 2.书写步骤:(1)写符合质量守恒的化学方程式(2)注明反应物,生成物聚集状态(s,l,g)(3)用△H表明化学反应放出或吸收的热量 2mol H2(气态) 与1mol O2(气态) 反应, 生成2mol H2O(液态) 放出571.6 kJ的热量,那么生成2mol H2O(气态)呢? 2H2(g)+ O2(g) = 2H2O(l);ΔH = -571.6kJ/mol 问题解决1、2H2(g)+O2(g) === 2H2O(l) △H=- 571.6 kJ/mol ①
H2(g)+1/2O2(g) === H2O(l) △H=- 285.8 kJ/mol ②
H2(g)+1/2O2(g) === H2O(g) △H=- 241.8 kJ/mol ③在上述表示氢气在氧气中燃烧生成水的三个热化学方程式中,方程式①的△H是方程式②的2倍,为什么?方程式③中的△H与方程式②的也有差别,为什么?问题解决2、C、C8H18、CH4、C2H5OH(乙醇)完全燃烧的热化学方程式可以分别表示为:
C(s) + O2(g) == CO2(g) △H= - 393.6kJ/mol
C8H18 (l) + 25/2O2(g) == 8CO2(g)+ 9H2O(l)
△H= - 5473kJ/mol
CH4+ 2O2(g) == CO2(g)+2 H2O(l) △H= - 889.6kJ/mol
C2H5OH + 3O2(g) == 2CO2(g)+3 H2O(l)
△H= - 1366.8kJ/mol
完全燃烧相等质量的上述物质,放出热量大小顺序为
。③②①④÷12÷114÷16÷463、注意事项:①、标聚集状态(g:气、l:液、s:固)不用↑↓②、注意ΔH的“+”与“-”,放热反应为-,吸热反应为“+”④、对于相同物质的反应,当化学计量数不同时,其△H 也不同,即△H 的值与计量数成正比③、热化学方程式中各物质前的化学计量数不表示分子个数,只表示物质的量单位是“摩” ,因此可以是整数或分数。⑤、注明反应的温度和压强(不注明通常指101 kPa和25℃)例1、250C (1.01)(105)Pa下,1g 硫粉在氧气中充分燃烧放出 9.36kJ热量,写出硫燃烧的热化学方程式。1g 硫粉在氧气中充分燃烧放出 9. 36kJ 热量1 mol 硫粉在氧气中充分燃烧放出热量为:
( 32g ) ×( 9.36 kJ /g ) = 299.62 kJ S (s) + O2(g) = SO2(g);?H= – 299.62kJ /mol 分析:练习1:1g H2燃烧,生成液态水并放出142.9 KJ热量,写出该反应的热化学方程式? 练习2:3mol甲烷燃烧时,生成液态水和二氧化碳,同时放出2670.9kJ的热。请写出热化学方程式。2H2(g)+O2(g) === 2H2O(l) △H=- 571.6 kJ/molCH4(g)+ 2O2(g) == CO2(g)+2 H2O(l) △H= - 890.3kJ/mol练习3.已知:X + Y ==M +N 为放热反应,下列关于该反应的说法正确的是 ( )
A:X的能量一定大于M
B:Y的能量一定大于N
C:X和Y的总能量一定高于M和N的总能量
D:因为该反应是放热反应,故不需要加热,反应就可以发生.C练习4:依据事实,写出下列反应的热化学方程式。
14 g N2(气态)与适量H2(气态)起反应,生成 NH3(气态),放出46.1 kJ的热量。
2molN2(气态)与适量O2(气态)起反应,生成NO2(气态),需吸收136 kJ的热量。
适量Cu(固态)与16 g O2(气态)起反应,生成CuO(固体),放出157kJ的热量。
适量C(固态)与适量H2O(气态)起反应,生成28 g CO(气态)和H2(气态),需吸收131.3kJ的热量。
