金属的化学性质[上学期]
文档属性
| 名称 | 金属的化学性质[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 130.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2005-11-20 00:00:00 | ||
图片预览





文档简介
课件16张PPT。课题2
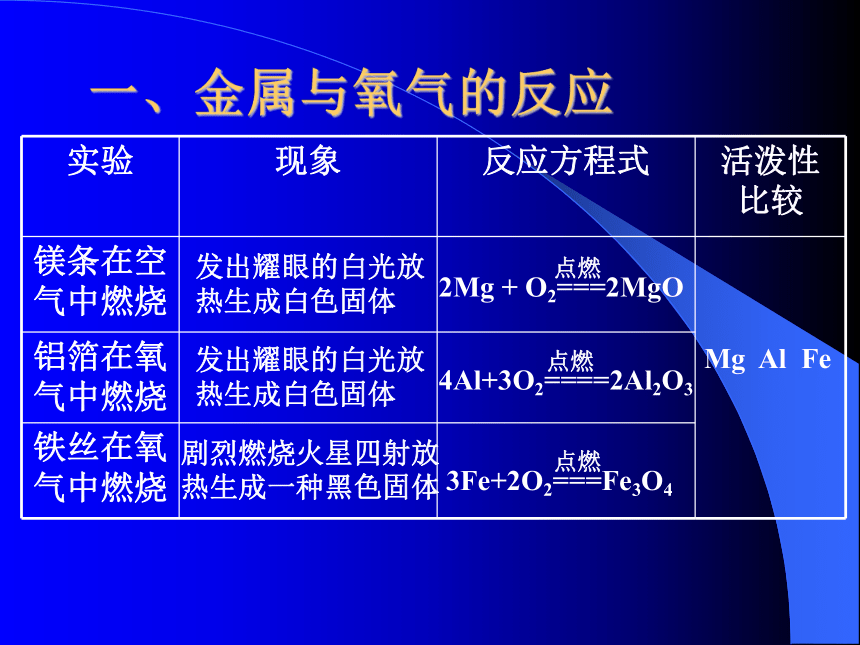
金属的化学性质一、金属与氧气的反应二、金属与稀盐酸、稀硫酸的反应:三、金属与其它化合物的反应一、金属与氧气的反应发出耀眼的白光放热生成白色固体发出耀眼的白光放热生成白色固体剧烈燃烧火星四射放热生成一种黑色固体2Mg + O2===2MgO点燃4Al+3O2====2Al2O3点燃3Fe+2O2===Fe3O4点燃Mg Al Fe1.为什么铝具有优良的抗腐蚀性能?2.“真金不怕火炼”蕴含什么意思?讨论:3.通过金属与氧气的反应 的难易和剧烈程度得出部分金属的活动性。结论一:
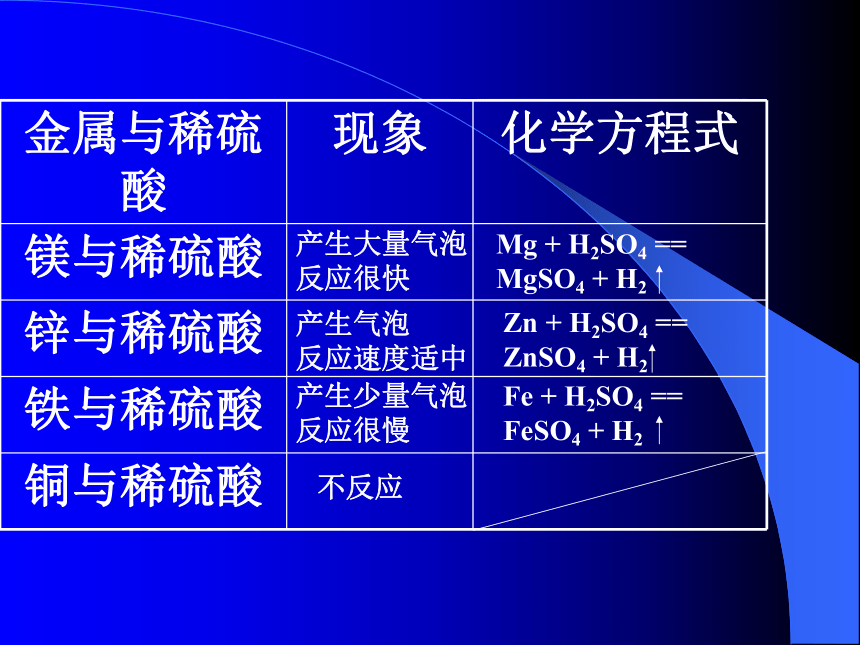
镁、铝比较活泼,铁、铜次之,金最不活泼。 返回产生大量气泡反应很快产生少量气泡反应很慢产生气泡 反应速度适中不反应二、金属与稀盐酸、稀硫酸的反应:Mg+2HCl==MgCl2+H2 Zn+2HCl==ZnCl2 +H2Fe+2HCl===FeCl2+H2 产生大量气泡反应很快产生气泡 反应速度适中产生少量气泡反应很慢不反应Mg + H2SO4 == MgSO4 + H2Zn + H2SO4 == ZnSO4 + H2Fe + H2SO4 == FeSO4 + H2Mg + 2HCl === MgCl2 + H2 Zn + 2HCl === ZnCl2 + H2Fe + 2HCl === FeCl2 + H2 单质化合物化合物单质置换反应——由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应。 结论二:
Mg Zn Fe (H) Cu
金属活动性由强减弱 Mg + H2SO4 === MgSO4 + H2
Zn + H2SO4 === ZnSO4 + H2
Fe + H2SO4 === FeSO4 + H2
返回铝丝表面出现红色物质溶液由蓝色变成无色Al + CuSO4 —
Al2﹙SO4﹚3+ Cu332铜丝表面出现银白色物质溶液由无色变成蓝色Cu+ AgNO3 — Cu﹙NO3﹚2+ Ag22======无现象三、金属与其它化合物的反应结论三:
Al Cu Ag
金属活动性由强减弱 返回金属活动性顺序: K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱 金属活动性顺序的应用:1.在金属活动性顺序里,金属的位置越前,它的活动性越强。2.在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。3.在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。练习1.判断下列反应能否发生,能发生的写出化学方程式,不能发生的说明原因。
⑴银和稀硫酸
⑵铁和稀盐酸
⑶铜和硫酸锌溶液
⑷锌和硫酸铜溶液
⑸镁和硝酸银溶液
⑹铜和氯化银固体2. “药金”又称为“愚人金”,实为铜、锌合金。由于“药金”外观与黄金相似,常被不法商贩用来冒充黄金牟取暴利。请你设计实验,证明实验台上的“药金”戒指是假黄金戒指。
镁、铝比较活泼,铁、铜次之,金最不活泼。 返回产生大量气泡反应很快产生少量气泡反应很慢产生气泡 反应速度适中不反应二、金属与稀盐酸、稀硫酸的反应:Mg+2HCl==MgCl2+H2 Zn+2HCl==ZnCl2 +H2Fe+2HCl===FeCl2+H2 产生大量气泡反应很快产生气泡 反应速度适中产生少量气泡反应很慢不反应Mg + H2SO4 == MgSO4 + H2Zn + H2SO4 == ZnSO4 + H2Fe + H2SO4 == FeSO4 + H2Mg + 2HCl === MgCl2 + H2 Zn + 2HCl === ZnCl2 + H2Fe + 2HCl === FeCl2 + H2 单质化合物化合物单质置换反应——由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应。 结论二:
Mg Zn Fe (H) Cu
金属活动性由强减弱 Mg + H2SO4 === MgSO4 + H2
Zn + H2SO4 === ZnSO4 + H2
Fe + H2SO4 === FeSO4 + H2
返回铝丝表面出现红色物质溶液由蓝色变成无色Al + CuSO4 —
Al2﹙SO4﹚3+ Cu332铜丝表面出现银白色物质溶液由无色变成蓝色Cu+ AgNO3 — Cu﹙NO3﹚2+ Ag22======无现象三、金属与其它化合物的反应结论三:
Al Cu Ag
金属活动性由强减弱 返回金属活动性顺序: K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱 金属活动性顺序的应用:1.在金属活动性顺序里,金属的位置越前,它的活动性越强。2.在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。3.在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。练习1.判断下列反应能否发生,能发生的写出化学方程式,不能发生的说明原因。
⑴银和稀硫酸
⑵铁和稀盐酸
⑶铜和硫酸锌溶液
⑷锌和硫酸铜溶液
⑸镁和硝酸银溶液
⑹铜和氯化银固体2. “药金”又称为“愚人金”,实为铜、锌合金。由于“药金”外观与黄金相似,常被不法商贩用来冒充黄金牟取暴利。请你设计实验,证明实验台上的“药金”戒指是假黄金戒指。
同课章节目录
