金属的化学性质[下学期]
文档属性
| 名称 | 金属的化学性质[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 639.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-02-15 00:00:00 | ||
图片预览




文档简介
课件18张PPT。化学性质崇礼中学 化学教研组第八单元 课题2金属deFeCuMgZn1、你知道那些金属可以和氧气反应吗? 镁、铝比较活泼,铁、铜次之,金最不活泼。2、你知道它们和氧气反应的条件吗?一.金属与氧气的反应讨论结论:1.不同的金属与氧气的反应条
件不同. 2.与氧气反应条件的不同,说明金属
的化学活动性不同.通过金属与氧气反应的条件的难易,可以得出金属的
活动性不同,那么还有其他的方法判断金属的活动性
吗?资料:
16世纪中叶,瑞士化学家帕拉塞斯和17世纪的一些
化学家,都发现了有些金属和酸可以反应生成一种可
燃性气体---氢气.并且发现不同的金属反应的剧烈
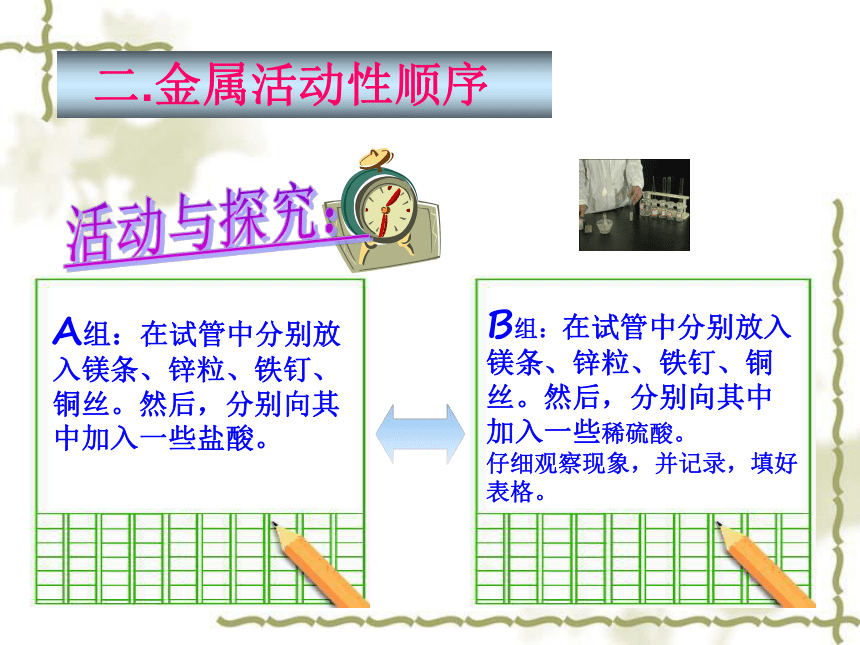
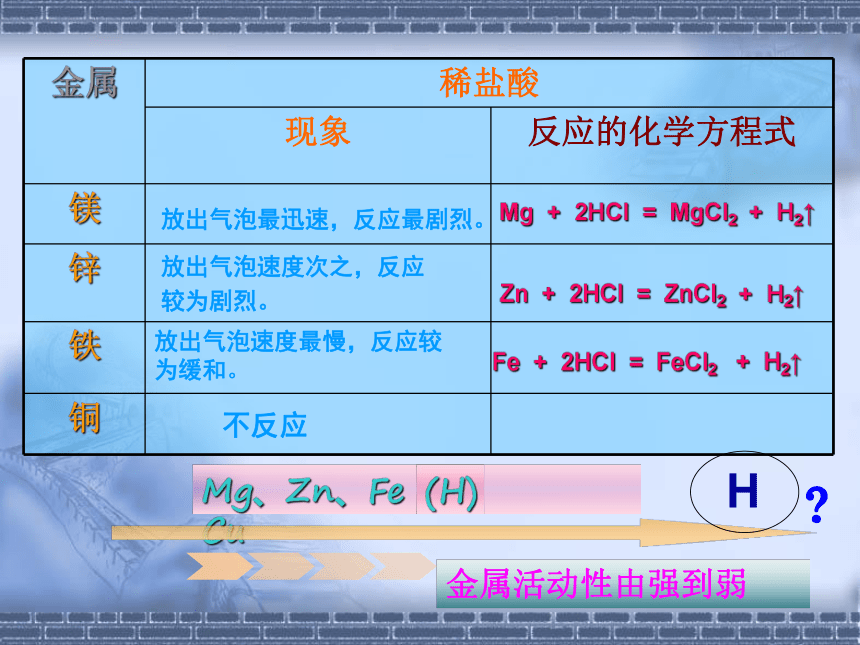
程度不同.活动与探究:Mg + 2HCl = MgCl2 + H2↑金属活动性由强到弱单质化合物化合物单质小结:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。
讨论: 对于以上的反应,从反应物和生成物的角度
分析,这些反应有何特点?将这一类反应与化合反
应、分解反应进行比较。
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Fe + 2HCl = FeCl2 + H2 ↑
化合反应:
分解反应:
置换反应:
多变一。一变多。让我们来对比:A+B→ABAB → A+BA+BC→B+AC说明:铁能把铜从硫酸铜溶液中反应出来,这也是比较金属活动性的依据之一。现象:_________________________________________________
________________________________________________________将铁钉投入到硫酸铜溶液中有何现象? 铁钉表面会有红色物质析出,若时间足够
长,则溶液会从蓝色变为浅绿色。Fe + CuSO4 = Cu + FeSO4 该反应的化学方程式:回忆:活动性:Fe﹥Cu活动与探究:利用Al丝Cu丝及 CuSO4 AgNO3 Al2(SO4)3溶液判断Al Cu Ag的活动性浸入溶液中的铝丝
表面覆盖一层紫红
色物质,溶液由蓝
色逐渐变为无色。浸入溶液中的铜丝
表面覆盖一层银白
色物质,溶液由无
色逐渐变为蓝色。不反应2Al + 3CuSO4= Al2(SO4)3 + 3CuCu +2Ag NO3 =Cu(NO3)2 + 2Ag根据刚才的实验填写表格以上三种金属活动性顺序为:
Al Cu Ag
金属活动性由强到弱 常见金属的活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au金属活动性顺序由强逐渐减弱结论:3.在金属活动顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液中反应出来.金属活动性顺序的应用:1.在金属活动顺序里,金属的位置越靠前,它的活动性
就越强.
2.在金属活动性顺序里,位于氢之前的金属能反应出
盐酸(稀硫酸)中的氢.
1.判断下列物质能否发生反应?若能,
写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
解答:可发生反应的:(2)(4)(6)
化学方程式:(2)Zn + CuSO4 = Cu + ZnSO4(4)Al +3AgNO3 = Al(NO3)3 + 3Ag(6)Mg + FeSO4 = MgSO4 +Fe练习: 2.有X Y Z三种金属,如果把X和Y分别放入
稀硫酸中, X 溶解并产生氢气,Y不反应;如果
把Y和Z分别放入硝酸银溶液中,过一会儿,在Y
的表面有银析出,而Z无变化.根据以上事实,判
断X Y Z的金属活动顺序.解答: 金属活动性顺序 X>Y>Z谢谢大家!
件不同. 2.与氧气反应条件的不同,说明金属
的化学活动性不同.通过金属与氧气反应的条件的难易,可以得出金属的
活动性不同,那么还有其他的方法判断金属的活动性
吗?资料:
16世纪中叶,瑞士化学家帕拉塞斯和17世纪的一些
化学家,都发现了有些金属和酸可以反应生成一种可
燃性气体---氢气.并且发现不同的金属反应的剧烈
程度不同.活动与探究:Mg + 2HCl = MgCl2 + H2↑金属活动性由强到弱单质化合物化合物单质小结:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。
讨论: 对于以上的反应,从反应物和生成物的角度
分析,这些反应有何特点?将这一类反应与化合反
应、分解反应进行比较。
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Fe + 2HCl = FeCl2 + H2 ↑
化合反应:
分解反应:
置换反应:
多变一。一变多。让我们来对比:A+B→ABAB → A+BA+BC→B+AC说明:铁能把铜从硫酸铜溶液中反应出来,这也是比较金属活动性的依据之一。现象:_________________________________________________
________________________________________________________将铁钉投入到硫酸铜溶液中有何现象? 铁钉表面会有红色物质析出,若时间足够
长,则溶液会从蓝色变为浅绿色。Fe + CuSO4 = Cu + FeSO4 该反应的化学方程式:回忆:活动性:Fe﹥Cu活动与探究:利用Al丝Cu丝及 CuSO4 AgNO3 Al2(SO4)3溶液判断Al Cu Ag的活动性浸入溶液中的铝丝
表面覆盖一层紫红
色物质,溶液由蓝
色逐渐变为无色。浸入溶液中的铜丝
表面覆盖一层银白
色物质,溶液由无
色逐渐变为蓝色。不反应2Al + 3CuSO4= Al2(SO4)3 + 3CuCu +2Ag NO3 =Cu(NO3)2 + 2Ag根据刚才的实验填写表格以上三种金属活动性顺序为:
Al Cu Ag
金属活动性由强到弱 常见金属的活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au金属活动性顺序由强逐渐减弱结论:3.在金属活动顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液中反应出来.金属活动性顺序的应用:1.在金属活动顺序里,金属的位置越靠前,它的活动性
就越强.
2.在金属活动性顺序里,位于氢之前的金属能反应出
盐酸(稀硫酸)中的氢.
1.判断下列物质能否发生反应?若能,
写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
解答:可发生反应的:(2)(4)(6)
化学方程式:(2)Zn + CuSO4 = Cu + ZnSO4(4)Al +3AgNO3 = Al(NO3)3 + 3Ag(6)Mg + FeSO4 = MgSO4 +Fe练习: 2.有X Y Z三种金属,如果把X和Y分别放入
稀硫酸中, X 溶解并产生氢气,Y不反应;如果
把Y和Z分别放入硝酸银溶液中,过一会儿,在Y
的表面有银析出,而Z无变化.根据以上事实,判
断X Y Z的金属活动顺序.解答: 金属活动性顺序 X>Y>Z谢谢大家!
同课章节目录
