甲烷[下学期]
图片预览





文档简介
课件22张PPT。甲烷1.了解烃的基本要概念.
2.了解甲烷的电子式、结构式和甲烷的正四面体结构.烃:只含有碳和氢两种元素的有机物
又称碳氢化合物练习:下列物质属于烃的是:
1、H2S 2、C2H2 3、CH3Cl 4、CH3CH2OH 5、CH4 6、CH3COOH 7、H2 8、金刚石 9、CO2 10、C2H4烃的分类:根据结构不同,
可以分为烷烃、烯烃、炔烃、芳香烃练习:
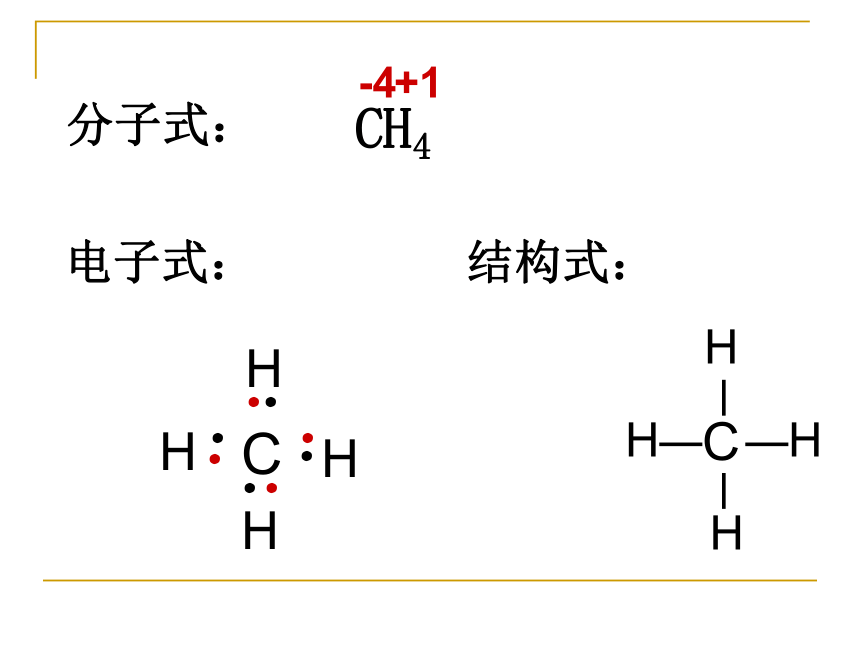
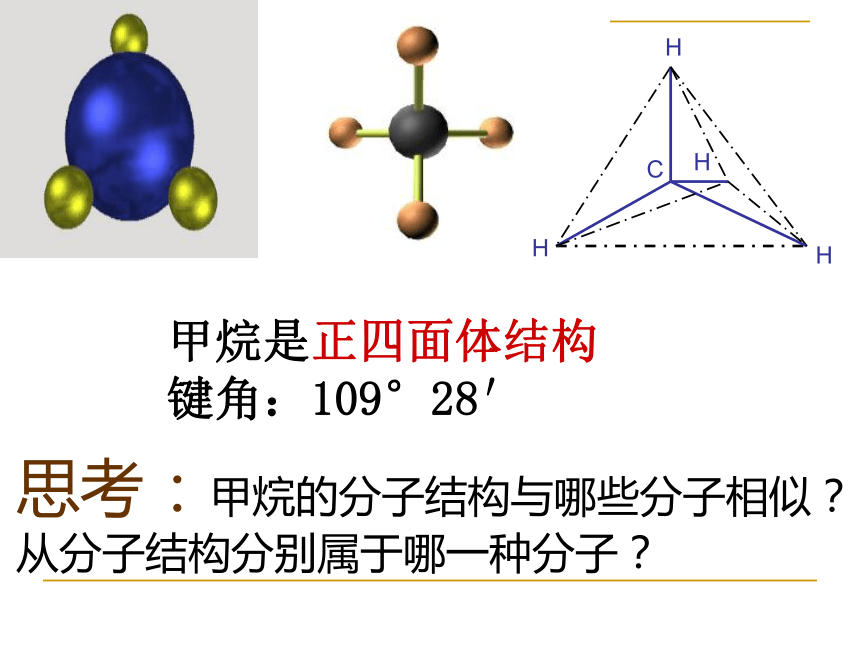
已知甲烷在标准状况下的密度为0.717g/L,甲烷中碳的质量分数为75%,氢的质量分数为25%,求甲烷的分子式 甲烷---最简单的烷烃分子式:CH4-4+1电子式:结构式:甲烷是正四面体结构
键角:109°28′思考:甲烷的分子结构与哪些分子相似?
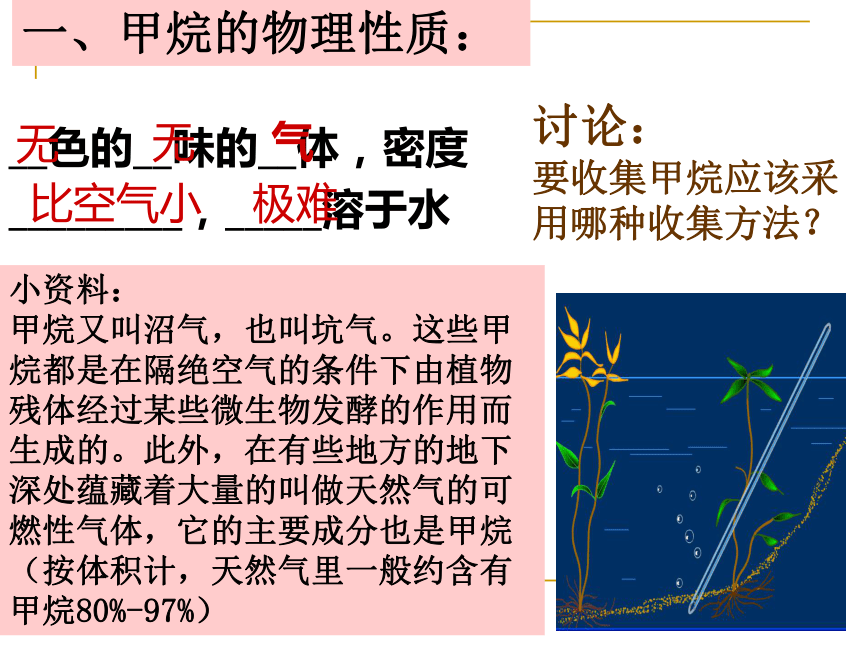
从分子结构分别属于哪一种分子? 一、甲烷的物理性质:__色的__味的__体,密度_________,_____溶于水无无气比空气小极难讨论:
要收集甲烷应该采用哪种收集方法? 小资料:
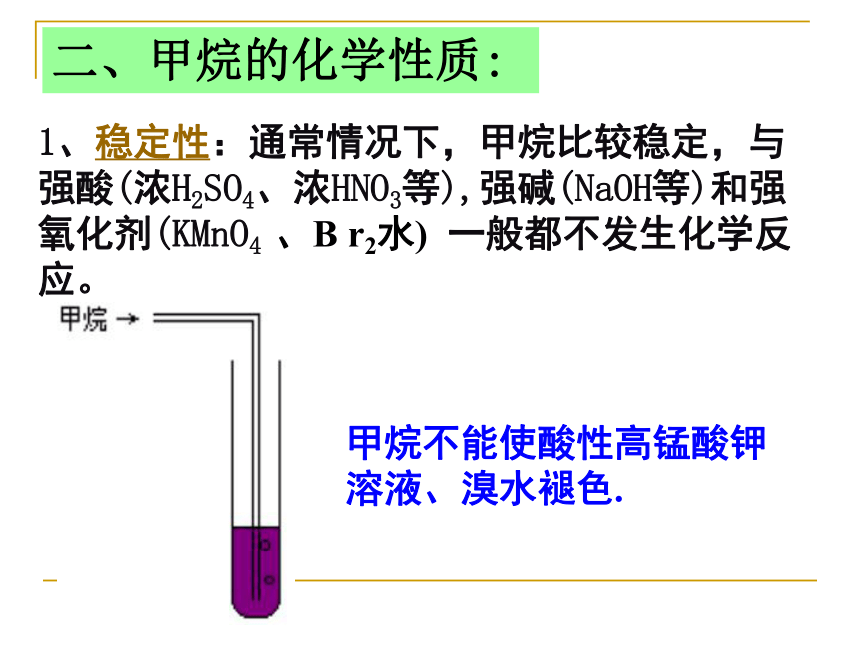
甲烷又叫沼气,也叫坑气。这些甲烷都是在隔绝空气的条件下由植物残体经过某些微生物发酵的作用而生成的。此外,在有些地方的地下深处蕴藏着大量的叫做天然气的可燃性气体,它的主要成分也是甲烷(按体积计,天然气里一般约含有甲烷80%-97%)1、稳定性:通常情况下,甲烷比较稳定,与强酸(浓H2SO4、浓HNO3等),强碱(NaOH等)和强氧化剂(KMnO4 、B r2水) 一般都不发生化学反应。甲烷不能使酸性高锰酸钾溶液、溴水褪色.二、甲烷的化学性质: 2、可燃性:现象:火焰呈蓝色并有水滴和能使澄清石灰水变浑浊的气体产生注意:点燃前必须验纯,否则可能发生爆炸!CH4可用作燃料空气中甲烷的含量在5%-15%(爆炸极限)就会发生爆炸。为了防止瓦斯爆炸,在煤矿矿井中应该采用通风,严禁烟火等安全措施思考:如何鉴别H2、CO、CH4?点燃,根据它们的燃烧产物进行鉴别。3、热分解: 甲烷是橡胶工业的重要原料,CH4可用于制炭黑和H2。H2可用于制NH3和汽油。炭黑是橡胶工业的重要原料,也可以用来制造颜料、油墨、油漆等3、取代反应(特征反应):实验!甲烷与氯气的反应实验现象:①量筒内气体的黄绿色逐渐变浅;
②量筒内壁出现油状液滴;
③量筒内液面上升;注:
不要放在日光直接照射的地方,否则会引起爆炸H+Cl一氯甲烷二氯甲烷三氯甲烷思考:
甲烷中加入氯气,在光照的条件下产物是什么?1mol甲烷在光照条件下最多可与多少氯气发生取代? 有机物分子中的某些原子或原子团被其他原子或原子团代替的反应甲烷能与卤素单质(如Cl2,Br2)发生连续取代反应,生成不同的四种卤代物。取代反应和置换反应的比较可与单质或化合物发生取代,生成物中往往没有单质反应物与生成物中均有单质反应是共价键断裂而交换原子或原子团,受反应条件的影响大,逐步取代,很多反应是可逆的,速率慢反应往往发生于水溶液中,有离子参加,遵循金属或非金属活动顺序,反应一般单向进行,速率快练习:
1、在光照条件下,将等体积的甲烷和氯气混合,得到产物物质的量最多的是:
A、CH3Cl B、CH2Cl2
C、CCl4 D、HCl
2、向下列物质的水溶液中加入硝酸银溶液,能得到白色沉淀的是:
A、CH3Cl B、NaCl C、KClO3
D、CCl4 E、HCl三、实验室制法:药品:无水醋酸钠、碱石灰注:
不能用醋酸钠晶体!(CH3COONa·3H2O)CaO的作用:
1、干燥剂(吸收反应产生的水分)
2、防止试管炸裂(高温下NaOH与玻璃反应)
3、CaO可使混合物疏松,便于CH4逸出实验装置:与氧气相同例1、1molCH4与一定量的Cl2发生取代反应,待反应完全后测得4种取代物质的量相等,则消耗Cl2为( )
A、0.5mol B、2mol
C、2.5mol D、4molC例2、某气态烃对空气相对密度为2,在氧气中充分燃烧1.16g这种烃,并将所得产物通过装有无水氯化钙的干燥的干燥管和装有碱石灰的干燥管.当称量这两个干燥管的质量时,它们依次增重1.8g和3.52g,求这种烃的化学式.例3、一定量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气重49.6g,当其缓缓经过无水CaCl2中,CaCl2增重25.2g,则原混合气中CO2质量为( )
A.12.5g B.13.2 g C.19.7 g D.24.4gB例4.将定量的 CH4、O2、Na2O2密封于一密闭容器中,在150℃条件下,用电火花引燃混合气,反应结束后若容器中压强近似为零,且残余物质溶于水无气体产生,则CH4、O2、Na2O2三种物质的量之比为( )
A.1:2:3 B.2:1:6
C.2:1:4 D.3:2:1B例5、瓦斯爆炸是空气中含CH45%~15%(体积分数)遇火所产生的,发生爆炸最强烈时,CH4在空气中的体积分数约是( )
A、10.5% B、9.1%
C、8% D、5% B
2.了解甲烷的电子式、结构式和甲烷的正四面体结构.烃:只含有碳和氢两种元素的有机物
又称碳氢化合物练习:下列物质属于烃的是:
1、H2S 2、C2H2 3、CH3Cl 4、CH3CH2OH 5、CH4 6、CH3COOH 7、H2 8、金刚石 9、CO2 10、C2H4烃的分类:根据结构不同,
可以分为烷烃、烯烃、炔烃、芳香烃练习:
已知甲烷在标准状况下的密度为0.717g/L,甲烷中碳的质量分数为75%,氢的质量分数为25%,求甲烷的分子式 甲烷---最简单的烷烃分子式:CH4-4+1电子式:结构式:甲烷是正四面体结构
键角:109°28′思考:甲烷的分子结构与哪些分子相似?
从分子结构分别属于哪一种分子? 一、甲烷的物理性质:__色的__味的__体,密度_________,_____溶于水无无气比空气小极难讨论:
要收集甲烷应该采用哪种收集方法? 小资料:
甲烷又叫沼气,也叫坑气。这些甲烷都是在隔绝空气的条件下由植物残体经过某些微生物发酵的作用而生成的。此外,在有些地方的地下深处蕴藏着大量的叫做天然气的可燃性气体,它的主要成分也是甲烷(按体积计,天然气里一般约含有甲烷80%-97%)1、稳定性:通常情况下,甲烷比较稳定,与强酸(浓H2SO4、浓HNO3等),强碱(NaOH等)和强氧化剂(KMnO4 、B r2水) 一般都不发生化学反应。甲烷不能使酸性高锰酸钾溶液、溴水褪色.二、甲烷的化学性质: 2、可燃性:现象:火焰呈蓝色并有水滴和能使澄清石灰水变浑浊的气体产生注意:点燃前必须验纯,否则可能发生爆炸!CH4可用作燃料空气中甲烷的含量在5%-15%(爆炸极限)就会发生爆炸。为了防止瓦斯爆炸,在煤矿矿井中应该采用通风,严禁烟火等安全措施思考:如何鉴别H2、CO、CH4?点燃,根据它们的燃烧产物进行鉴别。3、热分解: 甲烷是橡胶工业的重要原料,CH4可用于制炭黑和H2。H2可用于制NH3和汽油。炭黑是橡胶工业的重要原料,也可以用来制造颜料、油墨、油漆等3、取代反应(特征反应):实验!甲烷与氯气的反应实验现象:①量筒内气体的黄绿色逐渐变浅;
②量筒内壁出现油状液滴;
③量筒内液面上升;注:
不要放在日光直接照射的地方,否则会引起爆炸H+Cl一氯甲烷二氯甲烷三氯甲烷思考:
甲烷中加入氯气,在光照的条件下产物是什么?1mol甲烷在光照条件下最多可与多少氯气发生取代? 有机物分子中的某些原子或原子团被其他原子或原子团代替的反应甲烷能与卤素单质(如Cl2,Br2)发生连续取代反应,生成不同的四种卤代物。取代反应和置换反应的比较可与单质或化合物发生取代,生成物中往往没有单质反应物与生成物中均有单质反应是共价键断裂而交换原子或原子团,受反应条件的影响大,逐步取代,很多反应是可逆的,速率慢反应往往发生于水溶液中,有离子参加,遵循金属或非金属活动顺序,反应一般单向进行,速率快练习:
1、在光照条件下,将等体积的甲烷和氯气混合,得到产物物质的量最多的是:
A、CH3Cl B、CH2Cl2
C、CCl4 D、HCl
2、向下列物质的水溶液中加入硝酸银溶液,能得到白色沉淀的是:
A、CH3Cl B、NaCl C、KClO3
D、CCl4 E、HCl三、实验室制法:药品:无水醋酸钠、碱石灰注:
不能用醋酸钠晶体!(CH3COONa·3H2O)CaO的作用:
1、干燥剂(吸收反应产生的水分)
2、防止试管炸裂(高温下NaOH与玻璃反应)
3、CaO可使混合物疏松,便于CH4逸出实验装置:与氧气相同例1、1molCH4与一定量的Cl2发生取代反应,待反应完全后测得4种取代物质的量相等,则消耗Cl2为( )
A、0.5mol B、2mol
C、2.5mol D、4molC例2、某气态烃对空气相对密度为2,在氧气中充分燃烧1.16g这种烃,并将所得产物通过装有无水氯化钙的干燥的干燥管和装有碱石灰的干燥管.当称量这两个干燥管的质量时,它们依次增重1.8g和3.52g,求这种烃的化学式.例3、一定量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气重49.6g,当其缓缓经过无水CaCl2中,CaCl2增重25.2g,则原混合气中CO2质量为( )
A.12.5g B.13.2 g C.19.7 g D.24.4gB例4.将定量的 CH4、O2、Na2O2密封于一密闭容器中,在150℃条件下,用电火花引燃混合气,反应结束后若容器中压强近似为零,且残余物质溶于水无气体产生,则CH4、O2、Na2O2三种物质的量之比为( )
A.1:2:3 B.2:1:6
C.2:1:4 D.3:2:1B例5、瓦斯爆炸是空气中含CH45%~15%(体积分数)遇火所产生的,发生爆炸最强烈时,CH4在空气中的体积分数约是( )
A、10.5% B、9.1%
C、8% D、5% B
