乙醛[下学期]
图片预览






文档简介
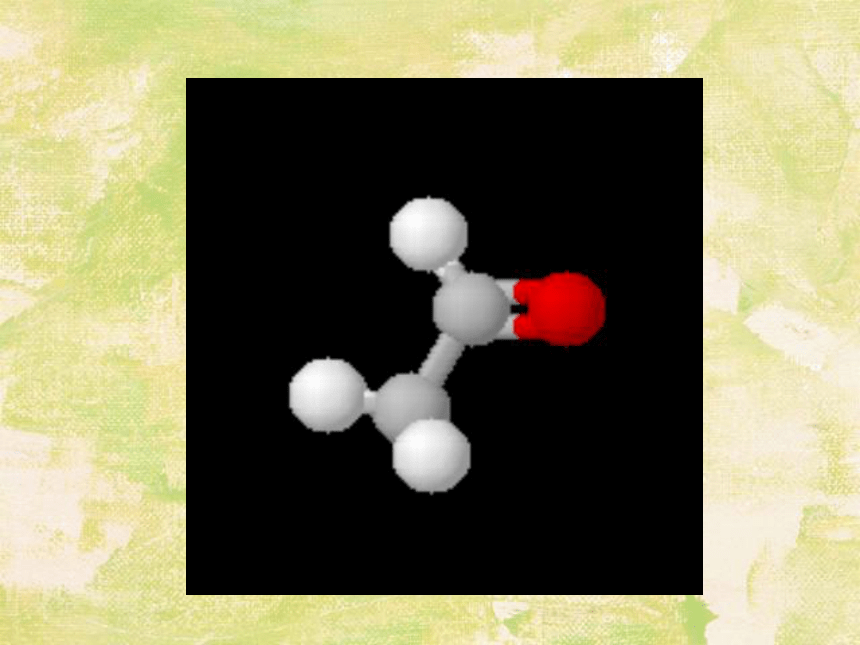
课件24张PPT。第五节 乙醛 醛类一、乙醛的结构1、官能团2、饱和一元醛的通式CnH2n+1CHO 或CnH2nOR—CHO醛基二、乙醛的性质物理性质1、乙醛常温下为无色有刺激性气味的液体,
密度比水小,能与水、乙醇、乙醚
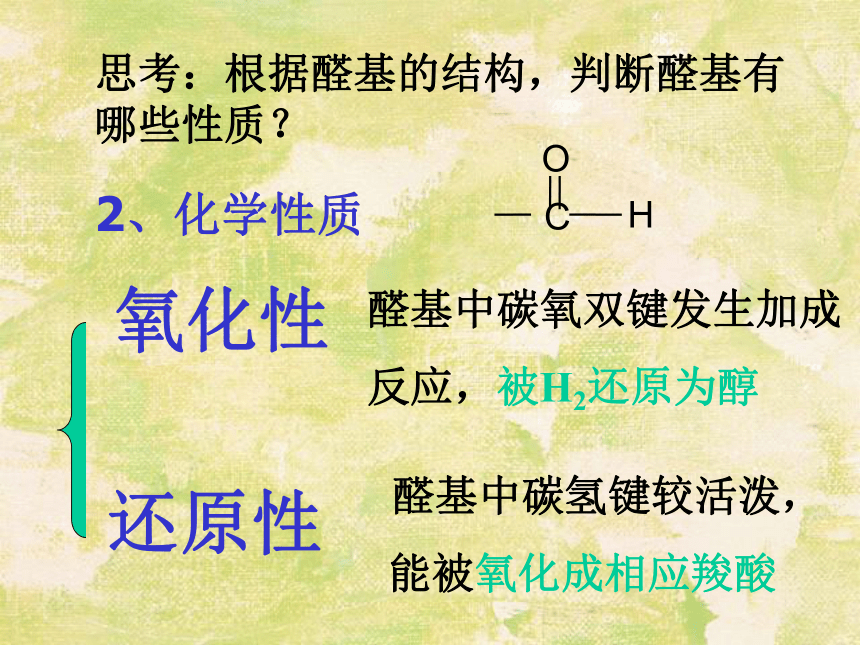
氯仿等互溶。思考:根据醛基的结构,判断醛基有哪些性质? 醛基中碳氧双键发生加成
反应,被H2还原为醇 醛基中碳氢键较活泼,
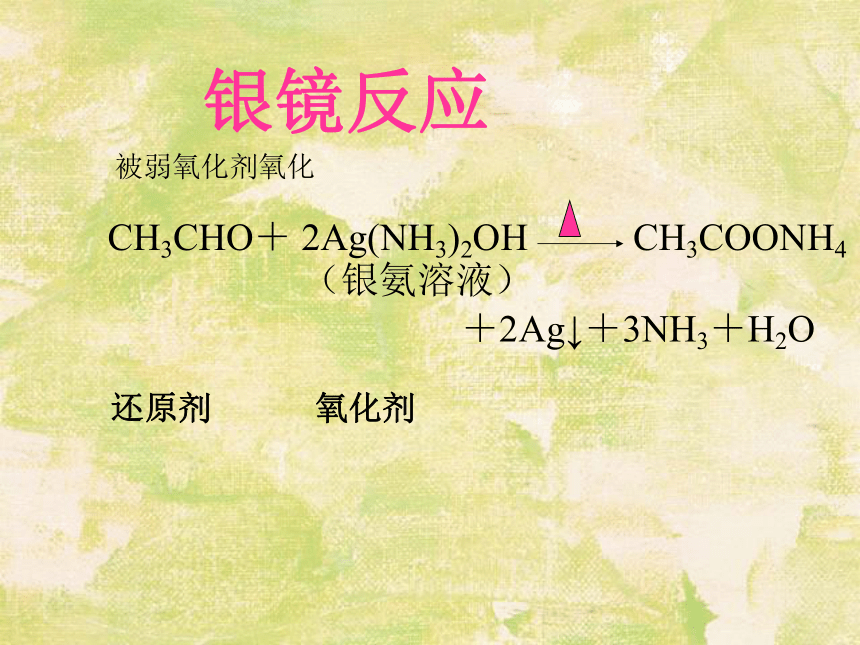
能被氧化成相应羧酸氧化性还原性2、化学性质银镜反应实验 :取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。 :在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。1、配制银氨溶液2、水浴加热生成银镜注意事项(1)试管内壁必须洁净;
(2)必须水浴;
(3)加热时不可振荡和摇动试管;
(4)须用新配制的银氨溶液;
(5)乙醛用量不可太多;
(6)实验后,银镜用HNO3浸泡,再用水洗银镜反应还原剂氧化剂被弱氧化剂氧化与新制的氢氧化铜反应实验1、配制新制的Cu(OH)2悬浊液:在2ml10%NaOH溶液中滴入2%CuSO4溶液4~8滴,振荡。2、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙醛溶液,碱必须过量
加热至沸腾。乙醛和新制的氢氧化铜反应 氧化剂还原剂常用的氧化剂:银氨溶液、新制的Cu(OH)2、O2、
酸性KMnO4溶液三、醛基的检验1、*哪些有机物中含有—CHO?
2、怎样检验醛基的存在?醛、HCOOH、HCOOR、
葡萄糖、麦芽糖新制的Cu(OH)2银镜反应*四、乙醛的工业制法1、乙炔水化法2、乙烯氧化法五:甲醛1、结构 2、性质 :与乙醛相似不同点: 1、常温下甲醛为无色有刺激性气味的气体
2、甲醛中有2个活泼氢可被氧化(点击观看放大图片)3、应用:(1)甲醛的水溶液叫福尔马林,具有防腐和杀菌能力。
(2)能合成酚醛树脂六、知识运用 1、判断下列哪些能使酸性KMnO4溶液褪色?乙烯、甲烷、苯、 乙酸、甲苯、乙醛、葡萄糖、SO2、H2S、苯酚、聚异戊二烯、裂化汽油2、用一种试剂鉴别乙醇、乙醛、乙酸、 甲酸四种无色液体新制的Cu(OH)2甲烷、苯、 乙酸3、已知柠檬醛的结构简式为
CH3C=CHCH2CH2CH=CHCH
CH3 O
若要检验出其中的碳碳双键,其方法是———————————— 先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化。然后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色4、迁移应用 RC=O +H-CH2CHOH根据上述信息,用乙炔合成1-丁醇。现有一化合物A,是由B、C两物质通过上述物质的反应生成的。试根据A的结构式写出B、C的结构式 CH3 H
A:CH3-C-CH2-C=O
OH B:C:CH3CHO醛可看成醛基取代了烃中的氢原子,书写同分异构体时应把醛写成
想一想:如何写出C5H10O表示醛的同分异构体R-CHO再判断烃基-R有几种同分异构体C5H10O→C4H9CHOC4H9C4H9-C4H9有四种同分异构体结束返回
密度比水小,能与水、乙醇、乙醚
氯仿等互溶。思考:根据醛基的结构,判断醛基有哪些性质? 醛基中碳氧双键发生加成
反应,被H2还原为醇 醛基中碳氢键较活泼,
能被氧化成相应羧酸氧化性还原性2、化学性质银镜反应实验 :取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。 :在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。1、配制银氨溶液2、水浴加热生成银镜注意事项(1)试管内壁必须洁净;
(2)必须水浴;
(3)加热时不可振荡和摇动试管;
(4)须用新配制的银氨溶液;
(5)乙醛用量不可太多;
(6)实验后,银镜用HNO3浸泡,再用水洗银镜反应还原剂氧化剂被弱氧化剂氧化与新制的氢氧化铜反应实验1、配制新制的Cu(OH)2悬浊液:在2ml10%NaOH溶液中滴入2%CuSO4溶液4~8滴,振荡。2、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙醛溶液,碱必须过量
加热至沸腾。乙醛和新制的氢氧化铜反应 氧化剂还原剂常用的氧化剂:银氨溶液、新制的Cu(OH)2、O2、
酸性KMnO4溶液三、醛基的检验1、*哪些有机物中含有—CHO?
2、怎样检验醛基的存在?醛、HCOOH、HCOOR、
葡萄糖、麦芽糖新制的Cu(OH)2银镜反应*四、乙醛的工业制法1、乙炔水化法2、乙烯氧化法五:甲醛1、结构 2、性质 :与乙醛相似不同点: 1、常温下甲醛为无色有刺激性气味的气体
2、甲醛中有2个活泼氢可被氧化(点击观看放大图片)3、应用:(1)甲醛的水溶液叫福尔马林,具有防腐和杀菌能力。
(2)能合成酚醛树脂六、知识运用 1、判断下列哪些能使酸性KMnO4溶液褪色?乙烯、甲烷、苯、 乙酸、甲苯、乙醛、葡萄糖、SO2、H2S、苯酚、聚异戊二烯、裂化汽油2、用一种试剂鉴别乙醇、乙醛、乙酸、 甲酸四种无色液体新制的Cu(OH)2甲烷、苯、 乙酸3、已知柠檬醛的结构简式为
CH3C=CHCH2CH2CH=CHCH
CH3 O
若要检验出其中的碳碳双键,其方法是———————————— 先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化。然后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色4、迁移应用 RC=O +H-CH2CHOH根据上述信息,用乙炔合成1-丁醇。现有一化合物A,是由B、C两物质通过上述物质的反应生成的。试根据A的结构式写出B、C的结构式 CH3 H
A:CH3-C-CH2-C=O
OH B:C:CH3CHO醛可看成醛基取代了烃中的氢原子,书写同分异构体时应把醛写成
想一想:如何写出C5H10O表示醛的同分异构体R-CHO再判断烃基-R有几种同分异构体C5H10O→C4H9CHOC4H9C4H9-C4H9有四种同分异构体结束返回
