江苏 选修5第三章第三节羧酸 酯(第1课时)PPT[下学期]
文档属性
| 名称 | 江苏 选修5第三章第三节羧酸 酯(第1课时)PPT[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 812.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-05-24 00:00:00 | ||
图片预览







文档简介
课件45张PPT。新课标人教版选修五有机化学基础第三章烃的含氧衍生物江苏省淮安中学 张正飞
2019年2月28日星期四第三节 羧酸 酯
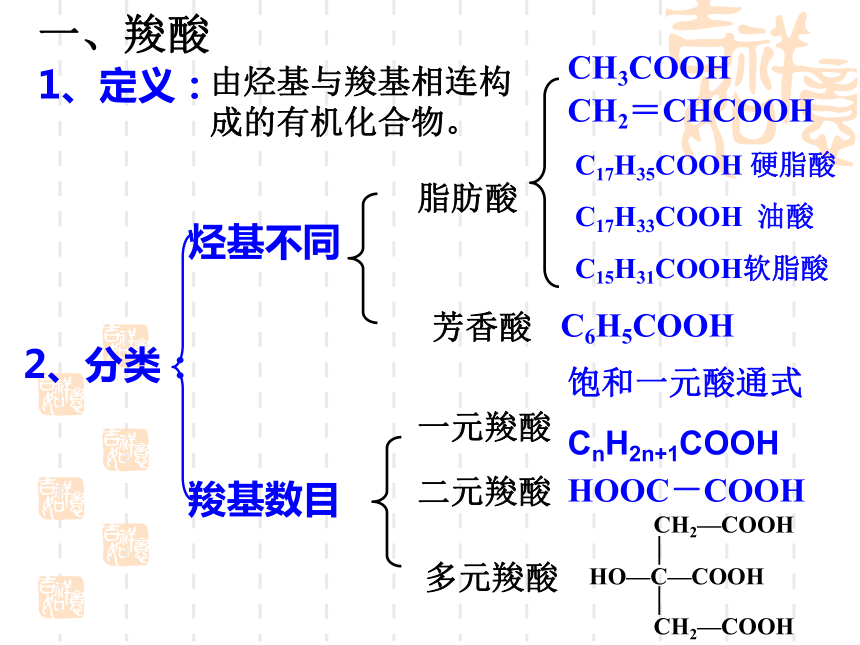
第一课时 醋酸 乙酸CH3COOH一、羧酸1、定义:由烃基与羧基相连构成的有机化合物。2、分类:烃基不同羧基数目芳香酸脂肪酸一元羧酸二元羧酸多元羧酸CH3COOHCH2=CHCOOHC17H35COOH 硬脂酸
C17H33COOH 油酸
C15H31COOH软脂酸C6H5COOHHOOC-COOH饱和一元酸通式
CnH2n+1COOH(1)甲酸 HCOOH (蚁酸)(2)苯甲酸 C6H5COOH (安息香酸)(3)草酸 HOOC-COOH
(乙二酸)(4)羟基酸:如柠檬酸:3、自然界中的有机酸(5)高级脂肪酸:硬脂酸、
软脂酸(饱和)、油酸(不饱和)等。1、乙酸的物理性质【思考与交流】在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。 二、乙酸在日常生活中,我们可以用醋除去水垢,
(水垢的主要成分:Mg(OH)2和CaCO3)
说明乙酸什么性质?并写出化学方程式。【思考与交流】2CH3COOH + CaCO3 = Ca(CH3COO)2 +H2O+CO2↑
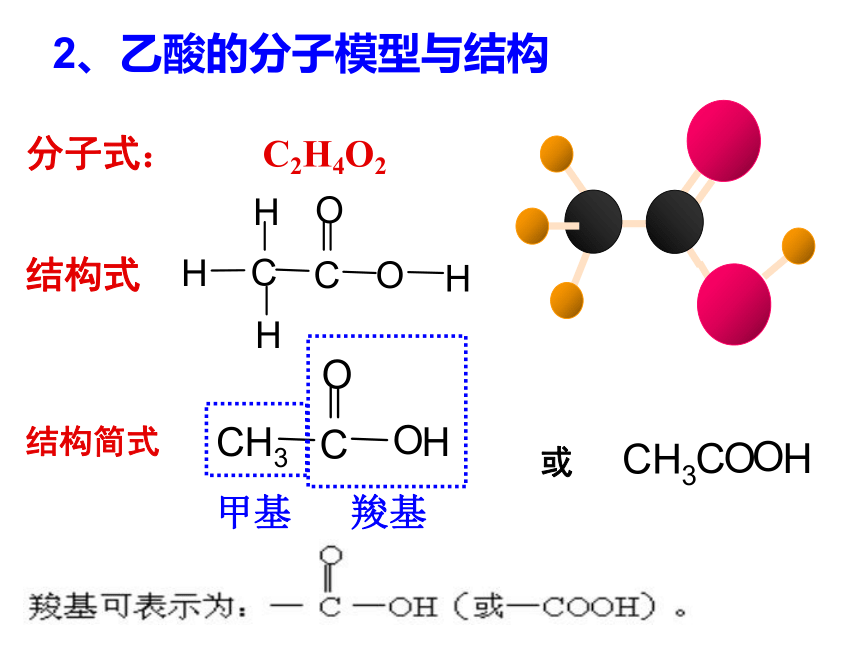
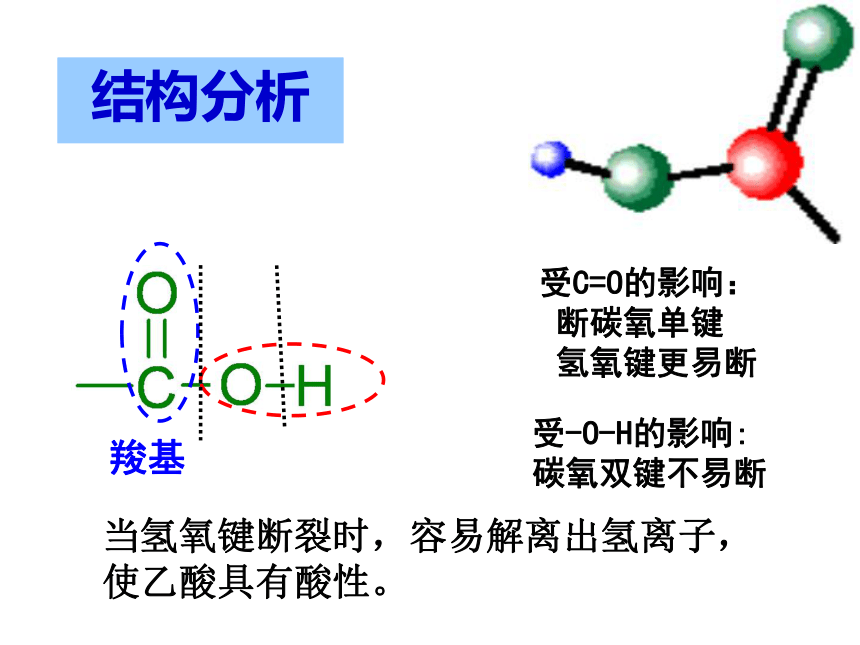
2CH3COOH + Mg(OH)2 = Mg(CH3COO)2 +2H2O说明乙酸具有酸性2、乙酸的分子模型与结构甲基羧基分子式:结构式结构简式或C2H4O2结构分析羧基受C=O的影响:
断碳氧单键
氢氧键更易断受-O-H的影响:
碳氧双键不易断当氢氧键断裂时,容易解离出氢离子,使乙酸具有酸性。科
学
探
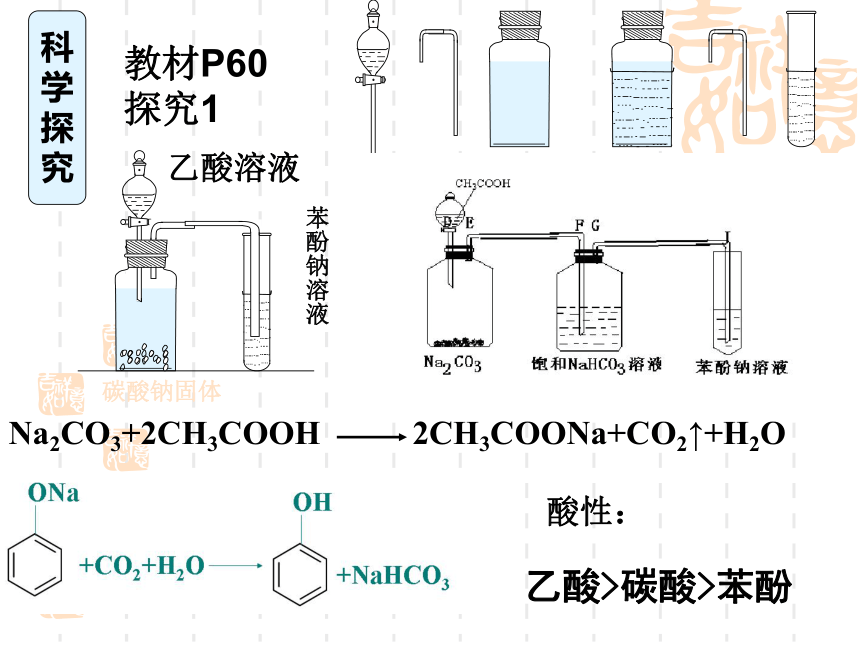
究酸性:乙酸>碳酸>苯酚教材P60探究12CH3COOH + Na2CO3 = 2CH3COONa +H2O+CO2↑2CH3COOH + Fe = Fe (CH3COO)2+H2↑CH3COOH + NaOH = CH3COONa+ H2O2CH3COOH+Na2O=2CH3COONa+2H2O3、乙酸的化学性质(1) 弱酸性:【思考 交流】证明乙酸是弱酸的方法:
1:配制一定浓度的乙酸测定PH值
2:配制一定浓度的乙酸钠溶液测定PH值
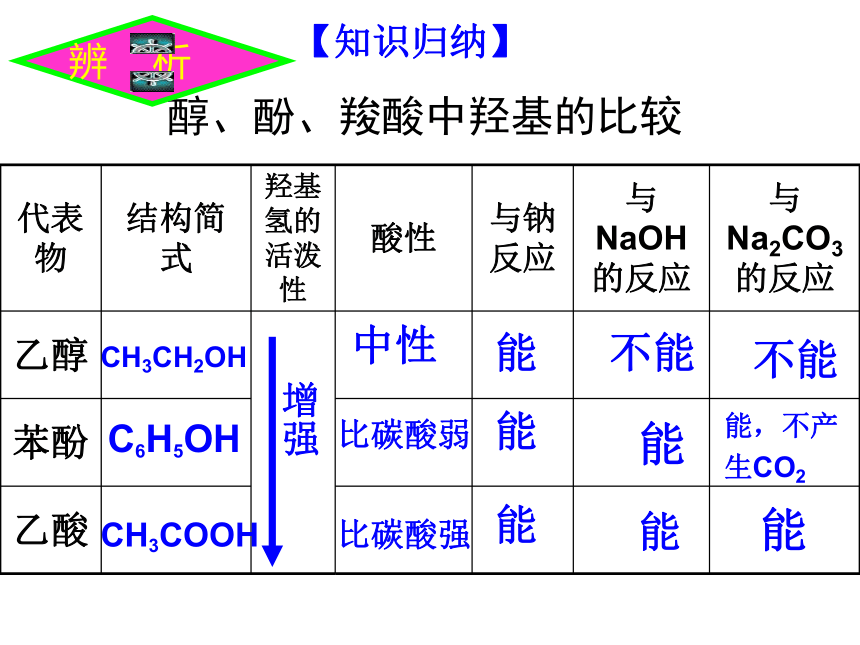
3:在相同条件下与同浓度的盐酸比较与金属反应的速率思考1:写出乙酸与Na、NaOH、Na2CO3反应的化学方程式。思考2:可以用几种方法证明乙酸是弱酸?CH3CH2OHC6H5OHCH3COOH增强中性比碳酸弱比碳酸强能能能能能不能不能能能,不产
生CO2醇、酚、羧酸中羟基的比较【知识归纳】 1、化合物 跟足量的下列哪种物质的溶液反应可得到一钠盐C7H5O3Na( )A NaOH B Na2CO3
C NaHCO3 D NaCl C【知识应用】2.确定乙酸是弱酸的依据是( )
A.乙酸可以和乙醇发生酯化反应
B.乙酸钠的水溶液显碱性
C.乙酸能使石蕊试液变红
D.Na2CO3中加入乙酸产生CO2
B3、请用一种试剂鉴别下面三种有机物?乙醇、乙醛、乙酸新制Cu(OH)2悬浊液碎瓷片
乙醇 3mL
浓硫酸 2mL
乙酸 2mL
饱和的Na2CO3溶液(2)乙酸的酯化反应(防止暴沸)反应后饱和Na2CO3溶液上层有什么现象?饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。定义:酸和醇起作用,生成酯和水的反应。
本质:酸脱羟基、醇脱羟基氢。 【知识回顾】1. 试管倾斜加热的目的是什么?
2.浓硫酸的作用是什么?
3.得到的反应产物是否纯净?主要杂质有哪些?
4.饱和Na2CO3溶液有什么作用?
5. 为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?催化剂,吸水剂不纯净;乙酸、乙醇① 中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味. ② 溶解乙醇。
③ 冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。防止受热不匀发生倒吸增大受热面积【探究】乙酸乙酯的酯化过程 ——酯化反应的脱水方式可能一可能二同位素示踪法酯化反应:酸和醇起作用,生成酯和水的反应。
酯化反应的本质:酸脱羟基、醇脱羟基氢。 实验验证C5、 若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )A 1种 B 2种 C 3 种 D 4种生成物中水的相对分子质量为 。204、 酯化反应属于( ).
A.中和反应 B.不可逆反应
C.离子反应 D.取代反应D【知识应用】【知识迁移】写出下列酸和醇的酯化反应C2H5O—NO2 + H2OCH3COOCH3 + H2O硝酸乙酯乙酸甲酯足量+ 2H2O 二乙酸乙二酯环乙二酸乙二酯【达标测试】1.下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是( )
A.金属钠 B.溴水
C.碳酸钠溶液 D.紫色石蕊试液C D2.除去乙酸乙酯中含有的乙酸,最好的处理和操作是( )
A.蒸馏 B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液 D.用过量氢氧化钠溶液洗涤后分液3.下列物质中,不能与乙醇发生酯化反应的是( )
A.乙醛 B.硝酸 C.苯甲酸 D.硫酸 CA4.关于乙酸的下列说法中不正确的是 ( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸D练 习8.用30g乙酸和46g乙醇反应,如果实际产率是理论产率的85%,则可得到的乙酸乙酯的质量是( )
A.37.4g B.44g
C.74.8g D.88g解: 60 46 88 30g 46g Xg求得: X = 44g实际产量 = 44g x 85% = 37.4g答案: 选 AA新课标人教版选修五有机化学基础第三章烃的含氧衍生物江苏省淮安中学 张正飞
2019年2月28日星期四第三节 羧酸 酯
第二课时1.下列物质中的溴原子在适当条件下都能被羟基所取代,所得产物能跟NaHCO3溶液反应的是( )
A. B. C. D.COHOHOHOH2.胆固醇是人体必需的生物活性物质,分子式为C25H45O,一种胆固醇酯是液晶材料,分子式为C32H49O2,合成这种胆固醇酯的酸是( )
A. C6H13COOH
B. C6H5COOH
C. C7H15COOH
D. C6H5CH2COOHBC25H45O + 酸 → C32H49O2 + H2O二、羧酸1、定义:分子里烃基跟羧基直接相连的有机物。丙酸甲酸苯甲酸乙二酸复习回忆2、结构①一元羧酸通式:R—COOH
②饱和一元羧酸的通式: CnH2n+1COOH
或CnH2nO2
③多元羧酸中含有多个羧基。3、化学性质(1)酸性(2)酯化反应三、三类重要的羧酸1、甲酸——俗称蚁酸结构特点:既有羧基又有醛基化学性质醛基羧基氧化反应(如银镜反应)酸性,酯化反应2、乙二酸——俗称草酸+ 2H2O3、高级脂肪酸(1)酸性(2)酯化反应(3)油酸加成 1mol有机物
最多能消耗下列各物质多少 mol?(1) Na(2) NaOH(3) NaHCO3练习四、酯的概念、命名和通式1.概念:酸跟醇起反应脱水后生成的一类化合物。
练习:写出硝酸和乙醇,苯甲酸和乙醇反应的化学方程式CH3CH2OH+HONO2→CH3CH2ONO2+H2O
硝酸乙酯说出下列化合物的名称:(1)CH3COOCH2CH3
(2)HCOOCH2CH3
(3)CH3CH2O—NO22.酯的命名——“某酸某酯” 3.酯的通式 饱和一元羧酸和饱和一元醇生成的酯
(1)一般通式:
(2)结构通式:
(3)组成通式:CnH2nO2 二、酯的结构、性质及用途1.酯的物理性质
①低级酯是具有芳香气味的液体。
②密度比水小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。 【实验探究】请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶中,以及不同温度下的水解速率。 (1)酯的水解反应在酸性条件好,还是碱性条件好?
(2)酯化反应H2SO4和NaOH哪种作催化剂好?
(3)酯为什么在中性条件下难水解,而在酸、碱性条件下易水解?(碱性)(浓H2SO4)2.酯+水 酸+醇
CH3COOCH2CH3+H2O CH3COOH+CH3CH2OH
CH3COOH + NaOH CH3COONa + H2O酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的【思考与交流】乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?根据化学平衡原理,提高乙酸乙醋产率措施有:由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率;
使用过量的乙醇,可提高乙酸转化为乙酸乙酯产率。
使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。1.酯在下列哪种环境中水解程度最大
A.水 B.稀硫酸
C.浓硫酸 D.碱溶液2.某有机物X能发生水解反应,水解产物为Y和Z。同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是
A.乙酸丙酯 B.甲酸乙酯
C.乙酸甲酯 D.乙酸乙酯3.对有机物
的叙述不正确的是
A.常温下能与Na2CO3反应放出CO2
B.在碱性条件下水解,0.5mol该有机物完全反应消耗4mol NaOH
C.与稀H2SO4共热生成两种有机物
D.该物质的化学式为C14H10O9小结2:几种衍生物之间的关系例2、一环酯化合物,结构简式如下:试推断:
1.该环酯化合物在酸性条件下水解的产物是什么?
写出其结构简式;
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应? 2、烧鱼时,又加酒又加醋,鱼的味道就变得 无腥、香醇、特别鲜美,其原因是 ( )
A.有盐类物质生成 B.有酸类物质生成
C.有醇类物质生成 D.有酯类物质生成1、可以说明乙酸是弱酸的事实是( ) A.乙酸能与水以任意比混溶
B.乙酸能与碳酸钠反应,产生二氧化碳 C.1mol/L的乙酸钠溶液的PH值约为9
D.1mol/L的乙酸水溶液能使紫色石蕊试液变红课堂练习3.写出能发生银镜反应的属于不同类别的物质的结构简式各一种.酯化反应与酯水解反应的比较
2019年2月28日星期四第三节 羧酸 酯
第一课时 醋酸 乙酸CH3COOH一、羧酸1、定义:由烃基与羧基相连构成的有机化合物。2、分类:烃基不同羧基数目芳香酸脂肪酸一元羧酸二元羧酸多元羧酸CH3COOHCH2=CHCOOHC17H35COOH 硬脂酸
C17H33COOH 油酸
C15H31COOH软脂酸C6H5COOHHOOC-COOH饱和一元酸通式
CnH2n+1COOH(1)甲酸 HCOOH (蚁酸)(2)苯甲酸 C6H5COOH (安息香酸)(3)草酸 HOOC-COOH
(乙二酸)(4)羟基酸:如柠檬酸:3、自然界中的有机酸(5)高级脂肪酸:硬脂酸、
软脂酸(饱和)、油酸(不饱和)等。1、乙酸的物理性质【思考与交流】在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。 二、乙酸在日常生活中,我们可以用醋除去水垢,
(水垢的主要成分:Mg(OH)2和CaCO3)
说明乙酸什么性质?并写出化学方程式。【思考与交流】2CH3COOH + CaCO3 = Ca(CH3COO)2 +H2O+CO2↑
2CH3COOH + Mg(OH)2 = Mg(CH3COO)2 +2H2O说明乙酸具有酸性2、乙酸的分子模型与结构甲基羧基分子式:结构式结构简式或C2H4O2结构分析羧基受C=O的影响:
断碳氧单键
氢氧键更易断受-O-H的影响:
碳氧双键不易断当氢氧键断裂时,容易解离出氢离子,使乙酸具有酸性。科
学
探
究酸性:乙酸>碳酸>苯酚教材P60探究12CH3COOH + Na2CO3 = 2CH3COONa +H2O+CO2↑2CH3COOH + Fe = Fe (CH3COO)2+H2↑CH3COOH + NaOH = CH3COONa+ H2O2CH3COOH+Na2O=2CH3COONa+2H2O3、乙酸的化学性质(1) 弱酸性:【思考 交流】证明乙酸是弱酸的方法:
1:配制一定浓度的乙酸测定PH值
2:配制一定浓度的乙酸钠溶液测定PH值
3:在相同条件下与同浓度的盐酸比较与金属反应的速率思考1:写出乙酸与Na、NaOH、Na2CO3反应的化学方程式。思考2:可以用几种方法证明乙酸是弱酸?CH3CH2OHC6H5OHCH3COOH增强中性比碳酸弱比碳酸强能能能能能不能不能能能,不产
生CO2醇、酚、羧酸中羟基的比较【知识归纳】 1、化合物 跟足量的下列哪种物质的溶液反应可得到一钠盐C7H5O3Na( )A NaOH B Na2CO3
C NaHCO3 D NaCl C【知识应用】2.确定乙酸是弱酸的依据是( )
A.乙酸可以和乙醇发生酯化反应
B.乙酸钠的水溶液显碱性
C.乙酸能使石蕊试液变红
D.Na2CO3中加入乙酸产生CO2
B3、请用一种试剂鉴别下面三种有机物?乙醇、乙醛、乙酸新制Cu(OH)2悬浊液碎瓷片
乙醇 3mL
浓硫酸 2mL
乙酸 2mL
饱和的Na2CO3溶液(2)乙酸的酯化反应(防止暴沸)反应后饱和Na2CO3溶液上层有什么现象?饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。定义:酸和醇起作用,生成酯和水的反应。
本质:酸脱羟基、醇脱羟基氢。 【知识回顾】1. 试管倾斜加热的目的是什么?
2.浓硫酸的作用是什么?
3.得到的反应产物是否纯净?主要杂质有哪些?
4.饱和Na2CO3溶液有什么作用?
5. 为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?催化剂,吸水剂不纯净;乙酸、乙醇① 中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味. ② 溶解乙醇。
③ 冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。防止受热不匀发生倒吸增大受热面积【探究】乙酸乙酯的酯化过程 ——酯化反应的脱水方式可能一可能二同位素示踪法酯化反应:酸和醇起作用,生成酯和水的反应。
酯化反应的本质:酸脱羟基、醇脱羟基氢。 实验验证C5、 若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )A 1种 B 2种 C 3 种 D 4种生成物中水的相对分子质量为 。204、 酯化反应属于( ).
A.中和反应 B.不可逆反应
C.离子反应 D.取代反应D【知识应用】【知识迁移】写出下列酸和醇的酯化反应C2H5O—NO2 + H2OCH3COOCH3 + H2O硝酸乙酯乙酸甲酯足量+ 2H2O 二乙酸乙二酯环乙二酸乙二酯【达标测试】1.下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是( )
A.金属钠 B.溴水
C.碳酸钠溶液 D.紫色石蕊试液C D2.除去乙酸乙酯中含有的乙酸,最好的处理和操作是( )
A.蒸馏 B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液 D.用过量氢氧化钠溶液洗涤后分液3.下列物质中,不能与乙醇发生酯化反应的是( )
A.乙醛 B.硝酸 C.苯甲酸 D.硫酸 CA4.关于乙酸的下列说法中不正确的是 ( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸D练 习8.用30g乙酸和46g乙醇反应,如果实际产率是理论产率的85%,则可得到的乙酸乙酯的质量是( )
A.37.4g B.44g
C.74.8g D.88g解: 60 46 88 30g 46g Xg求得: X = 44g实际产量 = 44g x 85% = 37.4g答案: 选 AA新课标人教版选修五有机化学基础第三章烃的含氧衍生物江苏省淮安中学 张正飞
2019年2月28日星期四第三节 羧酸 酯
第二课时1.下列物质中的溴原子在适当条件下都能被羟基所取代,所得产物能跟NaHCO3溶液反应的是( )
A. B. C. D.COHOHOHOH2.胆固醇是人体必需的生物活性物质,分子式为C25H45O,一种胆固醇酯是液晶材料,分子式为C32H49O2,合成这种胆固醇酯的酸是( )
A. C6H13COOH
B. C6H5COOH
C. C7H15COOH
D. C6H5CH2COOHBC25H45O + 酸 → C32H49O2 + H2O二、羧酸1、定义:分子里烃基跟羧基直接相连的有机物。丙酸甲酸苯甲酸乙二酸复习回忆2、结构①一元羧酸通式:R—COOH
②饱和一元羧酸的通式: CnH2n+1COOH
或CnH2nO2
③多元羧酸中含有多个羧基。3、化学性质(1)酸性(2)酯化反应三、三类重要的羧酸1、甲酸——俗称蚁酸结构特点:既有羧基又有醛基化学性质醛基羧基氧化反应(如银镜反应)酸性,酯化反应2、乙二酸——俗称草酸+ 2H2O3、高级脂肪酸(1)酸性(2)酯化反应(3)油酸加成 1mol有机物
最多能消耗下列各物质多少 mol?(1) Na(2) NaOH(3) NaHCO3练习四、酯的概念、命名和通式1.概念:酸跟醇起反应脱水后生成的一类化合物。
练习:写出硝酸和乙醇,苯甲酸和乙醇反应的化学方程式CH3CH2OH+HONO2→CH3CH2ONO2+H2O
硝酸乙酯说出下列化合物的名称:(1)CH3COOCH2CH3
(2)HCOOCH2CH3
(3)CH3CH2O—NO22.酯的命名——“某酸某酯” 3.酯的通式 饱和一元羧酸和饱和一元醇生成的酯
(1)一般通式:
(2)结构通式:
(3)组成通式:CnH2nO2 二、酯的结构、性质及用途1.酯的物理性质
①低级酯是具有芳香气味的液体。
②密度比水小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。 【实验探究】请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶中,以及不同温度下的水解速率。 (1)酯的水解反应在酸性条件好,还是碱性条件好?
(2)酯化反应H2SO4和NaOH哪种作催化剂好?
(3)酯为什么在中性条件下难水解,而在酸、碱性条件下易水解?(碱性)(浓H2SO4)2.酯+水 酸+醇
CH3COOCH2CH3+H2O CH3COOH+CH3CH2OH
CH3COOH + NaOH CH3COONa + H2O酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的【思考与交流】乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?根据化学平衡原理,提高乙酸乙醋产率措施有:由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率;
使用过量的乙醇,可提高乙酸转化为乙酸乙酯产率。
使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。1.酯在下列哪种环境中水解程度最大
A.水 B.稀硫酸
C.浓硫酸 D.碱溶液2.某有机物X能发生水解反应,水解产物为Y和Z。同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是
A.乙酸丙酯 B.甲酸乙酯
C.乙酸甲酯 D.乙酸乙酯3.对有机物
的叙述不正确的是
A.常温下能与Na2CO3反应放出CO2
B.在碱性条件下水解,0.5mol该有机物完全反应消耗4mol NaOH
C.与稀H2SO4共热生成两种有机物
D.该物质的化学式为C14H10O9小结2:几种衍生物之间的关系例2、一环酯化合物,结构简式如下:试推断:
1.该环酯化合物在酸性条件下水解的产物是什么?
写出其结构简式;
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应? 2、烧鱼时,又加酒又加醋,鱼的味道就变得 无腥、香醇、特别鲜美,其原因是 ( )
A.有盐类物质生成 B.有酸类物质生成
C.有醇类物质生成 D.有酯类物质生成1、可以说明乙酸是弱酸的事实是( ) A.乙酸能与水以任意比混溶
B.乙酸能与碳酸钠反应,产生二氧化碳 C.1mol/L的乙酸钠溶液的PH值约为9
D.1mol/L的乙酸水溶液能使紫色石蕊试液变红课堂练习3.写出能发生银镜反应的属于不同类别的物质的结构简式各一种.酯化反应与酯水解反应的比较
