蛋白质和核酸[上学期]
图片预览






文档简介
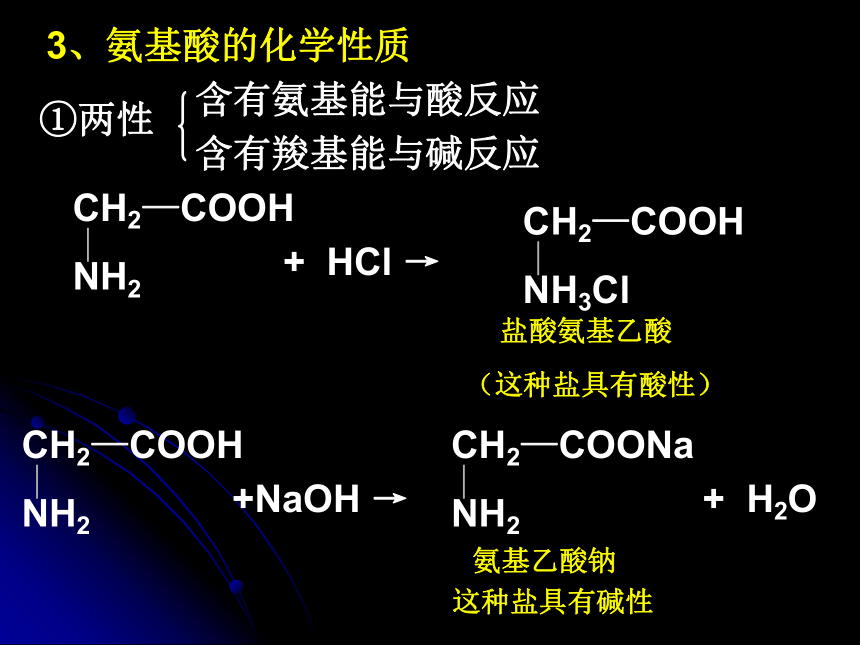
课件17张PPT。第四章 第三节蛋白质和核酸自然界中的蛋白质动物的肌肉、皮肤、血液、乳汁、毛、发、蹄、角等含蛋白质较多植物的各种器官,尤其是种子含蛋白质最多(例如麦粒中含18%)酶、蚕丝、激素、血红蛋白、细菌、病毒、抗体、阿胶中也含有蛋白质一切重要的生命现象和生理机能都与蛋白质密切相关氨基酸是组成蛋白质的基本结构单元一、氨基酸的结构与性质 1、定义从结构上说,氨基酸是羧酸分子里烃基上的氢原子被氨基取代的化合物2、α-氨基酸的结构简式可表示为分子结构中含有两种官能团即:氨基和羧基几种重要的氨基酸(也叫甘氨酸)是最简单的氨基酸(也叫丙氨酸)(也叫苯丙氨酸)α-氨基苯丙酸α-氨基丙酸氨基乙酸3、氨基酸的化学性质①两性含有氨基能与酸反应含有羧基能与碱反应盐酸氨基乙酸(这种盐具有酸性)氨基乙酸钠这种盐具有碱性②成肽反应二、蛋白质的结构和性质1、蛋白质的组成(1)蛋白质是由C、H、O、N、S等元素组成(2)蛋白质的相对分子质量很大,从几万到几千万,是天然高分子化合物(3)天然蛋白质的结构复杂,种类繁多,但水解的最终产物都是α-氨基酸2、蛋白质的结构任何一种蛋白质分子在天然状态下均具有独特而稳定的结构,这是蛋白质分子结构中最显著的特征蛋白质的结构很复杂。一个蛋白质分子可以含有一条或多条肽链,肽链中有很多肽键,一个肽键中的氧原子与另一个肽锓中的氨基的氢原子通过氢键连接,形成类似于螺旋状的结构,最后形成具有三维空间结构的蛋白质分子根据X射线法直接测定蛋白质结构而得到的计算机图象,展示了蛋白质复杂的折叠三维精细结构3、蛋白质的性质(1)蛋白质具有胶体的性质有些蛋白质能溶于水,由于蛋白质分子直径相对很大。已达到胶体微粒的大小,故蛋白质溶液能发生丁达尔效应(2)两性蛋白质的结构含有—NH2和—COOH,故有两性,它能分别与酸、碱反应,生成盐(3)水解反应在酸、碱或酶的作用下,蛋白质能发生水解反应,最终产物是氨基酸(4)盐析在有沉淀的试管中加入蒸馏水,试管中的沉淀能否溶解?现象:有沉淀生成现象:沉淀消失加入浓的无机轻金属盐(如硫酸铵、硫酸钠、氯化钠等),可以降低蛋白质的溶解度,从而析出蛋白质,这种作用称为盐析。①盐析的特征可逆②盐析的用途分离提纯蛋白质③盐析的过程是物理变化(5)变性[演示实验]在两支试管中各加入鸡蛋清溶液3mL,将一支试管加热,试管中有无沉淀产生?在另一支试管中加入2滴质量分数为1%的醋酸铅溶液,试管中有无沉淀产生?在有沉淀的试管中加入蒸馏水,两支试管中的沉淀能否溶解?观察现象。现象:出现沉淀且沉淀不消失当加入醋酸铅等重金属盐时,就会使蛋白质失去可溶性,同时也失去了生理活性,这种现象叫变性。由实验可以看出,加热也可以引起蛋白质的变性。在某些物理因素或化学因素的影响下,蛋白质的理化性质和生理功能发生改变的现象,称为蛋白质的变性。物理因素包括:加热、加压、搅拌、振荡、紫外线照射、超声波等;化学
因素包括:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等。①由蛋白质变性引起的蛋白质凝结是不可逆的,是化学变化②蛋白质变性凝结后丧失可溶性,还失去生理活性(6)颜色反应[演示实验] 在盛有2mL鸡蛋清溶液的试管中,滴入数滴浓硝酸,微热,观察现象。现象:开始有白色沉淀,加热沉淀变黄色。含有苯基的蛋白质和浓HNO3作用显黄色,称为“黄蛋白”反应,用于鉴别蛋白质三、酶1、酶的涵义酶是具有生物活性,对于许多有机化学反应和生物体内进行的复杂化学反应具有很强催化作用的蛋白质。2、酶的用途淀粉酶应用于食品、发酵、纺织、制药等工业;蛋白酶用于医药、制革等工业;脂肪酶用于使脂肪水解、羊毛脱脂等。酶还可用于疾病的诊断3、酶的催化作用的特点(1)条件温和、不需加热。在接近体温和接近中性的条件下,酶就可以起作用。在 30 ~ 500C之间酶的活性最强,超过适宜的温度时,酶将逐渐失去活性。(2)具有高度的专一性。如蛋白酶只能催化蛋白质的水解反应;淀粉酶只对淀粉水解起催化作用,如同一把钥匙开一把锁一样。(3)具有高效催化作用。酶催化的化学反应速率,比普通催化剂高107~1013倍。四、核酸核酸是含磷生物高分子化合物,分为脱氧核糖核酸(DNA)和核糖核酸(RNA),DNA是生物体遗传信息的载体,蛋白质合成的模板;RNA参与生物体内蛋白质的合成
因素包括:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等。①由蛋白质变性引起的蛋白质凝结是不可逆的,是化学变化②蛋白质变性凝结后丧失可溶性,还失去生理活性(6)颜色反应[演示实验] 在盛有2mL鸡蛋清溶液的试管中,滴入数滴浓硝酸,微热,观察现象。现象:开始有白色沉淀,加热沉淀变黄色。含有苯基的蛋白质和浓HNO3作用显黄色,称为“黄蛋白”反应,用于鉴别蛋白质三、酶1、酶的涵义酶是具有生物活性,对于许多有机化学反应和生物体内进行的复杂化学反应具有很强催化作用的蛋白质。2、酶的用途淀粉酶应用于食品、发酵、纺织、制药等工业;蛋白酶用于医药、制革等工业;脂肪酶用于使脂肪水解、羊毛脱脂等。酶还可用于疾病的诊断3、酶的催化作用的特点(1)条件温和、不需加热。在接近体温和接近中性的条件下,酶就可以起作用。在 30 ~ 500C之间酶的活性最强,超过适宜的温度时,酶将逐渐失去活性。(2)具有高度的专一性。如蛋白酶只能催化蛋白质的水解反应;淀粉酶只对淀粉水解起催化作用,如同一把钥匙开一把锁一样。(3)具有高效催化作用。酶催化的化学反应速率,比普通催化剂高107~1013倍。四、核酸核酸是含磷生物高分子化合物,分为脱氧核糖核酸(DNA)和核糖核酸(RNA),DNA是生物体遗传信息的载体,蛋白质合成的模板;RNA参与生物体内蛋白质的合成
