原子晶体[下学期]
图片预览



文档简介
课件18张PPT。原 子 晶 体 CO2 SiO2 C Si S P熔点/ ℃3550 1410 120 590 -56.2 17231、二氧化碳与二氧化硅都是酸性氧化物,碳和硅都是第
ⅣA元素,二氧化碳是分子晶体,二氧化硅也是吗?2、S 、P 单质在固态是是分子晶体, C 、Si 单质也是分子
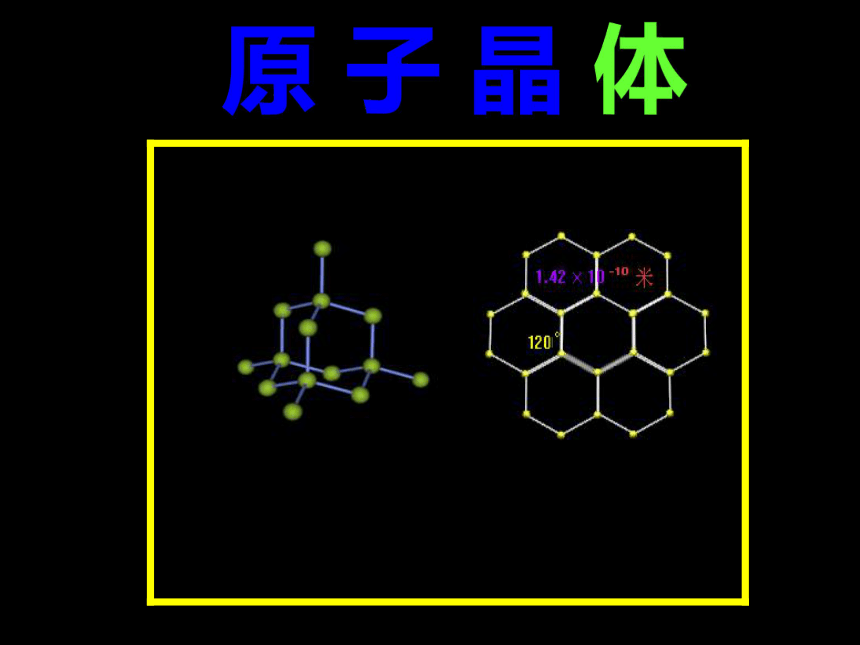
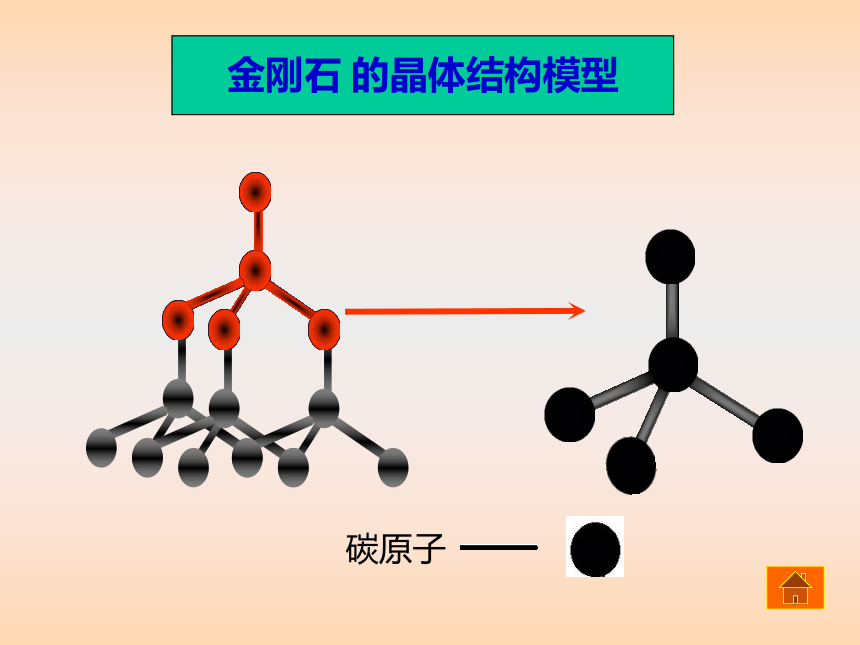
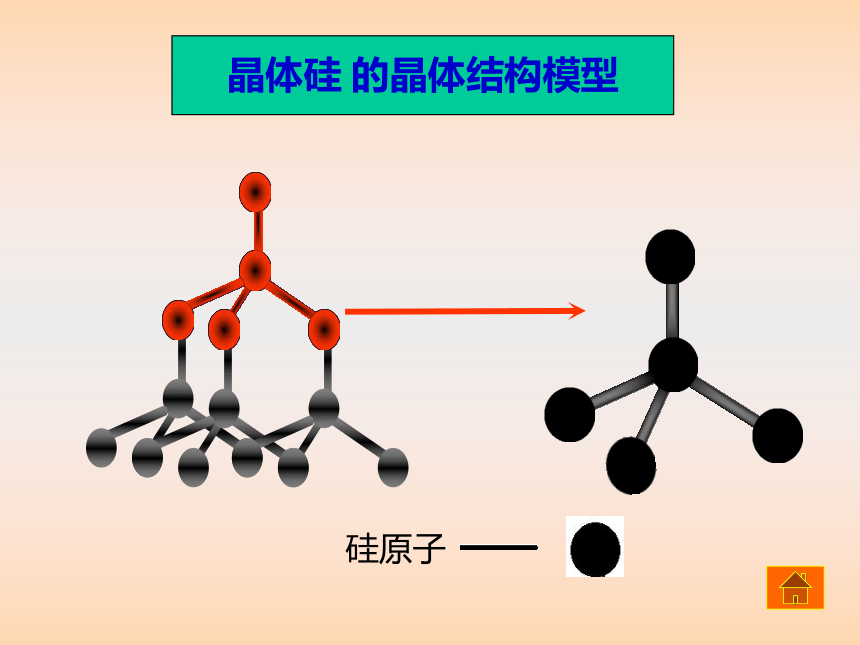
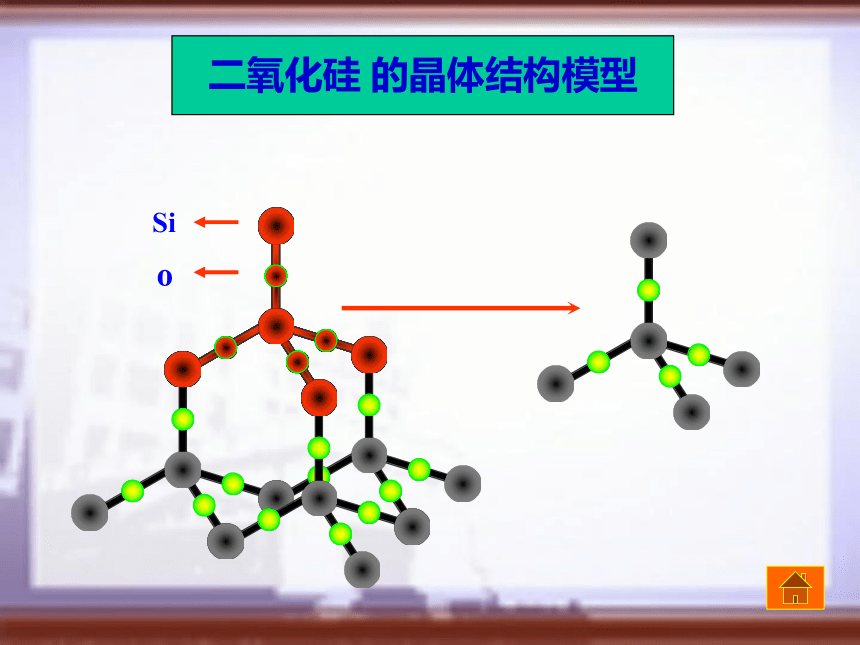
晶体吗?问题一、原子晶体原子间通过共价键相结合而形成空间网状结构的晶体 二、原子晶体的特点 1、熔沸点很高,硬度很大,难溶于一般溶剂 三、哪些物质属于原子晶体 金刚石、单晶硅、碳化硅、二氧化硅等 2、共价键的键能与半径有关,半径越大,键能越小。 C—C > C– Si >Si—Si 一、原子晶体的空间结构金刚石 的晶体结构模型碳原子晶体硅 的晶体结构模型硅原子Sio二氧化硅 的晶体结构模型二、原子晶体结构的计算(二)、晶体中距离最近的微粒数的计算: 1、在金刚石的网状结构中, 含有由共价键形成的碳原子环, 其中最小的环上有______(填数字)个碳原子,每个碳原子上的任意两个C─C键的夹角都是________ (填角度) 6109°28' 2.分析石墨结构中碳原子数与碳碳键数目比。 故正六边形中的碳碳键数为6×1/2=3(三).晶体中化学键数目的计算解析:
我们可以先选取一个正六边形此结构中的碳原子数为6一个碳原子被三个六元碳环共用,正六边形中的碳原子数为6×1/3=2。六边形中的任一条边(即碳碳键)
均被2个正六边形共用,所以碳原子数与碳碳键数目比为2:3。3.金刚石结构中,一个碳原子与 个碳原子成键,
则每个碳原子实际形成的化学键为 个;
a mol金刚石中,碳碳键数为 mol。422a石墨石墨为什么很软?
石墨的熔沸点为什么很高?石墨为层状结构,各层之间是范德华力结合,容易滑动,所以石墨很软。
石墨各层均为平面网状结构,碳原子之间存在很强的共价键,故熔沸点很高。
所以,石墨称为混合型晶体。—混合型晶体本节知识归纳晶体类型
离子晶体
分子晶体
原子晶体离子键
范德华力
共价键离子
分子
原子较高
较低
很高NaCl、CsCl
干冰
金刚石微粒结合力熔沸点典型实例一、三种晶体的比较二、晶体类型的判断晶体类型的判断从组成上判断(仅限于中学范围):
有无阴离子?(有:离子晶体)
是否属于“四种原子晶体”?
以上皆否定,则多数是分子晶体。
从性质上判断:
熔沸点和硬度;(高:原子晶体;中:离子晶体;低:分子晶体)
熔融状态的导电性。(导电:离子晶体) 根本依据: 构成晶体的微粒 微粒间的相互作用判断经验小结:课堂练习题下列不存在化学键的晶体是:
A.硝酸钾 B.干冰 C.石墨 D.固体氩
常温常压下的分子晶体是:
A.碘 B.水 C. 硫酸铵 D.干冰
晶体中的一个微粒周围有6个微粒,这种晶体是:
A.金刚石 B.石墨 C.干冰 D.氯化钠DAD开拓思考题仔细观察左边的示意图后,回答下列问题:
金刚石与石墨的熔点均很高,那么二者熔点是否相同?为什么?若不相同,哪种更高一些?石墨熔点更高. 键长越短键能越大熔点更高!金刚石的晶体结构石墨的晶体结构
ⅣA元素,二氧化碳是分子晶体,二氧化硅也是吗?2、S 、P 单质在固态是是分子晶体, C 、Si 单质也是分子
晶体吗?问题一、原子晶体原子间通过共价键相结合而形成空间网状结构的晶体 二、原子晶体的特点 1、熔沸点很高,硬度很大,难溶于一般溶剂 三、哪些物质属于原子晶体 金刚石、单晶硅、碳化硅、二氧化硅等 2、共价键的键能与半径有关,半径越大,键能越小。 C—C > C– Si >Si—Si 一、原子晶体的空间结构金刚石 的晶体结构模型碳原子晶体硅 的晶体结构模型硅原子Sio二氧化硅 的晶体结构模型二、原子晶体结构的计算(二)、晶体中距离最近的微粒数的计算: 1、在金刚石的网状结构中, 含有由共价键形成的碳原子环, 其中最小的环上有______(填数字)个碳原子,每个碳原子上的任意两个C─C键的夹角都是________ (填角度) 6109°28' 2.分析石墨结构中碳原子数与碳碳键数目比。 故正六边形中的碳碳键数为6×1/2=3(三).晶体中化学键数目的计算解析:
我们可以先选取一个正六边形此结构中的碳原子数为6一个碳原子被三个六元碳环共用,正六边形中的碳原子数为6×1/3=2。六边形中的任一条边(即碳碳键)
均被2个正六边形共用,所以碳原子数与碳碳键数目比为2:3。3.金刚石结构中,一个碳原子与 个碳原子成键,
则每个碳原子实际形成的化学键为 个;
a mol金刚石中,碳碳键数为 mol。422a石墨石墨为什么很软?
石墨的熔沸点为什么很高?石墨为层状结构,各层之间是范德华力结合,容易滑动,所以石墨很软。
石墨各层均为平面网状结构,碳原子之间存在很强的共价键,故熔沸点很高。
所以,石墨称为混合型晶体。—混合型晶体本节知识归纳晶体类型
离子晶体
分子晶体
原子晶体离子键
范德华力
共价键离子
分子
原子较高
较低
很高NaCl、CsCl
干冰
金刚石微粒结合力熔沸点典型实例一、三种晶体的比较二、晶体类型的判断晶体类型的判断从组成上判断(仅限于中学范围):
有无阴离子?(有:离子晶体)
是否属于“四种原子晶体”?
以上皆否定,则多数是分子晶体。
从性质上判断:
熔沸点和硬度;(高:原子晶体;中:离子晶体;低:分子晶体)
熔融状态的导电性。(导电:离子晶体) 根本依据: 构成晶体的微粒 微粒间的相互作用判断经验小结:课堂练习题下列不存在化学键的晶体是:
A.硝酸钾 B.干冰 C.石墨 D.固体氩
常温常压下的分子晶体是:
A.碘 B.水 C. 硫酸铵 D.干冰
晶体中的一个微粒周围有6个微粒,这种晶体是:
A.金刚石 B.石墨 C.干冰 D.氯化钠DAD开拓思考题仔细观察左边的示意图后,回答下列问题:
金刚石与石墨的熔点均很高,那么二者熔点是否相同?为什么?若不相同,哪种更高一些?石墨熔点更高. 键长越短键能越大熔点更高!金刚石的晶体结构石墨的晶体结构
