原子核的组成(共22张PPT)
文档属性
| 名称 | 原子核的组成(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2018-11-25 00:00:00 | ||
图片预览





文档简介
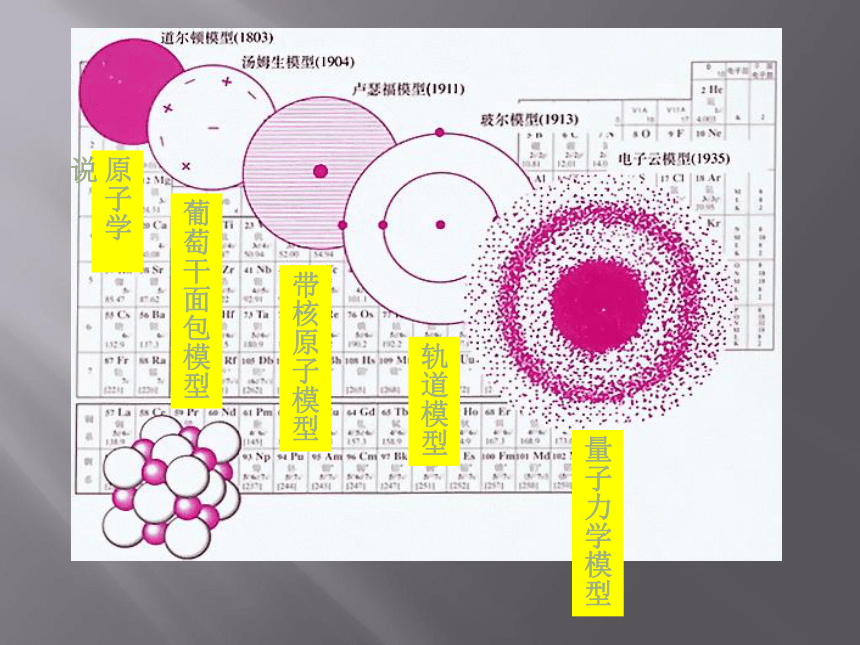
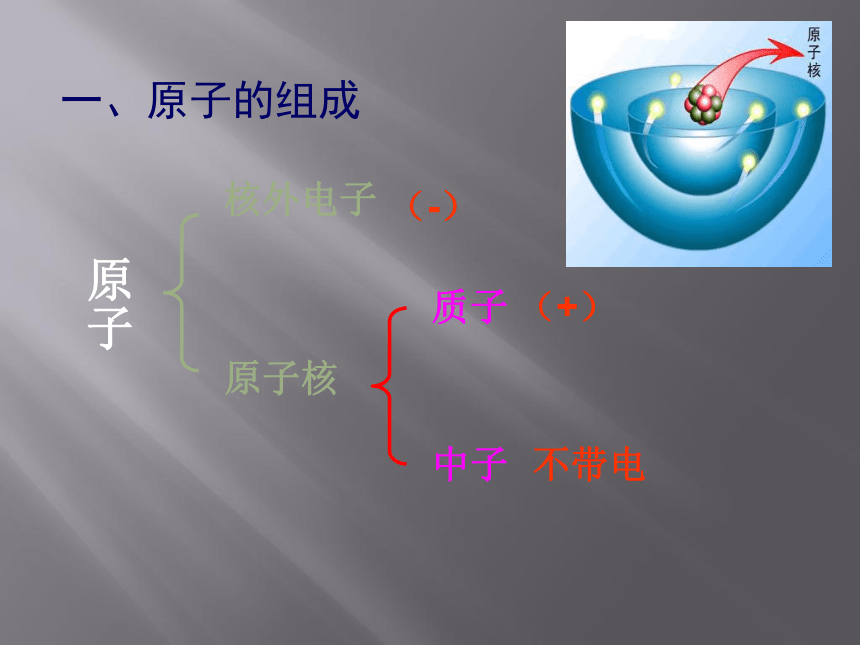
课件22张PPT。原子核的组成原子学说葡萄干面包模型带核原子模型轨道模型量子力学模型 原子是由原子核和核外电子所构成,那原子核可不可以再分呢?大多数原子的原子核由质子和中子构成原子核外电子原子核质子中子(-)(+)不带电一、原子的组成 质子 中子 电子
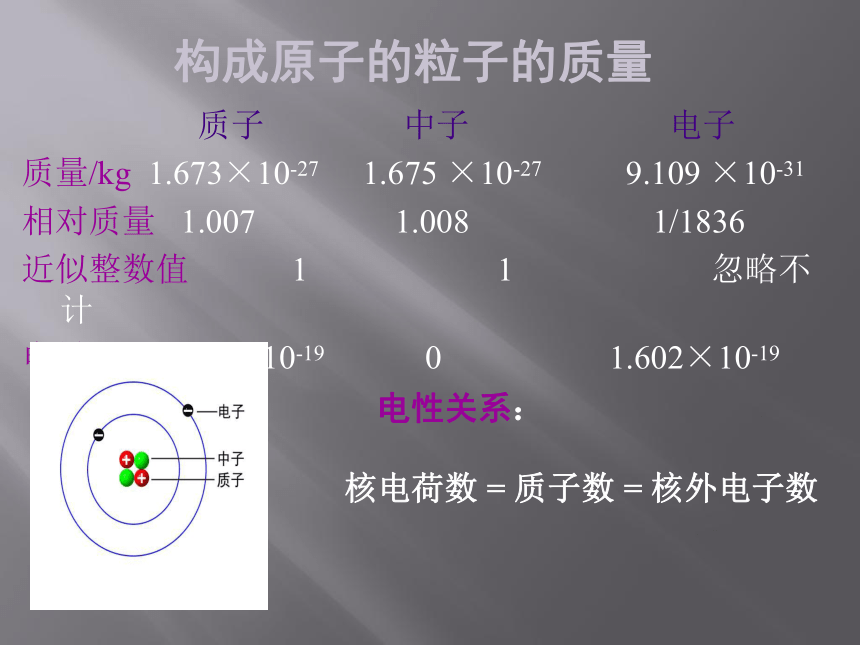
质量/kg 1.673×10-27 1.675 ×10-27 9.109 ×10-31
相对质量 1.007 1.008 1/1836
近似整数值 1 1 忽略不计
电量/C 1.602×10-19 0 1.602×10-19 构成原子的粒子的质量 电性关系:
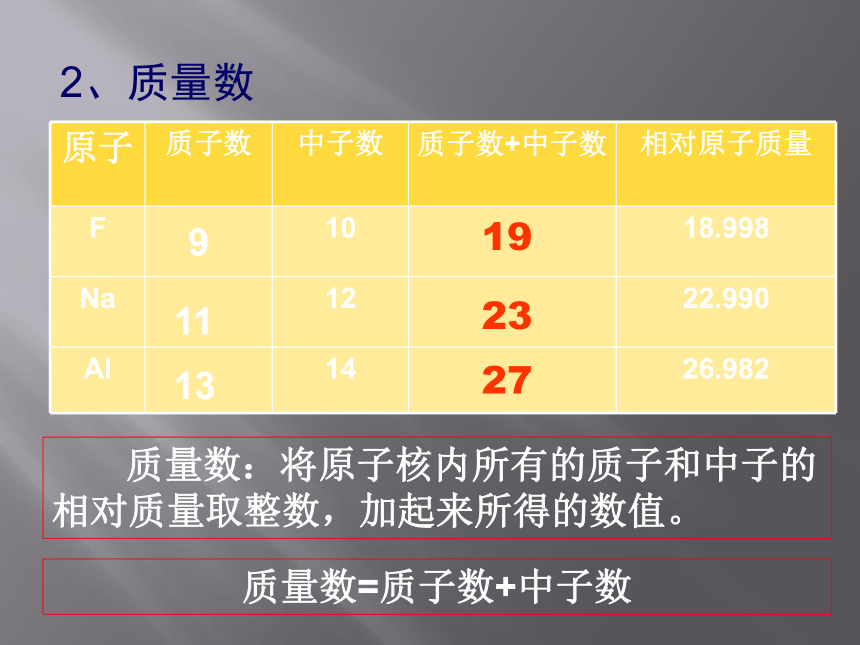
核电荷数 = 质子数 = 核外电子数质子数=核电荷数=原子序数=原子的核外电子数我们又知道原子显电中性,从中可以得到什么结论?1、微粒间的数量关系192327 质量数:将原子核内所有的质子和中子的相对质量取整数,加起来所得的数值。质量数=质子数+中子数911132、质量数X表示元素符号Z表示原子的质子数A表示原子的质量数3、原子的表示表示质量数为4,原子核内有2个质子和2中子的氦原子表示质量数为12,原子核内有6个质子和6个中子的碳原子。 表示质量数为14,原子核内有6个质子和8个中子的碳原子。 【练习】请表示出下列原子
核内有7个中子的氮原子 质量数为32的硫原子
核内有16个中子的磷原子 质量数为24的镁原子a——代表质量数
b——代表质子数
c——代表离子所带电荷数
d——代表化合价
e ——代表一个Xe分子所含
e个X原子a、b、c、d、e各代表什么?X表示元素符号【复习回顾】 微粒 核电荷数 质子数 中子数 电子数 质量数
(1)
(2)
(3)
(4)
(5)【练习】含有 个电子z-m含有 个电子z+m19191917171919191717202121181817181919183535404039 具有相同核电荷数(质子数)的同类原子的总称元素② 决定元素种类的因素:核电荷数(质子数)① 同类包括质子数相同的各种不同原子、以及各种状况下的原子或者离子(包括游离态和化合态)如 H H+ H- 都表示氢元素二、元素、核素与同位素核素 具有一定质子数和一定中子数的一种原子称为一种核素② 决定因素:质子数和中子数① 不同的核素可能质子数相同、或中子数相同、或质量数相同,或者三者都不同 如质子数相同,质量数不同(中子数不同)的核素,则互为同位素。同位素氕 氢 (H) 中子数为 0
氘 重氢(D) 中子数为 1
氚 超重氢(T) 中子数为 2元素:具有相同质子数的一类原子的总称。 核素:具有一定质子数和一定中子数的一种原子。 同位素:同种元素的不同种核素间的互称。 1、元素、核素和同位素的关系 在天然元素中,多数元素含有多种核素,少数元素只含有一种核素(例如Na、K等)。某种元素跟核素和同位素的关系:同素异形体:有同种元素形成的不同单质。如:金刚石和石墨、红磷和白磷、氧气和臭氧。练习:原子、元素、核素、同位素、同素异形体等都属于重要的化学基本概念,原子的构成属于重要的化学基本理论。下列九中化学符号:
H2 D2 T 1H 1H+ T+ O2 O3 35Cl-
共有———— 种元素,—————种核素,———— 和 ———
互为同位素,———————— 和 ———————互为同素异形体。
22O2O3T1H【扩展】同素异形体2、同位素的性质(1)同位素的质量数不同,物理性质不同(2)同位素的核外电子数相同,化学性质相同3、同位素的应用a、考古学b、医学c、国防d、农业 C :612C、613C、614C
614C每隔5568年它的质量就会减少一半,考古学家根据生物体内614C的含量,就可判断其生活的年代.a、考古学b、医学中用于显像、诊断、治疗、消毒等;H :11H 、 12H(D) 、 13H(T)
重氢和超重氢是制造氢弹的原料
U: 92234U 、 92235 U 、 92238U
铀-235 制原子弹 c、国防氢弹实验d、农业上的辐射育种技术,提高了农产品的质量和数量; 利用同位素示踪技术,可用于检测并确定植物的最佳肥料吸入量和农药吸入量。昆虫不育技术基于用γ辐射使昆虫不育(丧失繁衍能力)已成功地用于铲除损害谷物的昆虫种类,而对于人类健康和环境无任何副作用。至于动物生产,同位素常常用于监测和改进牛的健康。对于食品保藏,辐射已成为一种很有效的手段。食品辐照可控制微生物引起的食品腐败和食源性疾病的传播。
质量/kg 1.673×10-27 1.675 ×10-27 9.109 ×10-31
相对质量 1.007 1.008 1/1836
近似整数值 1 1 忽略不计
电量/C 1.602×10-19 0 1.602×10-19 构成原子的粒子的质量 电性关系:
核电荷数 = 质子数 = 核外电子数质子数=核电荷数=原子序数=原子的核外电子数我们又知道原子显电中性,从中可以得到什么结论?1、微粒间的数量关系192327 质量数:将原子核内所有的质子和中子的相对质量取整数,加起来所得的数值。质量数=质子数+中子数911132、质量数X表示元素符号Z表示原子的质子数A表示原子的质量数3、原子的表示表示质量数为4,原子核内有2个质子和2中子的氦原子表示质量数为12,原子核内有6个质子和6个中子的碳原子。 表示质量数为14,原子核内有6个质子和8个中子的碳原子。 【练习】请表示出下列原子
核内有7个中子的氮原子 质量数为32的硫原子
核内有16个中子的磷原子 质量数为24的镁原子a——代表质量数
b——代表质子数
c——代表离子所带电荷数
d——代表化合价
e ——代表一个Xe分子所含
e个X原子a、b、c、d、e各代表什么?X表示元素符号【复习回顾】 微粒 核电荷数 质子数 中子数 电子数 质量数
(1)
(2)
(3)
(4)
(5)【练习】含有 个电子z-m含有 个电子z+m19191917171919191717202121181817181919183535404039 具有相同核电荷数(质子数)的同类原子的总称元素② 决定元素种类的因素:核电荷数(质子数)① 同类包括质子数相同的各种不同原子、以及各种状况下的原子或者离子(包括游离态和化合态)如 H H+ H- 都表示氢元素二、元素、核素与同位素核素 具有一定质子数和一定中子数的一种原子称为一种核素② 决定因素:质子数和中子数① 不同的核素可能质子数相同、或中子数相同、或质量数相同,或者三者都不同 如质子数相同,质量数不同(中子数不同)的核素,则互为同位素。同位素氕 氢 (H) 中子数为 0
氘 重氢(D) 中子数为 1
氚 超重氢(T) 中子数为 2元素:具有相同质子数的一类原子的总称。 核素:具有一定质子数和一定中子数的一种原子。 同位素:同种元素的不同种核素间的互称。 1、元素、核素和同位素的关系 在天然元素中,多数元素含有多种核素,少数元素只含有一种核素(例如Na、K等)。某种元素跟核素和同位素的关系:同素异形体:有同种元素形成的不同单质。如:金刚石和石墨、红磷和白磷、氧气和臭氧。练习:原子、元素、核素、同位素、同素异形体等都属于重要的化学基本概念,原子的构成属于重要的化学基本理论。下列九中化学符号:
H2 D2 T 1H 1H+ T+ O2 O3 35Cl-
共有———— 种元素,—————种核素,———— 和 ———
互为同位素,———————— 和 ———————互为同素异形体。
22O2O3T1H【扩展】同素异形体2、同位素的性质(1)同位素的质量数不同,物理性质不同(2)同位素的核外电子数相同,化学性质相同3、同位素的应用a、考古学b、医学c、国防d、农业 C :612C、613C、614C
614C每隔5568年它的质量就会减少一半,考古学家根据生物体内614C的含量,就可判断其生活的年代.a、考古学b、医学中用于显像、诊断、治疗、消毒等;H :11H 、 12H(D) 、 13H(T)
重氢和超重氢是制造氢弹的原料
U: 92234U 、 92235 U 、 92238U
铀-235 制原子弹 c、国防氢弹实验d、农业上的辐射育种技术,提高了农产品的质量和数量; 利用同位素示踪技术,可用于检测并确定植物的最佳肥料吸入量和农药吸入量。昆虫不育技术基于用γ辐射使昆虫不育(丧失繁衍能力)已成功地用于铲除损害谷物的昆虫种类,而对于人类健康和环境无任何副作用。至于动物生产,同位素常常用于监测和改进牛的健康。对于食品保藏,辐射已成为一种很有效的手段。食品辐照可控制微生物引起的食品腐败和食源性疾病的传播。
