氯气[上学期]
图片预览







文档简介
课件23张PPT。Li(锂)
Na(钠)K (钾)
Rb(铷)
Cs(铯)
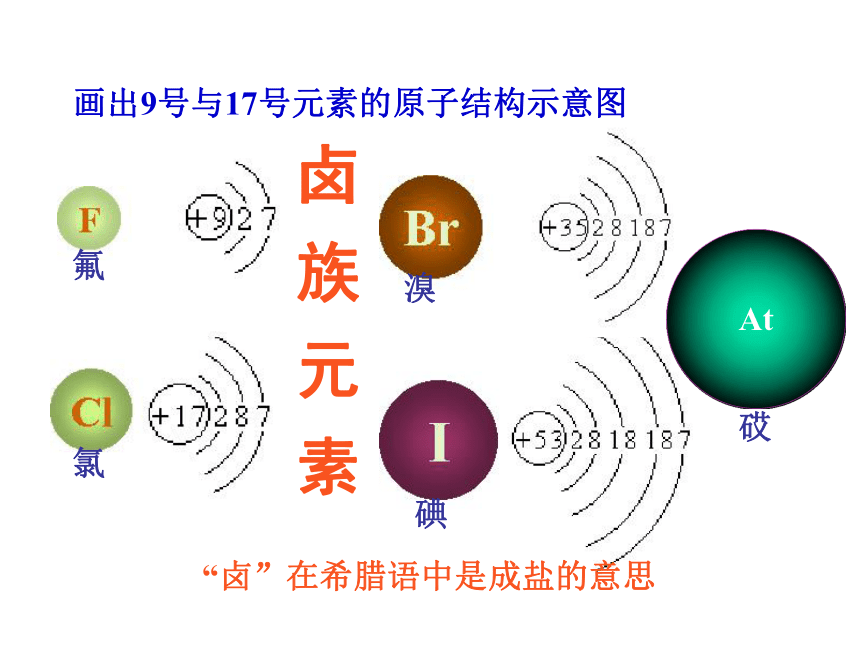
Fr(钫)碱金属元素 画出9号与17号元素的原子结构示意图卤 族 元 素“卤”在希腊语中是成盐的意思 Chapter 4 Halogens
(F、Cl、Br、I、At)
4.1 Chlorine (Cl2) 阅读资料:
瑞典著名的化学家舍勒(the Swedish chemist C.W.Scheele)
自1773年开始致力于研究当时叫黑锰矿的物质,黑锰矿就是
MnO2,舍勒在研究过程中惊奇发现当把MnO2和浓盐酸混合
加热时,很快就产生一种黄绿色的气体,舍勒简直高兴到了
极点,因为当时人们很少看到过有色气体。但很快兴奋变成
了厌恶,这种黄绿色气体源源不断地产生,几乎使舍勒窒息,
肺部极为难受。受科学家职业本能的驱使,舍勒对这种气体
进行观察和研究,发现把鲜艳的花或翠绿的叶子放到其中,
美丽的色泽很快褪去了,将蚱蜢放进去蹦达几下就死去了,
它还能与金属发生化学反应。
这种元素被命名为Chlorine,这个名称来自希腊文,
有“绿色的”意思。我国早年的译文将其译为“绿气”,后改
为氯气。
从资料中分析可得到Cl2哪些方面的信息? (Ⅰ)Cl2的物理性质(1)黄绿色气体 (greenish-yellow gas) (2)有刺激性气味、有毒(3)密度比空气大(4)易液化(5)能溶于水(常温常压下,1:2)(氯气是一种毒性气体,有很强的刺激性,主要是对
上呼吸道粘膜造成有害影响。空气中的氯气最高允许
含量为0.001mg/L,超过这含量就会引起中毒。)闻Ⅰ. Cl2的性质(1)氯原子的原子结构有什么特点?是否稳定?在反应中易发生怎样的变化?
(2)这一结构特点决定了氯气怎样的化学性质?
(3)氯元素在自然界以何种形式存在?
(Ⅱ) Cl2的化学性质强氧化性化合态在反应中很容易得到1个电子 1、 Cl2和金属的反应钠在氯气中燃烧,发出黄色火焰,产生白烟红热的铜丝在Cl2中剧烈燃烧,产生棕黄色烟氯气具有强氧化性,在加热或点燃的条件下,与大多数金属直接化合,且把变价金属氧化为高价。 2、 Cl2和非金属的反应H2 + Cl2 === 2HCl点燃或光照a现象:氢气在氯气中安静燃烧,发出苍白色火焰,瓶口呈白雾状白雾——生成的HCl与空气中的水蒸气结合形成
的盐酸(氢氯酸)小液滴。辨析:烟和雾有何区别?b现象:H2、Cl2混合光照——发生爆炸,产生白雾。思:为什么H2在Cl2中能安静燃烧,而在混合后光照会爆炸? Cl2和氢气的反应:1、比较铜在氯气中燃烧与H2在Cl2中燃烧现象的共同点 ?2、从刚才的反应看是否可燃物必须有氧气才能燃烧?
发光、发热、剧烈反应 燃烧不一定要氧气参加,任何发光、发热的剧烈化学反应,都可以叫燃烧。补充: P在Cl2中的燃烧P在Cl2中的燃烧现象:有白色烟雾生成
2P + 3Cl2 = 2PCl3 (l)
2P + 5Cl2 = 2PCl5(s)
PCl5固体小颗粒为烟,
PCl3液体小液滴为雾
形成白烟形成白雾白色烟雾?Cl2+H2O=HCl+HClO (次氯酸) 0 -1 +1化合价降低,得e-化合价升高,失e-Cl2既作氧化剂,又作还原剂,氧化产物:HClO,还原产物:HCl。次氯酸不稳定:2HClO == 2HCl + O2 +1 -2 -1 0光照次氯酸的特性: 漂白性、强氧化性、不稳定性、弱酸性 3、Cl2和水的反应[思考](1)液氯与氯水有何不同?
(2)新制的氯水中有哪些微粒?
(3)新制的氯水与久置的氯水有何不同?
液氯是纯净物,氯水是混合物
关于氯水(Chlorine water):1、氯水的颜色:黄绿色
2、新制氯水中:分子:Cl2、H2O、HClO、 离子有:H+ 、Cl-、ClO- 、OH-
3、主要成分 : Cl2
4、氯水的保存:棕色瓶、避光
5、久置氯水:H2O、H+ 、Cl- (无色) 氯水的化学性质实验结构性质存在用途制备知识小结1)与金属反应(Na、Fe、Cu)
2)与非金属反应(H2、P)
3)与水的反应强氧化性能力小结学会分析:1、下列物质中,属于纯净物的是:( )
A、氯水 B、氯化氢 C、液氯 D、漂粉精学会比较:2、下列说法正确的是:( )
A、Cl-的半径比Cl的半径大 B、Cl2有毒,Cl-也有毒
C、Cl和Cl-的 化学性质一样 D、Cl2和Cl-都是黄绿色BCA再见策划制作:肖亮
2005年11月轻、扇、飘1979年9月7日下午1时55分,温州电化厂液氯工段的工人正在充装作业,一只半吨重的充满液氯的钢瓶突然爆炸。随着震天的巨响,大量液氯气化,形成巨大黄绿色气柱冲天而起,蘑菇状,高达40余米。该工段的厂房全部倒塌,其它液氯钢瓶被引爆或击穿,大量液氯外泄。爆炸中心的一只重达1735kg的液氯钢瓶被气浪掀起,飞越12米的高压线,坠落在30米外的盐库内。
时值东北风,氯气迅速呈60度扇形向西北方扩散,共有32个居民区和6个生产队受到污染。1208人受到氯气危害,779人中毒。本次事故共死亡59人,其中现场死亡18人,另外41人均为氯气中毒死亡(均为重污染区的居民,本厂职工逆风疏散到一高坡上,故无中毒致死者)。 事故惊动了从中央到地方的各级行政和技术人员,组织了专门的指挥部协调救援工作。防化、消防人员用大量喷水抑制逸出氯气的扩散,关闭了所有储槽、管道的阀门。厂区周围人员全部疏散,共有8万人撤离了危险区。
CuCl2溶液的浓度不同,其颜色略有差别。这是因为在CuCl2
溶液中存在着两种复杂的离子—黄色的[CuCl4]2-和蓝色的水合
离子[Cu(H2O)4]2+。在浓CuCl2溶液中,Cl—浓度大,主要以
黄色的[CuCl4]2-离子存在,而蓝色的水合离子较少,因此浓CuCl2
溶呈黄色。在稀CuCl2溶液中,Cl-离子浓度小,Cu2+主要以水
合离子[Cu(H2O)4]2+的形式存在,因此稀CuCl2溶液呈蓝色。
而在中等浓度的CuCl2溶液中,Cu2+以两种复杂离子形式存在
于溶液中,因此CuCl2溶液就呈现出黄色和蓝色的混合色——蓝
绿色。
解释:CuCl2
晶体 CuCl2
浓溶液 CuCl2
稀溶液 纯净的氢气在氯气中燃烧,瞬间只有导管口处的少量氢分子与氯分子化合,产生的少量热能及时散发出去,故可安静燃烧。
而光照条件下混合气中大量的氯分子和氢分子迅速化合,短时间内产生大量的热,无法及时散去,使气体体积急剧膨胀,产生爆炸。爆炸原因分析: 次氯酸不稳定,容易分解放出氧气。当氯水受到日光照射时,次氯酸的分解速率加快。氯气的毒性
? 氯气主要通过呼吸道侵入人体,氯气对上呼吸道粘膜会造成有害的影响,它会溶解在粘膜所含的水分里,生成次氯酸和盐酸,次氯酸使组织受到强烈氧化;盐酸刺激粘膜发生炎性肿胀,使呼吸道粘膜浮肿,大量分泌粘液,造成呼吸困难,所以氯气中毒的明显症状是发生剧烈的咳嗽。症状重时,会发生肺水肿,使循环作用困难而导致死亡。由食道进入人体的氯气会使人恶心、呕吐、胸口疼痛和腹泻等。
Na(钠)K (钾)
Rb(铷)
Cs(铯)
Fr(钫)碱金属元素 画出9号与17号元素的原子结构示意图卤 族 元 素“卤”在希腊语中是成盐的意思 Chapter 4 Halogens
(F、Cl、Br、I、At)
4.1 Chlorine (Cl2) 阅读资料:
瑞典著名的化学家舍勒(the Swedish chemist C.W.Scheele)
自1773年开始致力于研究当时叫黑锰矿的物质,黑锰矿就是
MnO2,舍勒在研究过程中惊奇发现当把MnO2和浓盐酸混合
加热时,很快就产生一种黄绿色的气体,舍勒简直高兴到了
极点,因为当时人们很少看到过有色气体。但很快兴奋变成
了厌恶,这种黄绿色气体源源不断地产生,几乎使舍勒窒息,
肺部极为难受。受科学家职业本能的驱使,舍勒对这种气体
进行观察和研究,发现把鲜艳的花或翠绿的叶子放到其中,
美丽的色泽很快褪去了,将蚱蜢放进去蹦达几下就死去了,
它还能与金属发生化学反应。
这种元素被命名为Chlorine,这个名称来自希腊文,
有“绿色的”意思。我国早年的译文将其译为“绿气”,后改
为氯气。
从资料中分析可得到Cl2哪些方面的信息? (Ⅰ)Cl2的物理性质(1)黄绿色气体 (greenish-yellow gas) (2)有刺激性气味、有毒(3)密度比空气大(4)易液化(5)能溶于水(常温常压下,1:2)(氯气是一种毒性气体,有很强的刺激性,主要是对
上呼吸道粘膜造成有害影响。空气中的氯气最高允许
含量为0.001mg/L,超过这含量就会引起中毒。)闻Ⅰ. Cl2的性质(1)氯原子的原子结构有什么特点?是否稳定?在反应中易发生怎样的变化?
(2)这一结构特点决定了氯气怎样的化学性质?
(3)氯元素在自然界以何种形式存在?
(Ⅱ) Cl2的化学性质强氧化性化合态在反应中很容易得到1个电子 1、 Cl2和金属的反应钠在氯气中燃烧,发出黄色火焰,产生白烟红热的铜丝在Cl2中剧烈燃烧,产生棕黄色烟氯气具有强氧化性,在加热或点燃的条件下,与大多数金属直接化合,且把变价金属氧化为高价。 2、 Cl2和非金属的反应H2 + Cl2 === 2HCl点燃或光照a现象:氢气在氯气中安静燃烧,发出苍白色火焰,瓶口呈白雾状白雾——生成的HCl与空气中的水蒸气结合形成
的盐酸(氢氯酸)小液滴。辨析:烟和雾有何区别?b现象:H2、Cl2混合光照——发生爆炸,产生白雾。思:为什么H2在Cl2中能安静燃烧,而在混合后光照会爆炸? Cl2和氢气的反应:1、比较铜在氯气中燃烧与H2在Cl2中燃烧现象的共同点 ?2、从刚才的反应看是否可燃物必须有氧气才能燃烧?
发光、发热、剧烈反应 燃烧不一定要氧气参加,任何发光、发热的剧烈化学反应,都可以叫燃烧。补充: P在Cl2中的燃烧P在Cl2中的燃烧现象:有白色烟雾生成
2P + 3Cl2 = 2PCl3 (l)
2P + 5Cl2 = 2PCl5(s)
PCl5固体小颗粒为烟,
PCl3液体小液滴为雾
形成白烟形成白雾白色烟雾?Cl2+H2O=HCl+HClO (次氯酸) 0 -1 +1化合价降低,得e-化合价升高,失e-Cl2既作氧化剂,又作还原剂,氧化产物:HClO,还原产物:HCl。次氯酸不稳定:2HClO == 2HCl + O2 +1 -2 -1 0光照次氯酸的特性: 漂白性、强氧化性、不稳定性、弱酸性 3、Cl2和水的反应[思考](1)液氯与氯水有何不同?
(2)新制的氯水中有哪些微粒?
(3)新制的氯水与久置的氯水有何不同?
液氯是纯净物,氯水是混合物
关于氯水(Chlorine water):1、氯水的颜色:黄绿色
2、新制氯水中:分子:Cl2、H2O、HClO、 离子有:H+ 、Cl-、ClO- 、OH-
3、主要成分 : Cl2
4、氯水的保存:棕色瓶、避光
5、久置氯水:H2O、H+ 、Cl- (无色) 氯水的化学性质实验结构性质存在用途制备知识小结1)与金属反应(Na、Fe、Cu)
2)与非金属反应(H2、P)
3)与水的反应强氧化性能力小结学会分析:1、下列物质中,属于纯净物的是:( )
A、氯水 B、氯化氢 C、液氯 D、漂粉精学会比较:2、下列说法正确的是:( )
A、Cl-的半径比Cl的半径大 B、Cl2有毒,Cl-也有毒
C、Cl和Cl-的 化学性质一样 D、Cl2和Cl-都是黄绿色BCA再见策划制作:肖亮
2005年11月轻、扇、飘1979年9月7日下午1时55分,温州电化厂液氯工段的工人正在充装作业,一只半吨重的充满液氯的钢瓶突然爆炸。随着震天的巨响,大量液氯气化,形成巨大黄绿色气柱冲天而起,蘑菇状,高达40余米。该工段的厂房全部倒塌,其它液氯钢瓶被引爆或击穿,大量液氯外泄。爆炸中心的一只重达1735kg的液氯钢瓶被气浪掀起,飞越12米的高压线,坠落在30米外的盐库内。
时值东北风,氯气迅速呈60度扇形向西北方扩散,共有32个居民区和6个生产队受到污染。1208人受到氯气危害,779人中毒。本次事故共死亡59人,其中现场死亡18人,另外41人均为氯气中毒死亡(均为重污染区的居民,本厂职工逆风疏散到一高坡上,故无中毒致死者)。 事故惊动了从中央到地方的各级行政和技术人员,组织了专门的指挥部协调救援工作。防化、消防人员用大量喷水抑制逸出氯气的扩散,关闭了所有储槽、管道的阀门。厂区周围人员全部疏散,共有8万人撤离了危险区。
CuCl2溶液的浓度不同,其颜色略有差别。这是因为在CuCl2
溶液中存在着两种复杂的离子—黄色的[CuCl4]2-和蓝色的水合
离子[Cu(H2O)4]2+。在浓CuCl2溶液中,Cl—浓度大,主要以
黄色的[CuCl4]2-离子存在,而蓝色的水合离子较少,因此浓CuCl2
溶呈黄色。在稀CuCl2溶液中,Cl-离子浓度小,Cu2+主要以水
合离子[Cu(H2O)4]2+的形式存在,因此稀CuCl2溶液呈蓝色。
而在中等浓度的CuCl2溶液中,Cu2+以两种复杂离子形式存在
于溶液中,因此CuCl2溶液就呈现出黄色和蓝色的混合色——蓝
绿色。
解释:CuCl2
晶体 CuCl2
浓溶液 CuCl2
稀溶液 纯净的氢气在氯气中燃烧,瞬间只有导管口处的少量氢分子与氯分子化合,产生的少量热能及时散发出去,故可安静燃烧。
而光照条件下混合气中大量的氯分子和氢分子迅速化合,短时间内产生大量的热,无法及时散去,使气体体积急剧膨胀,产生爆炸。爆炸原因分析: 次氯酸不稳定,容易分解放出氧气。当氯水受到日光照射时,次氯酸的分解速率加快。氯气的毒性
? 氯气主要通过呼吸道侵入人体,氯气对上呼吸道粘膜会造成有害的影响,它会溶解在粘膜所含的水分里,生成次氯酸和盐酸,次氯酸使组织受到强烈氧化;盐酸刺激粘膜发生炎性肿胀,使呼吸道粘膜浮肿,大量分泌粘液,造成呼吸困难,所以氯气中毒的明显症状是发生剧烈的咳嗽。症状重时,会发生肺水肿,使循环作用困难而导致死亡。由食道进入人体的氯气会使人恶心、呕吐、胸口疼痛和腹泻等。
