氨、铵盐、硝酸[上学期]
文档属性
| 名称 | 氨、铵盐、硝酸[上学期] |  | |
| 格式 | rar | ||
| 文件大小 | 607.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-07-26 16:43:00 | ||
图片预览







文档简介
课件23张PPT。1、物理性质1)无色,有刺激性气味,比空气轻。2)易液化3)极易溶于水
(常温下,1体积水能溶解700体积氨)喷泉实验浓度越大,则密度越小2、氨分子的结构分子式: 电子式: 结构式:空间构型:三角锥形键角:107o18′讨论:①结合氨气的喷泉实验,预测其化学性质。
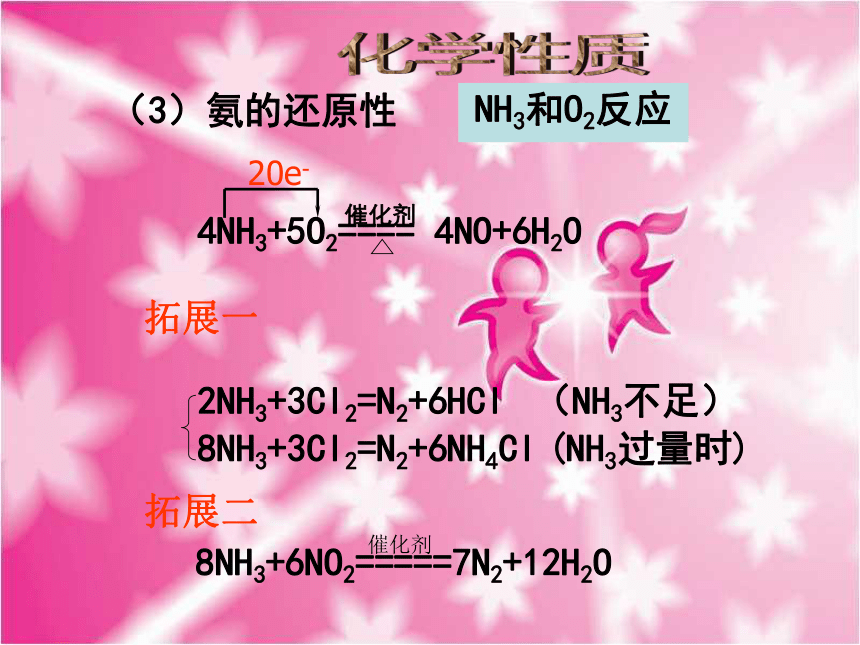
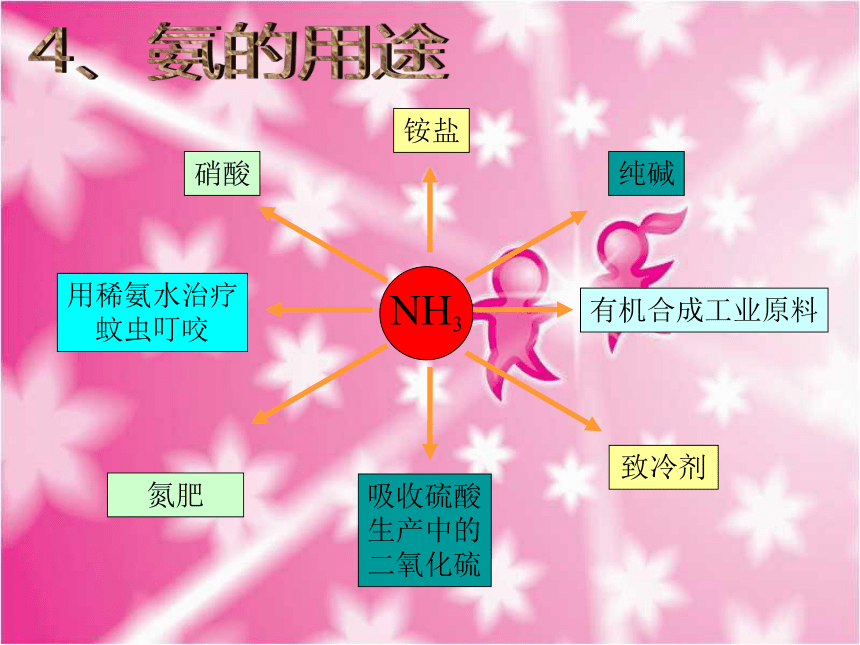
②从氮的化合价,预测其化学性质NH3小结极性分子3、化学性质(1)氨气与水反应小结a.氨水是混合物,成份有H2O、NH3、NH3·H2O、NH4+、OH-b.氨水是一种常见弱碱,一水合氨分子很不稳定,受热易分解如何保存?思考:液氨和氨水成份比较?化学性质NH3+HCl==== NH4Cl 2NH3+H2SO4==== (NH4)2SO4 白烟(2)氨气与酸反应小结a.氨与酸反应的本质:b.形成白烟的条件:NH3+ H+ ==NH4+挥发性酸与氨反应c.应用:检验氨气或挥发性酸吸收多余氨气(3)氨的还原性 NH3和O2反应拓展一拓展二化学性质4、氨的用途NH3小结1、掌握元素化合物的学习方法:2、本节课知识要点随堂检测1、下列各组气体,在通常情况下能稳定共存的是 ( )A.NH3 O2 HCl B.N2 H2 HCl
C.CO2 NO O2 D.H2S O2 SO2B2、常温常压下,密闭容器中充入下列气体后压强最大的是 ( )
A.0.3molHCl和0.3molNH3 B.0.2molH2和0.1molO2
C.0.2molNO和0.2molO2 D.0.2molH2S和0.1molSO2B3、如图所示:烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻震荡烧瓶,然后打开弹簧夹,烧杯中的液体呈喷泉状喷出,则a、b可能是: ( )
A、a为NH3,b为H2O
B、 a为CO2,b为浓NaOH溶液
C、a为Cl2,b为饱和NaCl溶液
D、a为N2,b为浓NaOH溶液A Babb4、如图所示,烧瓶中收集满的氨气。
(1)只打开a,现象__原因______
(2)只挤压b,现象__原因______
(3)挤压b,打开a,现象__原因___
(4)若装置气密性良好,而实验中有时液体不能充满烧瓶,原因______
(5)若液体充满烧瓶,则氨水的物质的量浓度为_______(S.T.P)
(6)若烧瓶中盛有排空气法收集的氨气,喷泉实验后,氨水的物质的量浓度为_______(S.T.P)止水夹ab水滴有酚酞的水氨的催化氧化喷泉实验放松黄山美景.swf休息 试剂:氯化铵 与 消石灰
5、氨气的实验室制法(装置)△反应方程式:
2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O
?动画
实验室制备氨气的装置选择安装 性质检验的操作练习 2:
[观察]在制氨装置中找错误 练习3:
讨论氨水的成份并与氯水成份对比:讨论:氨水的成分三分子三离子NH3 H2O NH3·H2ONH4+ OH— H+四离子三分子Cl2 H2O HClOH+ OH— Cl— c lO—碱性酸性回顾:氯水的成分溶液酸碱性:氧 化 性无有漂 白 性无有二、铵盐1、铵盐的性质( )
(1)易溶性:均易溶于水。
(2)不稳定性:受热易分解。
(3)与碱反应:
NH4++OH-===NH3↑ +H2O
2、用途:△铵盐的性质检验和用途氨盐的性质.swf
(常温下,1体积水能溶解700体积氨)喷泉实验浓度越大,则密度越小2、氨分子的结构分子式: 电子式: 结构式:空间构型:三角锥形键角:107o18′讨论:①结合氨气的喷泉实验,预测其化学性质。
②从氮的化合价,预测其化学性质NH3小结极性分子3、化学性质(1)氨气与水反应小结a.氨水是混合物,成份有H2O、NH3、NH3·H2O、NH4+、OH-b.氨水是一种常见弱碱,一水合氨分子很不稳定,受热易分解如何保存?思考:液氨和氨水成份比较?化学性质NH3+HCl==== NH4Cl 2NH3+H2SO4==== (NH4)2SO4 白烟(2)氨气与酸反应小结a.氨与酸反应的本质:b.形成白烟的条件:NH3+ H+ ==NH4+挥发性酸与氨反应c.应用:检验氨气或挥发性酸吸收多余氨气(3)氨的还原性 NH3和O2反应拓展一拓展二化学性质4、氨的用途NH3小结1、掌握元素化合物的学习方法:2、本节课知识要点随堂检测1、下列各组气体,在通常情况下能稳定共存的是 ( )A.NH3 O2 HCl B.N2 H2 HCl
C.CO2 NO O2 D.H2S O2 SO2B2、常温常压下,密闭容器中充入下列气体后压强最大的是 ( )
A.0.3molHCl和0.3molNH3 B.0.2molH2和0.1molO2
C.0.2molNO和0.2molO2 D.0.2molH2S和0.1molSO2B3、如图所示:烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻震荡烧瓶,然后打开弹簧夹,烧杯中的液体呈喷泉状喷出,则a、b可能是: ( )
A、a为NH3,b为H2O
B、 a为CO2,b为浓NaOH溶液
C、a为Cl2,b为饱和NaCl溶液
D、a为N2,b为浓NaOH溶液A Babb4、如图所示,烧瓶中收集满的氨气。
(1)只打开a,现象__原因______
(2)只挤压b,现象__原因______
(3)挤压b,打开a,现象__原因___
(4)若装置气密性良好,而实验中有时液体不能充满烧瓶,原因______
(5)若液体充满烧瓶,则氨水的物质的量浓度为_______(S.T.P)
(6)若烧瓶中盛有排空气法收集的氨气,喷泉实验后,氨水的物质的量浓度为_______(S.T.P)止水夹ab水滴有酚酞的水氨的催化氧化喷泉实验放松黄山美景.swf休息 试剂:氯化铵 与 消石灰
5、氨气的实验室制法(装置)△反应方程式:
2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O
?动画
实验室制备氨气的装置选择安装 性质检验的操作练习 2:
[观察]在制氨装置中找错误 练习3:
讨论氨水的成份并与氯水成份对比:讨论:氨水的成分三分子三离子NH3 H2O NH3·H2ONH4+ OH— H+四离子三分子Cl2 H2O HClOH+ OH— Cl— c lO—碱性酸性回顾:氯水的成分溶液酸碱性:氧 化 性无有漂 白 性无有二、铵盐1、铵盐的性质( )
(1)易溶性:均易溶于水。
(2)不稳定性:受热易分解。
(3)与碱反应:
NH4++OH-===NH3↑ +H2O
2、用途:△铵盐的性质检验和用途氨盐的性质.swf
