化学平衡及图象[上学期]
文档属性
| 名称 | 化学平衡及图象[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 138.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-10-24 00:00:00 | ||
图片预览





文档简介
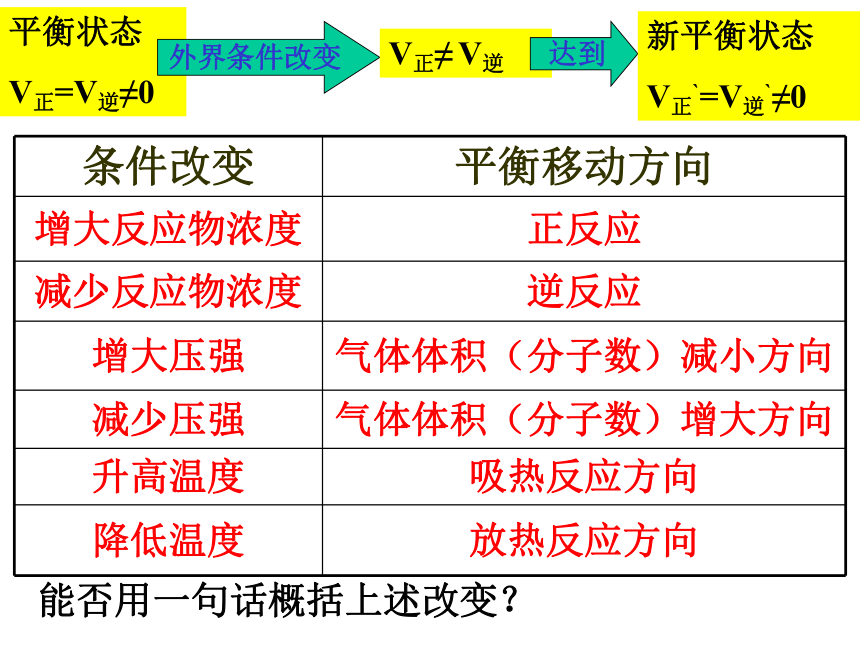
课件14张PPT。化学平衡及图象平衡状态
V正=V逆≠0 外界条件改变V正≠ V逆达到新平衡状态
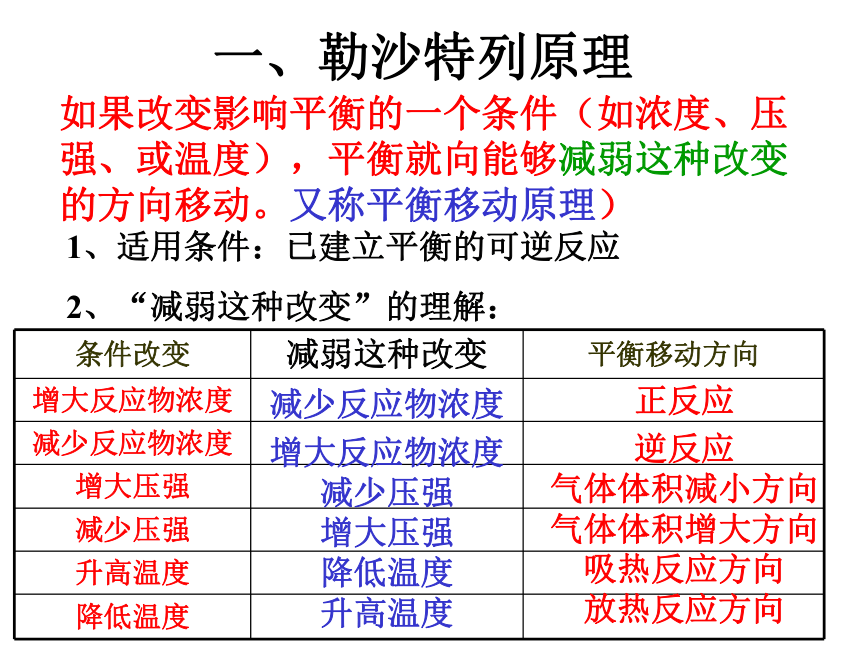
V正`=V逆`≠0 能否用一句话概括上述改变?一、勒沙特列原理如果改变影响平衡的一个条件(如浓度、压强、或温度),平衡就向能够减弱这种改变的方向移动。又称平衡移动原理)1、适用条件:已建立平衡的可逆反应
2、“减弱这种改变”的理解:正反应
逆反应
气体体积减小方向
气体体积增大方向
吸热反应方向
放热反应方向减少反应物浓度
增大反应物浓度
减少压强
增大压强
降低温度
升高温度练习1:在高温下,反应2HBr(g) H2 (g) + Br2 (g) -Q达到平衡,要使混气颜色加深,可采取的方法是( )
A.减压 B.缩小体积
C.升温 D.增大H2浓度 B、C练习2:乙酸蒸气能形成二聚分子
2CH3COOH(g) (CH3COOH)2 (g) +Q,欲测定单体乙酸的分子量,应采用的条件是( )
A.高温低压 B.低温高压
C.低温低压 D.高温高压 A练习3:某温度下反应S2Cl2 (l) + Cl2 (g) 2SCl2 (l)
(橙黄色) (鲜红色)
+50.16KJ,在密闭容器中达到平衡,下列说法错误的是( )
A.温度不变,增大容器体积,S2Cl2的转化率降低
B.温度不变,缩小容器体积,液体颜色加深
C.升高温度,压强不变,液体颜色变浅
D.降低温度,体积不变,Cl2的转化率降低 D练习5:在下列已达到化学平衡的反应中,当升温并同时降压时平衡必右移的是( )
A.A(g) + 3B(g) 2C(g) +Q
B.A(g) +B(g) C(g) + D(g)-Q
C.A(s) + 2B(g) C(g)-Q
D.A(g) B(g) +C(g) +Q B二、外界条件对化学平衡 图象的影响1、一个条件的改变的化学平衡图像2、二个及以上条件改变的化学平衡图像练1:18. 密闭容器中mA(g)+nB(g) pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:
(1)增大压强,A的转化率____,平衡向____移动,达到平衡后,混合物中C的质量分数________。
(2)上述化学方程式中的系数m、n、p的正确关系是____,向上述平衡体系中加入B,则平衡________。
(3)当降低温度时,C的质量分数增大,则A的转化率____,正反应是____热反应。降低左减少m+nM(气)+N(气) R(气)+2L
此反应符合下面图像,下列叙述是正确的是( )
(A) 正反应吸热,L是气体
(B) 正反应吸热,L是固体
(C) 正反应放热,L是气体
(D) 正反应放热,L是固体或液体 C练习3可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是( )。
(A)达平衡后,加入催化剂
则C%增大(B)达平衡后,
若升温,平衡左移
(C)化学方程式中n>e+f
(D)达平衡后,增加A的量有利于平衡向右移动 B、C练4:在可逆反应mA(g)+nB(g) pC(g)+Q中m、n、p为系数,且m+n>p Q>0。分析下列各图,在平衡体系中A的质量分数与温度toC、压强P关系正确的是( ) B练5:图中表示外界条件(t、p)的变化对下列反应的影响:L(固)+G(气) 2R(气)-Q,y 轴表示的是( )
(A) 平衡时,混合气中R的百分含量
(B) 平衡时,混合气中G的百分含量
(C) G的转化率
(D) L的转化率 B练6:某可逆反应L(s)+G(g) 3R(g)-Q,本图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示( )
(A)平衡混合气中R的质量分数
(B)达到平衡时G的转化率
(C)平衡混合气中G的质量分数
(D)达到平衡时L的转化率 C
V正=V逆≠0 外界条件改变V正≠ V逆达到新平衡状态
V正`=V逆`≠0 能否用一句话概括上述改变?一、勒沙特列原理如果改变影响平衡的一个条件(如浓度、压强、或温度),平衡就向能够减弱这种改变的方向移动。又称平衡移动原理)1、适用条件:已建立平衡的可逆反应
2、“减弱这种改变”的理解:正反应
逆反应
气体体积减小方向
气体体积增大方向
吸热反应方向
放热反应方向减少反应物浓度
增大反应物浓度
减少压强
增大压强
降低温度
升高温度练习1:在高温下,反应2HBr(g) H2 (g) + Br2 (g) -Q达到平衡,要使混气颜色加深,可采取的方法是( )
A.减压 B.缩小体积
C.升温 D.增大H2浓度 B、C练习2:乙酸蒸气能形成二聚分子
2CH3COOH(g) (CH3COOH)2 (g) +Q,欲测定单体乙酸的分子量,应采用的条件是( )
A.高温低压 B.低温高压
C.低温低压 D.高温高压 A练习3:某温度下反应S2Cl2 (l) + Cl2 (g) 2SCl2 (l)
(橙黄色) (鲜红色)
+50.16KJ,在密闭容器中达到平衡,下列说法错误的是( )
A.温度不变,增大容器体积,S2Cl2的转化率降低
B.温度不变,缩小容器体积,液体颜色加深
C.升高温度,压强不变,液体颜色变浅
D.降低温度,体积不变,Cl2的转化率降低 D练习5:在下列已达到化学平衡的反应中,当升温并同时降压时平衡必右移的是( )
A.A(g) + 3B(g) 2C(g) +Q
B.A(g) +B(g) C(g) + D(g)-Q
C.A(s) + 2B(g) C(g)-Q
D.A(g) B(g) +C(g) +Q B二、外界条件对化学平衡 图象的影响1、一个条件的改变的化学平衡图像2、二个及以上条件改变的化学平衡图像练1:18. 密闭容器中mA(g)+nB(g) pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:
(1)增大压强,A的转化率____,平衡向____移动,达到平衡后,混合物中C的质量分数________。
(2)上述化学方程式中的系数m、n、p的正确关系是____,向上述平衡体系中加入B,则平衡________。
(3)当降低温度时,C的质量分数增大,则A的转化率____,正反应是____热反应。降低左减少m+n
此反应符合下面图像,下列叙述是正确的是( )
(A) 正反应吸热,L是气体
(B) 正反应吸热,L是固体
(C) 正反应放热,L是气体
(D) 正反应放热,L是固体或液体 C练习3可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是( )。
(A)达平衡后,加入催化剂
则C%增大(B)达平衡后,
若升温,平衡左移
(C)化学方程式中n>e+f
(D)达平衡后,增加A的量有利于平衡向右移动 B、C练4:在可逆反应mA(g)+nB(g) pC(g)+Q中m、n、p为系数,且m+n>p Q>0。分析下列各图,在平衡体系中A的质量分数与温度toC、压强P关系正确的是( ) B练5:图中表示外界条件(t、p)的变化对下列反应的影响:L(固)+G(气) 2R(气)-Q,y 轴表示的是( )
(A) 平衡时,混合气中R的百分含量
(B) 平衡时,混合气中G的百分含量
(C) G的转化率
(D) L的转化率 B练6:某可逆反应L(s)+G(g) 3R(g)-Q,本图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示( )
(A)平衡混合气中R的质量分数
(B)达到平衡时G的转化率
(C)平衡混合气中G的质量分数
(D)达到平衡时L的转化率 C
