元素周期表(第三课时)[下学期]
文档属性
| 名称 | 元素周期表(第三课时)[下学期] |  | |
| 格式 | rar | ||
| 文件大小 | 238.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-03-15 08:47:00 | ||
图片预览






文档简介
课件15张PPT。元素周期表(三) 第一章 第一节学习目标:一、了解核素、同位素的概念;二、知道元素原子量的计算方法
复习:元素的定义:想一想:同种元素的中子数是不是都相同?元素是具有相同核电荷数一类原子总称。质量数(A) = 质子数(Z) + 中子数(N) P9核电荷数 = 质子数氢 重氢 超重氢 氕氘氚H D T1、核素:具有一定数目的质子和一定数目
的中子的一种原子叫核素。 质子数:111中子数:012★2、同位素:★3、同位素的性质:(1)同一元素的各种同位素虽然质量数
不同,但它们的化学性质几乎完全相同。质子数相同而中子数不同的同一元素
的不同原子,互称同位素。(2)天然存在的某种元素里,各种同位素
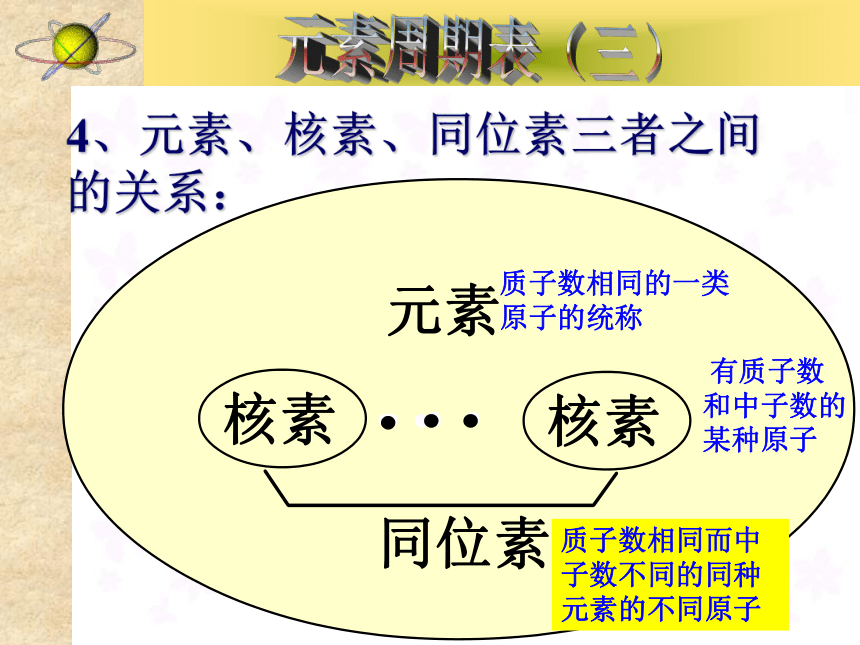
所占的原子个数百分比一般是不变的。4、元素、核素、同位素三者之间
的关系: 质子数相同的一类原子的统称 有质子数和中子数的某种原子质子数相同而中子数不同的同种元素的不同原子 5、同位素举例及应用(1)H的三种同位素:
(2)U的三种同位素:
是造原子弹及核反应堆的材料。(3)C的三种同位素:
是原子量的标准 是制造氢弹的材料。92U2346C126C12练习1:A、氢的5种同位素
B、5种氢元素
C、氢的5种同素异形体
D、氢元素的5种不同微粒 H+、H2 是( )同素异形体是指同一种元素形成的多种不同单质 D练习2:A、它们可能是不同的分子
B、可能是相同的原子
C、可能是同位素
D、可能是一种分子和一种离子 一种微粒的质子数和电子数与另一种微粒的质子数和电子数均相等,下列对2种微粒间关系的说法错误的是( )D如:H2O HF如: 二、元素的(平均)相对原子质量: 同位素的相对原子质量:是各同位素原子的真实质量分别与 C的真实质量1/12的比值。二、元素的(平均)相对原子质量: =A1×a1%+A2×a2%+… 其中A1、A2…为同位素的相对原子质量 a1%、a2%…为同位素原子的个数分数或摩尔分数(不代表质量分数)元素的(平均)相对原子质量: 按各种天然同位素原子所占的一定的百分比算出的平均值
Cl 34.969 75.77% Cl 36.966 24.23% 34.969×0.7577+36.966×0.2423
=35.453,
即:氯的原子量为35.453。作业:1、课本P11 习题 4. (1)、(2) 题 2、预习课本第二节元素周期律及高中化学 全解P21-----P43练习3:已知某元素X的一种同位素的质量数为A,中子数为N,则下列判断不正确的是( ) A.这种同位素的符号可表示为 X B.A可代表这种同位素的近似相对原
子质量 C.A小于X的元素的相对原子质量
D.A不能代表X元素的相对原子质量 AA-NC小结:2、(1)同一元素的各种同位素虽然质量数
不同,但它们的化学性质几乎完全相同。1、质子数相同而中子数不同的同一元素的不同原子,互称同位素。(2)天然存在的某种元素里,各种同位素
所占的原子个数百分比一般是不变的。
复习:元素的定义:想一想:同种元素的中子数是不是都相同?元素是具有相同核电荷数一类原子总称。质量数(A) = 质子数(Z) + 中子数(N) P9核电荷数 = 质子数氢 重氢 超重氢 氕氘氚H D T1、核素:具有一定数目的质子和一定数目
的中子的一种原子叫核素。 质子数:111中子数:012★2、同位素:★3、同位素的性质:(1)同一元素的各种同位素虽然质量数
不同,但它们的化学性质几乎完全相同。质子数相同而中子数不同的同一元素
的不同原子,互称同位素。(2)天然存在的某种元素里,各种同位素
所占的原子个数百分比一般是不变的。4、元素、核素、同位素三者之间
的关系: 质子数相同的一类原子的统称 有质子数和中子数的某种原子质子数相同而中子数不同的同种元素的不同原子 5、同位素举例及应用(1)H的三种同位素:
(2)U的三种同位素:
是造原子弹及核反应堆的材料。(3)C的三种同位素:
是原子量的标准 是制造氢弹的材料。92U2346C126C12练习1:A、氢的5种同位素
B、5种氢元素
C、氢的5种同素异形体
D、氢元素的5种不同微粒 H+、H2 是( )同素异形体是指同一种元素形成的多种不同单质 D练习2:A、它们可能是不同的分子
B、可能是相同的原子
C、可能是同位素
D、可能是一种分子和一种离子 一种微粒的质子数和电子数与另一种微粒的质子数和电子数均相等,下列对2种微粒间关系的说法错误的是( )D如:H2O HF如: 二、元素的(平均)相对原子质量: 同位素的相对原子质量:是各同位素原子的真实质量分别与 C的真实质量1/12的比值。二、元素的(平均)相对原子质量: =A1×a1%+A2×a2%+… 其中A1、A2…为同位素的相对原子质量 a1%、a2%…为同位素原子的个数分数或摩尔分数(不代表质量分数)元素的(平均)相对原子质量: 按各种天然同位素原子所占的一定的百分比算出的平均值
Cl 34.969 75.77% Cl 36.966 24.23% 34.969×0.7577+36.966×0.2423
=35.453,
即:氯的原子量为35.453。作业:1、课本P11 习题 4. (1)、(2) 题 2、预习课本第二节元素周期律及高中化学 全解P21-----P43练习3:已知某元素X的一种同位素的质量数为A,中子数为N,则下列判断不正确的是( ) A.这种同位素的符号可表示为 X B.A可代表这种同位素的近似相对原
子质量 C.A小于X的元素的相对原子质量
D.A不能代表X元素的相对原子质量 AA-NC小结:2、(1)同一元素的各种同位素虽然质量数
不同,但它们的化学性质几乎完全相同。1、质子数相同而中子数不同的同一元素的不同原子,互称同位素。(2)天然存在的某种元素里,各种同位素
所占的原子个数百分比一般是不变的。
