元素周期表[下学期]
图片预览






文档简介
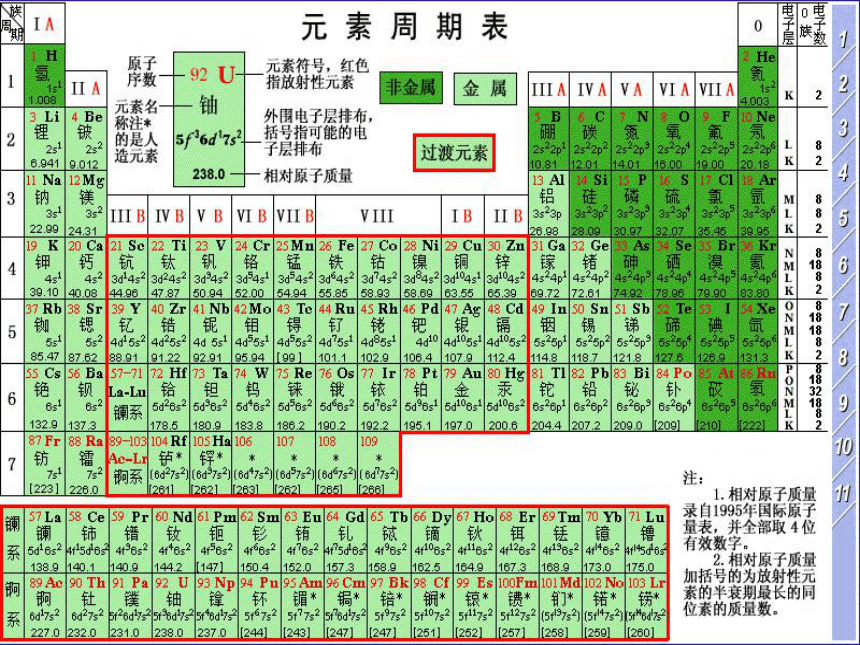
课件22张PPT。 第一课时元素周期表双峰一中化学组:谢战春由1—18号元素的原子结构分析1.每一横行有什么相同点?2.每一纵行有什么相同点?每一横行的电子层数相同每一纵行的最外层电子数相同(除稀有气体元素外)一﹑元素周期表的编排㈡编排原则: ⑴ 按原子序数递增的顺序从左到右排列 ⑵ 将电子层数相同的元素排列成一个横行. ⑶ 把最外层电子数相同的元素按电子层
数递增的顺序从上到下排成纵行.㈠编排依据:元素周期律二.元素周期表的结构周期序数 = 电子层数 1.横行( 个)—⑴具有相同的电子层数的元素按照原子序数递增的顺序排列的一个横行称为一个周期。 周期(7个)7⑵周期第1周期:第2周期:第3周期:第4周期:第5周期:第6周期:第7周期:2种元素8种元素8种元素18种元素18种元素32种元素26种元素③锕89Ac – 铹103Lr 共15 种元素称锕系元素,
位于第七周期.②镧57La – 镥71Lu 共15 种元素称镧系元素,
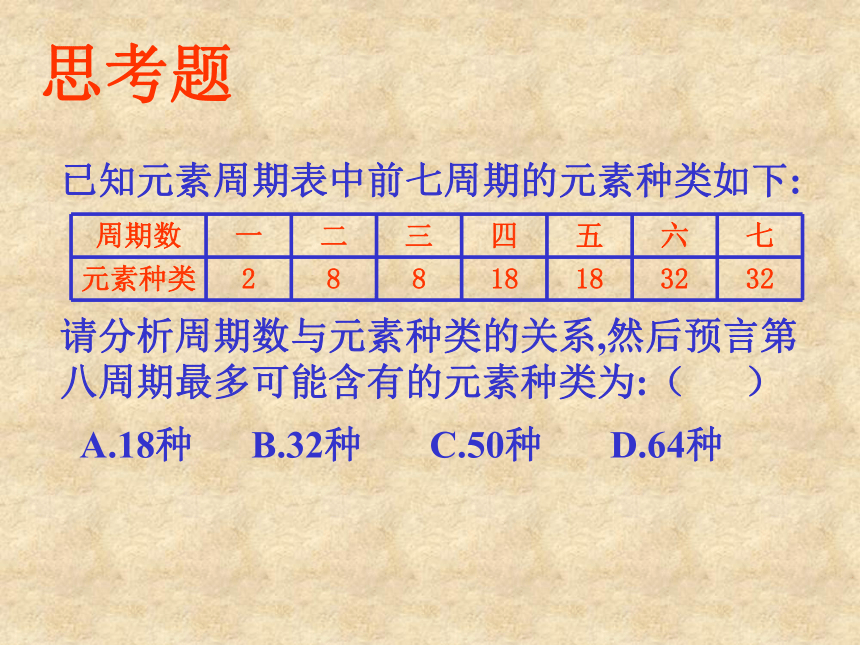
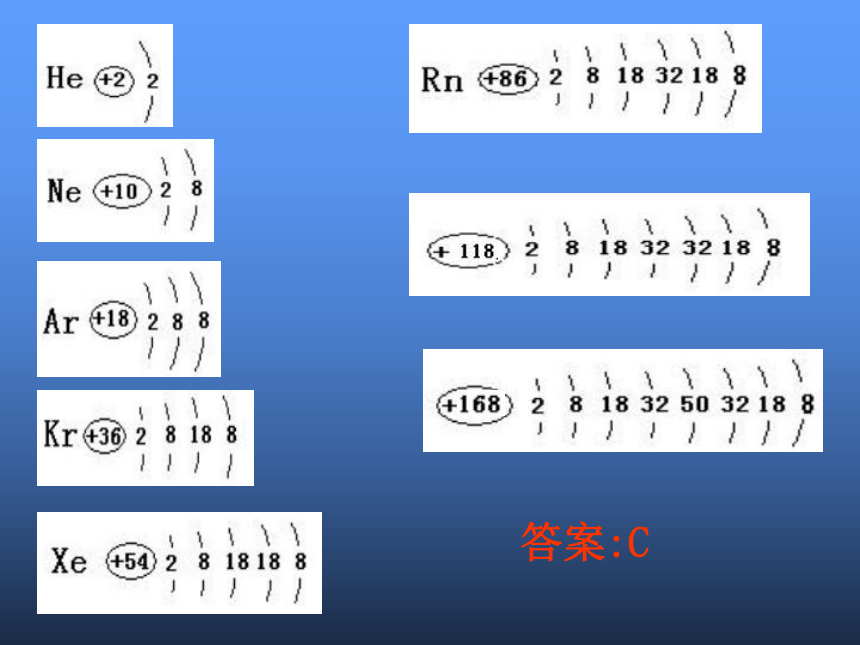
位于第六周期.⑶注意:①除第1、7周期外,每个周期都是从碱金属元 素开始,逐渐过渡到卤素,最后以稀有气体元素结束.④超铀元素:92号元素铀以后的元素它们的电子层结构和性质十分相似它们的电子层结构和性质十分相似思考题已知元素周期表中前七周期的元素种类如下:请分析周期数与元素种类的关系,然后预言第八周期最多可能含有的元素种类为:( )A.18种 B.32种 C.50种 D.64种答案:C2.纵行( 个)—(1)族又有主族和副族之分。 主族:由短周期元素和长周期元素共
同构成的族. 副族:完全由长周期元素构成的族。 族(16个)18族ⅠA , ⅡA , ⅢA , ⅣA ,ⅤA , ⅥA , ⅦA 第VIII 族:稀有气体元素 零族:共七个主族ⅠB , ⅡB , ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB 共七个副族第八、九、十纵行,位于Ⅶ B 与ⅠB中间 (2)⑶注意:主族序数 = 最外层电子数 ①②各族在元素周期表中的位置 ③过渡元素:ⅠA、 从ⅢB族到ⅡB族10个纵行的元素.它包括了第Ⅷ族和全部副族元素,这些元素都是金属元素0。ⅦA、ⅥA、ⅤA、ⅣA、ⅢA、ⅡB、ⅠB、Ⅷ,ⅦB、ⅥB、ⅤB、ⅣB,ⅢB、ⅡA、请你回答1.氦元素原子最外层有两个电子,为什么不把它排在ⅡA族?2.卤族元素和碱金属元素分别是周期表的哪一族?3.IA族就是碱金属元素吗? K层填充两个电子已达饱和,性质与ⅡA族的元素完全不同ⅦA、 不对,它还包括氢元素。IA4.短周期元素、长周期元素和不完全周期元素分别包括哪些族元素?短周期元素只包括主族和零族元素长周期元素和不完全周期元素均包括主族、副族、 Ⅷ族、零族元素5.过渡元素包括哪些族元素?过渡元素都是金属元素吗?只包括Ⅷ族、副族元素过渡元素都是金属元素练习已知某主族元素的原子结构示意图,判断其在周期表中的位置第三周期ⅦA族第四周期ⅠA族小结元素周期表的结构: 七主七副七周期,熟记: 三个短周期,七个主族和零族的元素符号和名称。 Ⅷ族零族镧锕系。课后练习 A、B、C是周期表中相邻的三种短周期元素,其中A、B是同周期,B、C是同主族。此三种元素原子最外层电子数之和为17,质子数之和为31,则A、B、C分别为什么元素?M分析 设A.B.C的位置关系用联立方程式求解.由三元素有如下四种位置关系:常规解法:①②设①中B的质子数为X,则A为(X-1),C为(X+8)可得:X+(X-1)+ (X+8)=31,X=8.
故B为O, A为N, C为S. 设②中B的质子数为X,则A为(X+1),C为(X+8)可得: X+(X+1)+ (X+8)=31,X=22/3.
(不合题意)③④设③中B的质子数为X,则A为(X-1),C为(X-8)可得:
X+(X-1)+ (X-8)=31,X=40/3.
(不合题意)设④中B的质子数为X, 则A为(X+1),C为(X+8)可得:
X+(X+1)+ (X-8)=31,X=38/3.
(不合题意)分析 三种元素原子最外层电子平均数为
17/3 = 5.7 三种元素位于第ⅤA、ⅥA族。 三种元素质子数之和为31, 应为第二第三周期元素观察,可得 A是氮元素 B是氧元素 C是硫元素 5 + 2×6 = 17试商法:再
见
数递增的顺序从上到下排成纵行.㈠编排依据:元素周期律二.元素周期表的结构周期序数 = 电子层数 1.横行( 个)—⑴具有相同的电子层数的元素按照原子序数递增的顺序排列的一个横行称为一个周期。 周期(7个)7⑵周期第1周期:第2周期:第3周期:第4周期:第5周期:第6周期:第7周期:2种元素8种元素8种元素18种元素18种元素32种元素26种元素③锕89Ac – 铹103Lr 共15 种元素称锕系元素,
位于第七周期.②镧57La – 镥71Lu 共15 种元素称镧系元素,
位于第六周期.⑶注意:①除第1、7周期外,每个周期都是从碱金属元 素开始,逐渐过渡到卤素,最后以稀有气体元素结束.④超铀元素:92号元素铀以后的元素它们的电子层结构和性质十分相似它们的电子层结构和性质十分相似思考题已知元素周期表中前七周期的元素种类如下:请分析周期数与元素种类的关系,然后预言第八周期最多可能含有的元素种类为:( )A.18种 B.32种 C.50种 D.64种答案:C2.纵行( 个)—(1)族又有主族和副族之分。 主族:由短周期元素和长周期元素共
同构成的族. 副族:完全由长周期元素构成的族。 族(16个)18族ⅠA , ⅡA , ⅢA , ⅣA ,ⅤA , ⅥA , ⅦA 第VIII 族:稀有气体元素 零族:共七个主族ⅠB , ⅡB , ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB 共七个副族第八、九、十纵行,位于Ⅶ B 与ⅠB中间 (2)⑶注意:主族序数 = 最外层电子数 ①②各族在元素周期表中的位置 ③过渡元素:ⅠA、 从ⅢB族到ⅡB族10个纵行的元素.它包括了第Ⅷ族和全部副族元素,这些元素都是金属元素0。ⅦA、ⅥA、ⅤA、ⅣA、ⅢA、ⅡB、ⅠB、Ⅷ,ⅦB、ⅥB、ⅤB、ⅣB,ⅢB、ⅡA、请你回答1.氦元素原子最外层有两个电子,为什么不把它排在ⅡA族?2.卤族元素和碱金属元素分别是周期表的哪一族?3.IA族就是碱金属元素吗? K层填充两个电子已达饱和,性质与ⅡA族的元素完全不同ⅦA、 不对,它还包括氢元素。IA4.短周期元素、长周期元素和不完全周期元素分别包括哪些族元素?短周期元素只包括主族和零族元素长周期元素和不完全周期元素均包括主族、副族、 Ⅷ族、零族元素5.过渡元素包括哪些族元素?过渡元素都是金属元素吗?只包括Ⅷ族、副族元素过渡元素都是金属元素练习已知某主族元素的原子结构示意图,判断其在周期表中的位置第三周期ⅦA族第四周期ⅠA族小结元素周期表的结构: 七主七副七周期,熟记: 三个短周期,七个主族和零族的元素符号和名称。 Ⅷ族零族镧锕系。课后练习 A、B、C是周期表中相邻的三种短周期元素,其中A、B是同周期,B、C是同主族。此三种元素原子最外层电子数之和为17,质子数之和为31,则A、B、C分别为什么元素?M分析 设A.B.C的位置关系用联立方程式求解.由三元素有如下四种位置关系:常规解法:①②设①中B的质子数为X,则A为(X-1),C为(X+8)可得:X+(X-1)+ (X+8)=31,X=8.
故B为O, A为N, C为S. 设②中B的质子数为X,则A为(X+1),C为(X+8)可得: X+(X+1)+ (X+8)=31,X=22/3.
(不合题意)③④设③中B的质子数为X,则A为(X-1),C为(X-8)可得:
X+(X-1)+ (X-8)=31,X=40/3.
(不合题意)设④中B的质子数为X, 则A为(X+1),C为(X+8)可得:
X+(X+1)+ (X-8)=31,X=38/3.
(不合题意)分析 三种元素原子最外层电子平均数为
17/3 = 5.7 三种元素位于第ⅤA、ⅥA族。 三种元素质子数之和为31, 应为第二第三周期元素观察,可得 A是氮元素 B是氧元素 C是硫元素 5 + 2×6 = 17试商法:再
见
