元素周期律[下学期]
图片预览





文档简介
课件18张PPT。第二课时理论推测 11-18号( 第三周期)元素的金属性和非金属性递变规律 当电子层数相同时,随着元素原子序数的递增,最外层电子数从1递增到8,原子半径(除稀有气体元素)逐渐减小,原子核对外层电子的吸引力逐渐增强,因此失电子能力逐渐减弱,得电子能力逐渐增强,即元素的金属性逐渐减弱,非金属性逐渐增强。一、判断元素金属性强弱的依据: 1、单质跟水(或酸)反应置换出氢的难易; 2、最高价氧化物的水化物——氢氧化物的碱性强弱; 3、置换反应,强置换弱,被置换的金属性弱; 越容易反应,元素的金属性越强M(OH)x的碱性越强,M的金属性越强元素的金属性和非金属性 实验原理实验探究1、跟氢气生成气态氢化物的难易程度以及氢化物的稳定性; 越容易反应,生成的氢化物越稳定,元素的非金属性越强2、元素最高价氧化物的水化物的酸性强弱。 酸性越强,元素的非金属性越强3、置换反应,被置换出的非金属的非金属性较弱二、判断非金属性强弱的依据实验一:钠、镁与水反应现象:钠与冷水剧烈反应,镁与沸水较快反应;分别滴加酚酞二者的水溶液颜色变红。结论: Na的金属性比Mg强实验探究Na、Mg、Al的金属性实验二:镁、铝与盐酸的反应现象:镁与酸剧烈反应,铝与酸较为迅速反应。结论:Mg的金属性比Al强实验探究冷水剧烈沸水反应盐酸剧烈盐酸较快NaOH
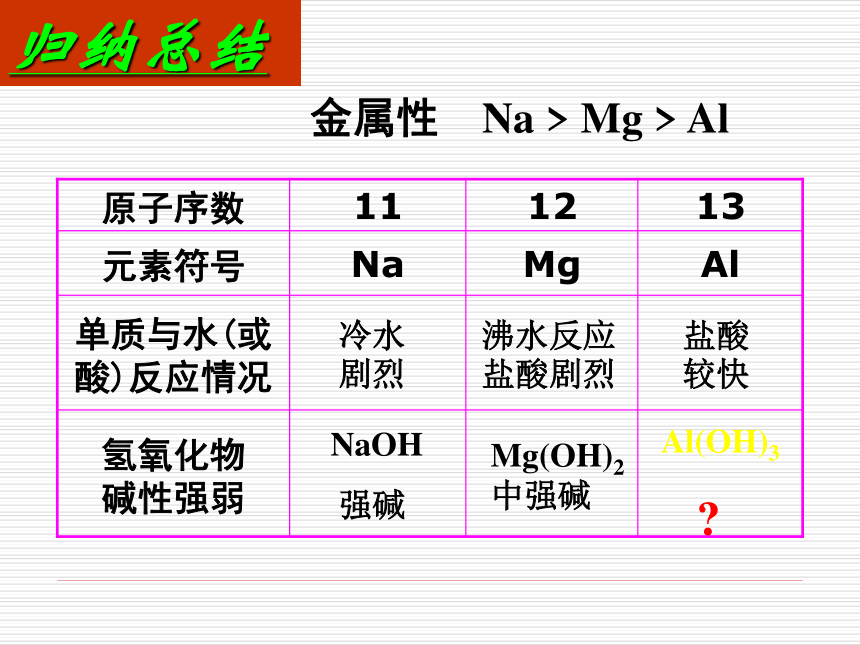
强碱Mg(OH)2中强碱Al(OH)3
?金属性 Na > Mg > Al归纳总结 既能跟酸反应,又能跟碱反应的氢氧化物,叫作两性氢氧化物。Al(OH)3 + 3HCl = AlCl3 + 3H2OAl(OH)3 + 3H+ = Al3+ + 3H2O Al(OH)3 + OH– = AlO2– + 2H2OAl(OH)3是两性氢氧化物结论: 反应:实验探究实验三:铝的氢氧化物性质探讨H3AlO3金属性 Na > Mg > Al强碱中强碱归纳总结?两性氢氧化物
我们曾把氧化物分为酸性氧化物和碱性氧化物。那么,Na2O、MgO、Al2O3分别属哪类化合物呢??Na2O、MgO为碱性氧化物,什么是两性氧化物? 既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,叫两性氧化物。如:Al2O3、ZnO?Al2O3+6HCl=2AlCl3+3H2OAl2O3+2NaOH=2NaAlO2+H2O偏铝酸钠问题探究Al2O3为两性氧化物高温光照或点燃爆炸化合磷蒸气加热自学归纳Si、P、S、Cl的非金属性稀有气体元素金属性逐渐减弱,非金属性逐渐增强归纳总结小 结: 元素的性质随着元素原子序数的递增而呈周期性的变化,这个规律叫做元素周期律. 元素性质的周期性变化是元素原子的核外电子排布的周期性变化的必然结果.1.下列对铯(Cs)的性质预测中,
错误的是 ( )
A.它只有一种氧化物Cs2O
B.它与水剧烈反应放出H2
C.其离子有很强的氧化性
D.它的碳酸盐稳定,受热很难分解
巩固提高AC2、现代无机化学理论的基石之一 ——元素周期律,是1869年门捷列夫在总结前人经验的基础上发现的,对新元素的发现、化学理论和实验等研究工作起到了指导作用。周期律揭示的规律包括以下内容中的 ( ) ① 性质随相对原子质量的递增作周期性变化 ② 元素的性质是元素原子序数的周期性函数 ③ 事物的量变可以引起质变 ④ 元素性质的递变只取决于其核电荷数的递变,与原子结构无关 A、① ② B、 ② ③ C、① ④ D、 ① ② ③ ④ B 3、 (2002年上海市高考题)制冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到制冷目的。人们曾采用过乙醚、NH3、CH3Cl等作制冷剂,但它们不是有毒,就是易燃,于是科学家根据元素性质的递变规律来开发新的制冷剂。
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期: > >H2O>HF;
第三周期:SiH4>PH3> > 。
(2)化合物的毒性:PH3>NH3,H2S H2O;
CS2 CO2,CCl4 CF4(选填“>”、“<”或“=”)。
CH4 NH3
H2S
HCl
>>>于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl4的沸点为76.8 ℃,CF4的沸点-128℃,新制冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的制冷剂氟里昂CF2Cl2终于诞生了,其它类
似的还可以是 。
(4)然而,这种制冷剂造成了当今的某一环境问题
是 。
但求助于周期表中元素及其化合物的 变化趋势来开发制冷剂的科学思维方法是值得借鉴的。
①毒性②沸点③易燃性④水溶性⑤颜色
a?①②③ b?②④⑤ c?②③④
巩固提高CFCl3(或CF3Cl)使大气臭氧层出现空洞
a原子半径
强碱Mg(OH)2中强碱Al(OH)3
?金属性 Na > Mg > Al归纳总结 既能跟酸反应,又能跟碱反应的氢氧化物,叫作两性氢氧化物。Al(OH)3 + 3HCl = AlCl3 + 3H2OAl(OH)3 + 3H+ = Al3+ + 3H2O Al(OH)3 + OH– = AlO2– + 2H2OAl(OH)3是两性氢氧化物结论: 反应:实验探究实验三:铝的氢氧化物性质探讨H3AlO3金属性 Na > Mg > Al强碱中强碱归纳总结?两性氢氧化物
我们曾把氧化物分为酸性氧化物和碱性氧化物。那么,Na2O、MgO、Al2O3分别属哪类化合物呢??Na2O、MgO为碱性氧化物,什么是两性氧化物? 既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,叫两性氧化物。如:Al2O3、ZnO?Al2O3+6HCl=2AlCl3+3H2OAl2O3+2NaOH=2NaAlO2+H2O偏铝酸钠问题探究Al2O3为两性氧化物高温光照或点燃爆炸化合磷蒸气加热自学归纳Si、P、S、Cl的非金属性稀有气体元素金属性逐渐减弱,非金属性逐渐增强归纳总结小 结: 元素的性质随着元素原子序数的递增而呈周期性的变化,这个规律叫做元素周期律. 元素性质的周期性变化是元素原子的核外电子排布的周期性变化的必然结果.1.下列对铯(Cs)的性质预测中,
错误的是 ( )
A.它只有一种氧化物Cs2O
B.它与水剧烈反应放出H2
C.其离子有很强的氧化性
D.它的碳酸盐稳定,受热很难分解
巩固提高AC2、现代无机化学理论的基石之一 ——元素周期律,是1869年门捷列夫在总结前人经验的基础上发现的,对新元素的发现、化学理论和实验等研究工作起到了指导作用。周期律揭示的规律包括以下内容中的 ( ) ① 性质随相对原子质量的递增作周期性变化 ② 元素的性质是元素原子序数的周期性函数 ③ 事物的量变可以引起质变 ④ 元素性质的递变只取决于其核电荷数的递变,与原子结构无关 A、① ② B、 ② ③ C、① ④ D、 ① ② ③ ④ B 3、 (2002年上海市高考题)制冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到制冷目的。人们曾采用过乙醚、NH3、CH3Cl等作制冷剂,但它们不是有毒,就是易燃,于是科学家根据元素性质的递变规律来开发新的制冷剂。
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期: > >H2O>HF;
第三周期:SiH4>PH3> > 。
(2)化合物的毒性:PH3>NH3,H2S H2O;
CS2 CO2,CCl4 CF4(选填“>”、“<”或“=”)。
CH4 NH3
H2S
HCl
>>>于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl4的沸点为76.8 ℃,CF4的沸点-128℃,新制冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的制冷剂氟里昂CF2Cl2终于诞生了,其它类
似的还可以是 。
(4)然而,这种制冷剂造成了当今的某一环境问题
是 。
但求助于周期表中元素及其化合物的 变化趋势来开发制冷剂的科学思维方法是值得借鉴的。
①毒性②沸点③易燃性④水溶性⑤颜色
a?①②③ b?②④⑤ c?②③④
巩固提高CFCl3(或CF3Cl)使大气臭氧层出现空洞
a原子半径
