化学键[下学期]
图片预览





文档简介
课件16张PPT。第三节 化学键——离子键高一化学备课组
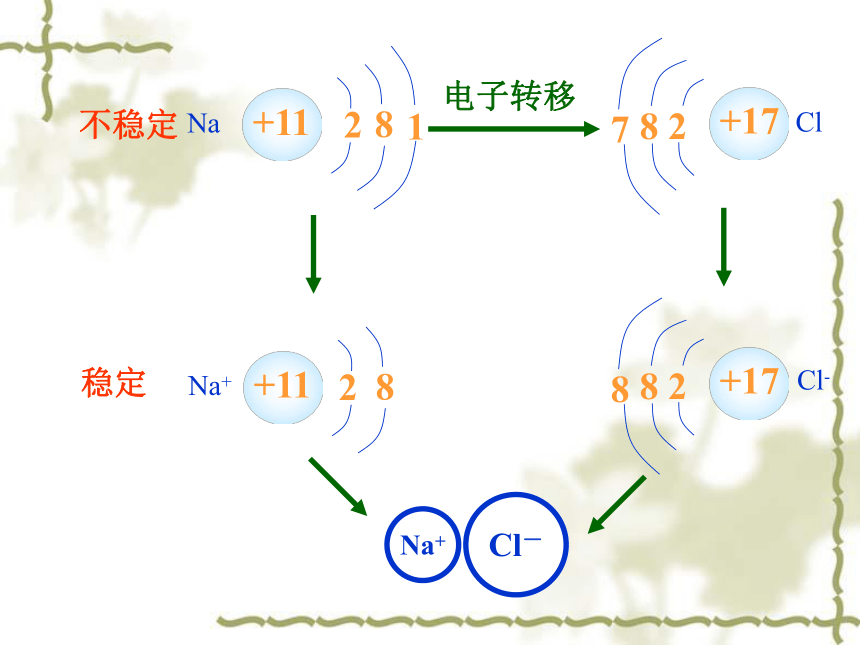
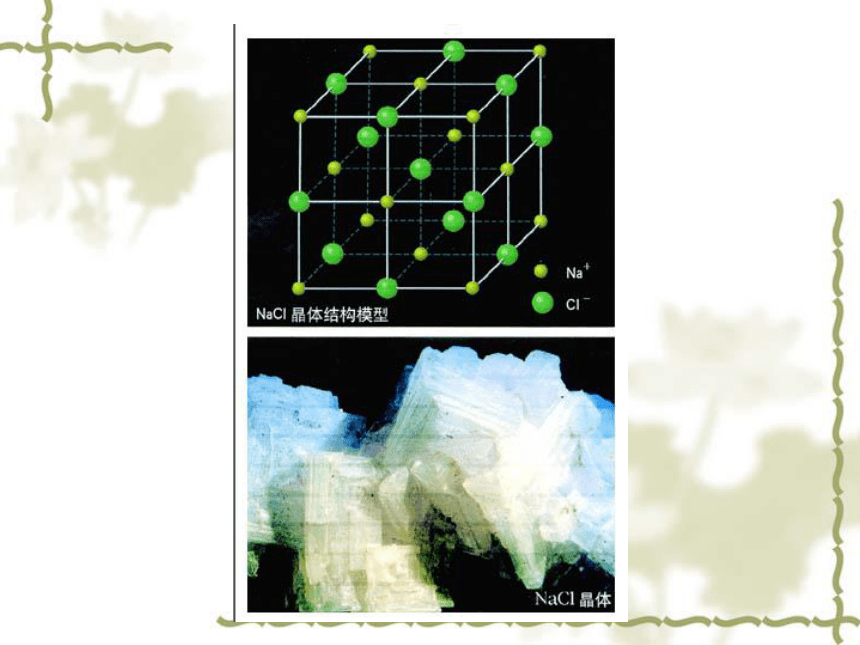
电子转移不稳定稳定ClCl-思考在氯化钠晶体中,Na+和Cl- 间存在哪些力? Na+离子和Cl-离子原子核和核外电子之间的静电相互吸引作用当阴阳离子接近到某一定距离时,吸引和排斥作
用达到平衡,阴阳离子间形成稳定的化学键。 阴阳离子间电子与电子、原子核与原子核间的相互排斥作用定义: 使阴阳离子结合成化合物的静电作用,叫做离子键。成键微粒:阴阳离子相互作用:静电作用(静电引力和斥力)成键过程:阴阳离子接近到某一定距离时,吸引和排斥达到平衡,就形成了离子键。含有离子键的化合物就是离子化合物。离子键 使阴阳离子结合成化合物的静电作用,叫 做离子键。思考 哪些物质能形成离子键? 活泼的金属元素(IA,IIA)和活泼的非金属
元素(VIA,VIIA)之间的化合物。 活泼的金属元素和酸根离子形成的盐 铵盐子和酸根离子(或活泼非金属元素)形成的盐。 在元素符号周围用“ · ”或“×”来表示
原子最外层电子的式子,叫电子式。H ·Na · ·Mg · ·Ca · 原子的电子式: 离子的电子式:H+Na+Mg2+Ca2+ ··(1)原子的电子式:常把其最外层电子数用小黑点“.”或小叉“×”来表示。(2)阳离子的电子式:不要求画出离子最外层电子数,只要在元素、符号右上角标出“n+”电荷字样。(3)阴离子的电子式:不但要画出最外层电子数,而且还应用于括号“[ ]”括起来,并在右上角标出“n·-”电荷字样。电子式 [ 练习] 写出下列微粒的电子式:
硫原子, 溴原子, 硫离子, 溴离子表示出原子之间是怎样结合的用 电子式 表示 离子化合物 的 形成过程 用电子式表示氯化钠的形成过程 用电子式表示溴化钙的形成过程 注意点1 离子须注明电荷数;2 相同的原子可以合并写,相同的离子要单个写;3.阴离子要用方括号括起;4.不能把 “→”写成 “ ==”5.用箭头表明电子转移方向(也可不标)离子化合物的电子式:由阴、阳离子的电子式组成,但对相同离子不能合并AB型AB2型A2B型[ 练习] ⑴ 用电子式表示氧化镁的形成过程 ⑵ 用电子式表示硫化钾的形成过程 箭头左方相同的微粒可以合并,
箭头右方相同的微粒不可以合并。注
意小结 使阴阳离子结合成化合物的静电作用,叫做离子键。 含有离子键的化合物一定是离子化合物区分: 用电子式表示物质
用电子式表示物质形成过程1.下列说法中正确的是 (??? )
A.两个原子或多个原子之间的相互作用叫做离子键。
B.阴、阳离子通过静电引力而形成的化学键叫做离子键。
C.只有金属元素和非金属元素化合时才能形成离子键。
D.大多数的盐、碱和低价金属氧化物中含有离子键。用电子式表示Na2S、MgBr2、Na2O
的形成过程
电子转移不稳定稳定ClCl-思考在氯化钠晶体中,Na+和Cl- 间存在哪些力? Na+离子和Cl-离子原子核和核外电子之间的静电相互吸引作用当阴阳离子接近到某一定距离时,吸引和排斥作
用达到平衡,阴阳离子间形成稳定的化学键。 阴阳离子间电子与电子、原子核与原子核间的相互排斥作用定义: 使阴阳离子结合成化合物的静电作用,叫做离子键。成键微粒:阴阳离子相互作用:静电作用(静电引力和斥力)成键过程:阴阳离子接近到某一定距离时,吸引和排斥达到平衡,就形成了离子键。含有离子键的化合物就是离子化合物。离子键 使阴阳离子结合成化合物的静电作用,叫 做离子键。思考 哪些物质能形成离子键? 活泼的金属元素(IA,IIA)和活泼的非金属
元素(VIA,VIIA)之间的化合物。 活泼的金属元素和酸根离子形成的盐 铵盐子和酸根离子(或活泼非金属元素)形成的盐。 在元素符号周围用“ · ”或“×”来表示
原子最外层电子的式子,叫电子式。H ·Na · ·Mg · ·Ca · 原子的电子式: 离子的电子式:H+Na+Mg2+Ca2+ ··(1)原子的电子式:常把其最外层电子数用小黑点“.”或小叉“×”来表示。(2)阳离子的电子式:不要求画出离子最外层电子数,只要在元素、符号右上角标出“n+”电荷字样。(3)阴离子的电子式:不但要画出最外层电子数,而且还应用于括号“[ ]”括起来,并在右上角标出“n·-”电荷字样。电子式 [ 练习] 写出下列微粒的电子式:
硫原子, 溴原子, 硫离子, 溴离子表示出原子之间是怎样结合的用 电子式 表示 离子化合物 的 形成过程 用电子式表示氯化钠的形成过程 用电子式表示溴化钙的形成过程 注意点1 离子须注明电荷数;2 相同的原子可以合并写,相同的离子要单个写;3.阴离子要用方括号括起;4.不能把 “→”写成 “ ==”5.用箭头表明电子转移方向(也可不标)离子化合物的电子式:由阴、阳离子的电子式组成,但对相同离子不能合并AB型AB2型A2B型[ 练习] ⑴ 用电子式表示氧化镁的形成过程 ⑵ 用电子式表示硫化钾的形成过程 箭头左方相同的微粒可以合并,
箭头右方相同的微粒不可以合并。注
意小结 使阴阳离子结合成化合物的静电作用,叫做离子键。 含有离子键的化合物一定是离子化合物区分: 用电子式表示物质
用电子式表示物质形成过程1.下列说法中正确的是 (??? )
A.两个原子或多个原子之间的相互作用叫做离子键。
B.阴、阳离子通过静电引力而形成的化学键叫做离子键。
C.只有金属元素和非金属元素化合时才能形成离子键。
D.大多数的盐、碱和低价金属氧化物中含有离子键。用电子式表示Na2S、MgBr2、Na2O
的形成过程
