《化学反应速率》教学设计案例(朱征 魏雯 陈懿)[下学期]
文档属性
| 名称 | 《化学反应速率》教学设计案例(朱征 魏雯 陈懿)[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 166.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-09-01 00:00:00 | ||
图片预览


文档简介
《化学反应速率》教学设计案例
朱征1 魏雯2 陈懿1
(1. 南京市外国语学校 2.南京师范大学化学教育研究所 江苏南京 210097)
一、教材分析与教学思路
1、教材分析
案例章节:《普通高中标准实验教科书(人教版)》必修②第二章化学反应与能量第三节化学反应的速率和限度(第一课时)
内容分析:化学反应速率是对教材前两节内容的拓展和完善,化学反应速率的学习也为后面反应限度知识奠定了基础。本节教材从日常生活中学生熟悉的化学现象入手,引出反应速率的概念。在此基础上通过实验探究,总结影响化学反应速率的因素。
教学方法:问题教学、分组协作学习、实验探究
2、教学思路与设计
学生通过一年多的化学学习,了解到不同的化学反应速率有快有慢,同一个化学反应在不同的外界条件影响下也可能速率不同,而且基本上能够用微粒的观点加以解释。本课时选择浓度这一影响因素为载体,教会学生从定性、定量的角度设计实验比较反应快慢的方法,在实验中培养学生的实验设计能力和小组合作意识,掌握从实验数据出发,建立数学图像、数学模型,进而从物质微观结构做出解释的化学问题的研究方法。
在传统的教学中,学生在整章学完之后,仅记住书本上几个具体的实验,而今后遇到新问题,很难独立设计实验进行探究。“授人以鱼,不如授人以渔”。如何在这节课上,调动学生的思维,从已有知识中搜索相关信息,总结、归纳出一些可行的比较反应速率的方法是这节课的关键。因此用“影响反应速率的外部因素有哪些?”“借助哪些实验现象可以帮助我们比较反应的快慢?”“设计实验获取数据,定量的比较反应的快慢?”三个层层深入的讨论题贯穿这节课,促进学生科学探究的方法的习得,而不仅仅是知识本身。
二、教学目标与流程
1、教学目的确定
知识与技能:了解影响化学反应速率的主要因素;了解常用的比较反应快慢的简便方法;通过实验认识到浓度对化学反应速率的影响,并能以粒子的观点初步解释。
过程与方法:能够设计简单实验方法测定浓度对化学反应速率的影响,掌握从实验数据出发,建立数学图像、数学模型,进而形成一个由简单到复杂、宏观到微观、定性到定量的科学探究过程。
情感态度与价值观:能体会到实验是化学学习的重要手段,培养科学探究意识和实事求是的科学精神。
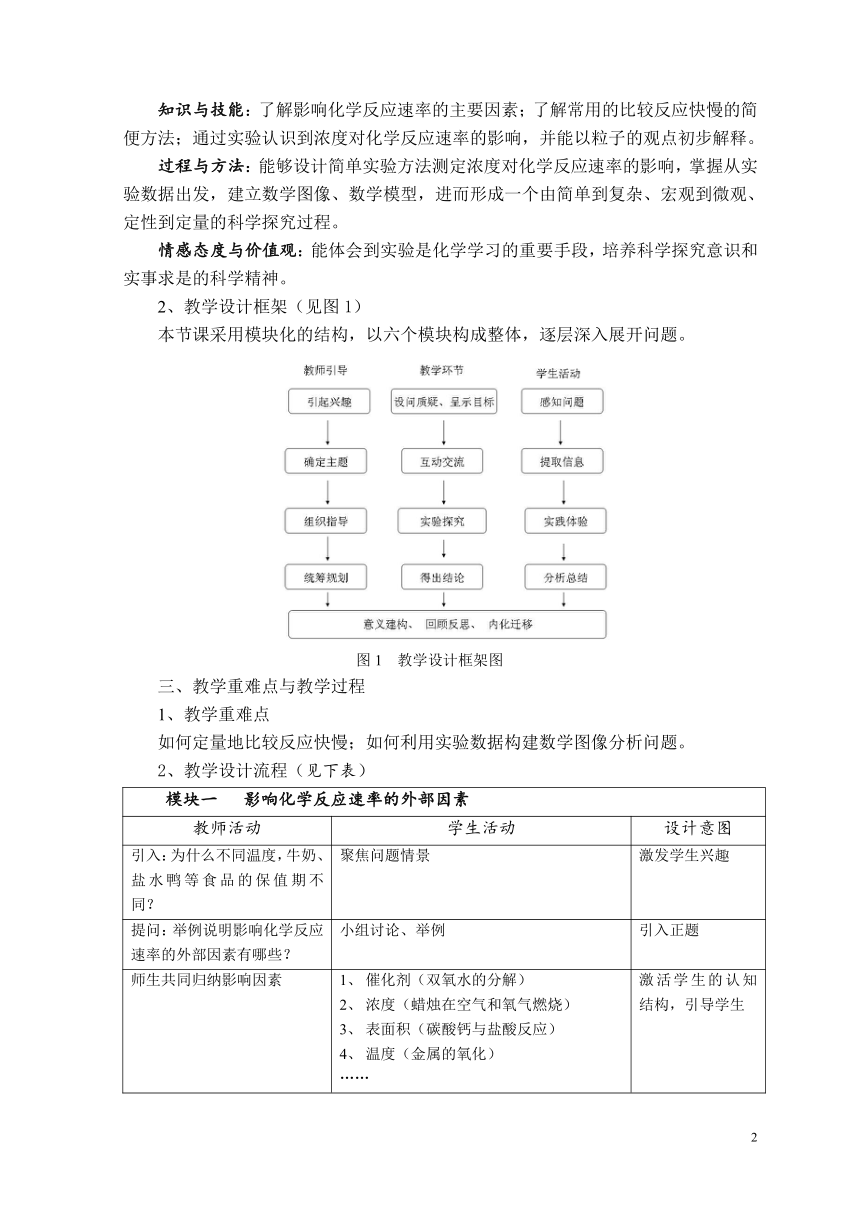
2、教学设计框架(见图1)
本节课采用模块化的结构,以六个模块构成整体,逐层深入展开问题。
图1 教学设计框架图
三、教学重难点与教学过程
1、教学重难点
如何定量地比较反应快慢;如何利用实验数据构建数学图像分析问题。
2、教学设计流程(见下表)
模块一 影响化学反应速率的外部因素
教师活动 学生活动 设计意图
引入:为什么不同温度,牛奶、盐水鸭等食品的保值期不同? 聚焦问题情景 激发学生兴趣
提问:举例说明影响化学反应速率的外部因素有哪些? 小组讨论、举例 引入正题
师生共同归纳影响因素 催化剂(双氧水的分解)浓度(蜡烛在空气和氧气燃烧)表面积(碳酸钙与盐酸反应)温度(金属的氧化)…… 激活学生的认知结构,引导学生
模块二 如何定性地比较反应快慢
教师活动 学生活动 设计意图
选择浓度进行探究提问:在探究浓度对反应速率影响时,借助哪些现象可以比较反应速度的快慢? 小组讨论、举例并总结在日常生活和化学实验过程中观察化学反应进行得快慢的方法 化学反应速率的定性观察
引导学生、拓宽思路 归纳总结:气泡多少,沉淀快慢,固体消失快慢,温度变化,颜色变化…… 为后面引出定量实验做铺垫
总结:比较反应的快慢,一般比较反应物消耗的快慢或者生成物增加的快慢。 内化、概括、建立概念体系
模块三 如何定量地比较反应快慢
教师活动 学生活动 设计意图
给予及时的评价和启发 小组讨论、交流:
针对镁条与不同浓度盐酸的反应,如何设计实验,通过数据,定量地比较反应的快慢? 思考、讨论、汇报1、测定单位时间内生成氢气的体积2、测定镁条消耗所需时间长短3、测定密闭容器内气压增加的快慢4、测定敞开体系质量减少的快慢…… 培养学生的思维发散能力与知识迁移运用能力
学生讨论、交流,提出疑问
密闭容器内气压增加的快慢实验演示(利用数据采集技术) 及时巩固
小结学生方案归纳常用实验方法①体系质量变化②生成气体体积③生成沉淀的量…… 提高知识的可利用性,将陈述性知识组织成程序性知识。
模块四 实验探究
教师活动 学生活动 设计意图
给出实验步骤方法 学生分组分工完成实验探究,记录数据,分析数据。利用所得数据,绘制曲线。 培养学生的实验动手能力、合作意识与数据分析处理能力
适时点评 学生以小组为单位,进行数据汇报
模块五 从微观角度解释
教师活动 学生活动 设计意图
提问:如何从微粒的角度解释这一结果? 学生积极思考 由宏观到微观,培养学生认识物质本质的科学探究方法
提问:还有什么因素会影响反应物微粒的碰撞几率? 思考、回答
演示Flash动画 观看、思考 多媒体辅助教学,促进学生对微观粒子的理解
模块六 评价与反思
教师活动 学生活动 设计意图
本实验中忽略了什么因素的影响? 学生回答 培养学生思考问题的严密性与实验评价能力
对学生在探究过程中的表现进行评价 集中注意,倾听 适时的评价强化学生参与的主动性
四、教学设计的思考
1、教学环节分析
设问质疑、呈示目标——笔者通过展示真实的图片(牛奶和咸水鸭的外包装),引出教学任务(化学反应速率),将学生的注意力都吸引到学习任务中来。通过温度条件的不同保存时间不同,使学生对此产生困惑(好奇)并对学习活动产生积极的兴趣和动机。当学生提出可能是温度影响了食品变质这样一个过程的速率时,笔者及时给予肯定,并马上提出“影响反应速率的因素还有哪些?”,激发学生的思考,导入下一个环节。
互动交流——教师是学生学习动机的激发者,是善于归纳问题的指导者,更是教学活动的调节者和组织者。策划好个别研究与集体讨论的步骤、节奏和深广度,在学习过程中培养学生的合作精神和创新精神,学生在问题情境中去“发现”问题,提出解决方案,从探究和讨论中掌握知识,获得发展。教师适时的激发学生的思考,让问题的讨论环环相扣,步步深入。
实验探究——这是引导学生深入学习的关键环节。实践出真知。本节课采用引导-发现教学模式,引导学生通过实验(镁条与不同浓度盐酸的反应),去观察、分析、研究,从而“发现”知识,探究规律;从生活实际中发现问题(牛奶、咸水鸭的外包装),通过设计,用实验去探究,用数据去分析,再用理论去论证,从而使问题获得解决。
得出结论—— 学生通过亲身经历的科学探究活动,在教师的引导下,得到正确的结论。以此为基础,构建数学图像分析问题(学生根据测得数据,绘制表格)。教师帮助学生将在探究阶段所构建的陈述性知识重新组织成有利于运用的程序性知识形式(师生共同归纳总结,把一般性知识概括成),建立并加强其与其他知识之间的联系,以便于将来的提取和使用。
总结与反思——在这节探究课的最后,教师和学生一起进行总结与反思。总结从两方面进行:一方面是学生在完成一阶段的探究活动后,反思这节课所做实验的严密性,还有哪些方面有待解决,比如,学生在探究实验结束之后,反思实验过程中,手握反应试管,会导致反应温度变化,影响实验结果。另一方面,教师依据整节课的环节,结合教材对全课及探究过程进行总结。
2、充分利用数据采集技术
数据采集技术具有方便、精确、细微化等优势,解决传统实验技术方法无法进行的或无法显示的实验或无法处理数据的实验,充分挖掘化学实验的资源价值,提高实验的探索性,使信息技术从学习对象转变为学习工具。例如,密闭容器内气压增加快慢的实验。利用计算机开发和控制化学演示实验过程,利用数、模转换技术和传感器使数字采集、分析和报告自动化、科学化,提高了演示实验效果和水平,为化学实验提供了一种新的计算机辅助教学模式。
运用数据采集技术不仅是改进教学的手段,而是改变学生的学习方式,开拓了学生的视野,大大扩展了学生思考设计实验方案的空间。进而促使学生自主学习,引发化学教学模式变革,为培养信息时代的接班人开辟了新的途径。
3、现代教学媒体与传统板书有机结合
现代教学媒体(Flash动画、PowerPoint)能把文字、声音、图像、动画等传媒集于一体,具有促思,激趣,高效等功能。吸引学生的注意,在发现学习教学中,充分利用多媒体手段可以收到事半功倍的效果。但传统的教学手段板书,也有着不可替代的作用,在教师提问、学生回答的过程中,教师的板书有助于学生倾听已有意见,在此基础上,发表自己的观点,师生共同完成教学过程。
4、小组协作学习,积极参与问题解决过程
引导-发现探究教学模式强调学生的积极参与,学习任务主要是通过学生自主探索和协作学习完成的。本节课采用小组协作的形式,一般由4人组成,各小组按照探究活动进行分工(记录、掐表、搭建仪器、操作),由小组成员共同完成一个研究课题。在探究过程中,小组成员既有分工,又有合作。学生要积极主动地利用各种信息工具获取、分析、处理信息,并在活动中学会与人交流、合作共同完成学习任务。
5、发展学生的思维品质
传统课上,老师的演示实验或是学生实验其实变成了验证性的实验。而笔者在英国进修期间,留意到英国中学在处理这一部分内容时,首先通过计算机辅助手段让学生了解有关化学反应中的微粒碰撞理论,然后在具体研究每一种因素时,都是采用学生实验得出结论,再尝试用碰撞理论解释,最后迁移运用。这样一种方式是一种真正的探究模式,学生从实验中形象的感知,再从理论中抽象的概括,符合学生的认知规律。
教师从学科领域和现实生活中选择主题,创设一种类似科学研究的情境,运用类似科学研究的办法,使学生主动探究问题,获得知识、技能、情感、态度的发展,促进学生创新意识、创新能力的提高。通过实验之后的反思,培养了学生思维的严密性,并对物质探究由定性到定量,由宏观到微观的科学认识方法。
附【学案】
浓度对化学反应速率的影响
实验用品:
镁条 砂纸 100cm3锥形瓶 橡皮塞(带直角导管) 30cm3注射器 铁架台(带铁夹) 量筒(50mL) 秒表
0.5 mol/L HCl 1 mol/L HCl
实验步骤(如右图):
1、 截取3cm镁条,用砂纸打磨掉表面氧化物
2、 组装好实验装置
3、 量取50 mL 0.5 mol/L HCl倒入锥形瓶中
4、 将镁条投入锥形瓶中,立刻塞好橡皮塞
5、 每隔5秒记录收集到氢气的体积,至第60秒
6、 清洗锥形瓶
7、 量取50 mL 1 mol/L HCl倒入锥形瓶中,重复上述实验
8、 将所得数据绘成曲线(时间为横坐标,气体体积为纵坐标)
数据记录:
时间(s) 体积(mL) 时间(s) 体积(mL)
5 35
10 40
15 45
20 50
25 55
30 60
实验结论: ;
理论解释: ;
收获体会: 。
2006年全国实验区高中化学新课程实施成果交流大会成果征集 稿 件
PAGE
5
朱征1 魏雯2 陈懿1
(1. 南京市外国语学校 2.南京师范大学化学教育研究所 江苏南京 210097)
一、教材分析与教学思路
1、教材分析
案例章节:《普通高中标准实验教科书(人教版)》必修②第二章化学反应与能量第三节化学反应的速率和限度(第一课时)
内容分析:化学反应速率是对教材前两节内容的拓展和完善,化学反应速率的学习也为后面反应限度知识奠定了基础。本节教材从日常生活中学生熟悉的化学现象入手,引出反应速率的概念。在此基础上通过实验探究,总结影响化学反应速率的因素。
教学方法:问题教学、分组协作学习、实验探究
2、教学思路与设计
学生通过一年多的化学学习,了解到不同的化学反应速率有快有慢,同一个化学反应在不同的外界条件影响下也可能速率不同,而且基本上能够用微粒的观点加以解释。本课时选择浓度这一影响因素为载体,教会学生从定性、定量的角度设计实验比较反应快慢的方法,在实验中培养学生的实验设计能力和小组合作意识,掌握从实验数据出发,建立数学图像、数学模型,进而从物质微观结构做出解释的化学问题的研究方法。
在传统的教学中,学生在整章学完之后,仅记住书本上几个具体的实验,而今后遇到新问题,很难独立设计实验进行探究。“授人以鱼,不如授人以渔”。如何在这节课上,调动学生的思维,从已有知识中搜索相关信息,总结、归纳出一些可行的比较反应速率的方法是这节课的关键。因此用“影响反应速率的外部因素有哪些?”“借助哪些实验现象可以帮助我们比较反应的快慢?”“设计实验获取数据,定量的比较反应的快慢?”三个层层深入的讨论题贯穿这节课,促进学生科学探究的方法的习得,而不仅仅是知识本身。
二、教学目标与流程
1、教学目的确定
知识与技能:了解影响化学反应速率的主要因素;了解常用的比较反应快慢的简便方法;通过实验认识到浓度对化学反应速率的影响,并能以粒子的观点初步解释。
过程与方法:能够设计简单实验方法测定浓度对化学反应速率的影响,掌握从实验数据出发,建立数学图像、数学模型,进而形成一个由简单到复杂、宏观到微观、定性到定量的科学探究过程。
情感态度与价值观:能体会到实验是化学学习的重要手段,培养科学探究意识和实事求是的科学精神。
2、教学设计框架(见图1)
本节课采用模块化的结构,以六个模块构成整体,逐层深入展开问题。
图1 教学设计框架图
三、教学重难点与教学过程
1、教学重难点
如何定量地比较反应快慢;如何利用实验数据构建数学图像分析问题。
2、教学设计流程(见下表)
模块一 影响化学反应速率的外部因素
教师活动 学生活动 设计意图
引入:为什么不同温度,牛奶、盐水鸭等食品的保值期不同? 聚焦问题情景 激发学生兴趣
提问:举例说明影响化学反应速率的外部因素有哪些? 小组讨论、举例 引入正题
师生共同归纳影响因素 催化剂(双氧水的分解)浓度(蜡烛在空气和氧气燃烧)表面积(碳酸钙与盐酸反应)温度(金属的氧化)…… 激活学生的认知结构,引导学生
模块二 如何定性地比较反应快慢
教师活动 学生活动 设计意图
选择浓度进行探究提问:在探究浓度对反应速率影响时,借助哪些现象可以比较反应速度的快慢? 小组讨论、举例并总结在日常生活和化学实验过程中观察化学反应进行得快慢的方法 化学反应速率的定性观察
引导学生、拓宽思路 归纳总结:气泡多少,沉淀快慢,固体消失快慢,温度变化,颜色变化…… 为后面引出定量实验做铺垫
总结:比较反应的快慢,一般比较反应物消耗的快慢或者生成物增加的快慢。 内化、概括、建立概念体系
模块三 如何定量地比较反应快慢
教师活动 学生活动 设计意图
给予及时的评价和启发 小组讨论、交流:
针对镁条与不同浓度盐酸的反应,如何设计实验,通过数据,定量地比较反应的快慢? 思考、讨论、汇报1、测定单位时间内生成氢气的体积2、测定镁条消耗所需时间长短3、测定密闭容器内气压增加的快慢4、测定敞开体系质量减少的快慢…… 培养学生的思维发散能力与知识迁移运用能力
学生讨论、交流,提出疑问
密闭容器内气压增加的快慢实验演示(利用数据采集技术) 及时巩固
小结学生方案归纳常用实验方法①体系质量变化②生成气体体积③生成沉淀的量…… 提高知识的可利用性,将陈述性知识组织成程序性知识。
模块四 实验探究
教师活动 学生活动 设计意图
给出实验步骤方法 学生分组分工完成实验探究,记录数据,分析数据。利用所得数据,绘制曲线。 培养学生的实验动手能力、合作意识与数据分析处理能力
适时点评 学生以小组为单位,进行数据汇报
模块五 从微观角度解释
教师活动 学生活动 设计意图
提问:如何从微粒的角度解释这一结果? 学生积极思考 由宏观到微观,培养学生认识物质本质的科学探究方法
提问:还有什么因素会影响反应物微粒的碰撞几率? 思考、回答
演示Flash动画 观看、思考 多媒体辅助教学,促进学生对微观粒子的理解
模块六 评价与反思
教师活动 学生活动 设计意图
本实验中忽略了什么因素的影响? 学生回答 培养学生思考问题的严密性与实验评价能力
对学生在探究过程中的表现进行评价 集中注意,倾听 适时的评价强化学生参与的主动性
四、教学设计的思考
1、教学环节分析
设问质疑、呈示目标——笔者通过展示真实的图片(牛奶和咸水鸭的外包装),引出教学任务(化学反应速率),将学生的注意力都吸引到学习任务中来。通过温度条件的不同保存时间不同,使学生对此产生困惑(好奇)并对学习活动产生积极的兴趣和动机。当学生提出可能是温度影响了食品变质这样一个过程的速率时,笔者及时给予肯定,并马上提出“影响反应速率的因素还有哪些?”,激发学生的思考,导入下一个环节。
互动交流——教师是学生学习动机的激发者,是善于归纳问题的指导者,更是教学活动的调节者和组织者。策划好个别研究与集体讨论的步骤、节奏和深广度,在学习过程中培养学生的合作精神和创新精神,学生在问题情境中去“发现”问题,提出解决方案,从探究和讨论中掌握知识,获得发展。教师适时的激发学生的思考,让问题的讨论环环相扣,步步深入。
实验探究——这是引导学生深入学习的关键环节。实践出真知。本节课采用引导-发现教学模式,引导学生通过实验(镁条与不同浓度盐酸的反应),去观察、分析、研究,从而“发现”知识,探究规律;从生活实际中发现问题(牛奶、咸水鸭的外包装),通过设计,用实验去探究,用数据去分析,再用理论去论证,从而使问题获得解决。
得出结论—— 学生通过亲身经历的科学探究活动,在教师的引导下,得到正确的结论。以此为基础,构建数学图像分析问题(学生根据测得数据,绘制表格)。教师帮助学生将在探究阶段所构建的陈述性知识重新组织成有利于运用的程序性知识形式(师生共同归纳总结,把一般性知识概括成),建立并加强其与其他知识之间的联系,以便于将来的提取和使用。
总结与反思——在这节探究课的最后,教师和学生一起进行总结与反思。总结从两方面进行:一方面是学生在完成一阶段的探究活动后,反思这节课所做实验的严密性,还有哪些方面有待解决,比如,学生在探究实验结束之后,反思实验过程中,手握反应试管,会导致反应温度变化,影响实验结果。另一方面,教师依据整节课的环节,结合教材对全课及探究过程进行总结。
2、充分利用数据采集技术
数据采集技术具有方便、精确、细微化等优势,解决传统实验技术方法无法进行的或无法显示的实验或无法处理数据的实验,充分挖掘化学实验的资源价值,提高实验的探索性,使信息技术从学习对象转变为学习工具。例如,密闭容器内气压增加快慢的实验。利用计算机开发和控制化学演示实验过程,利用数、模转换技术和传感器使数字采集、分析和报告自动化、科学化,提高了演示实验效果和水平,为化学实验提供了一种新的计算机辅助教学模式。
运用数据采集技术不仅是改进教学的手段,而是改变学生的学习方式,开拓了学生的视野,大大扩展了学生思考设计实验方案的空间。进而促使学生自主学习,引发化学教学模式变革,为培养信息时代的接班人开辟了新的途径。
3、现代教学媒体与传统板书有机结合
现代教学媒体(Flash动画、PowerPoint)能把文字、声音、图像、动画等传媒集于一体,具有促思,激趣,高效等功能。吸引学生的注意,在发现学习教学中,充分利用多媒体手段可以收到事半功倍的效果。但传统的教学手段板书,也有着不可替代的作用,在教师提问、学生回答的过程中,教师的板书有助于学生倾听已有意见,在此基础上,发表自己的观点,师生共同完成教学过程。
4、小组协作学习,积极参与问题解决过程
引导-发现探究教学模式强调学生的积极参与,学习任务主要是通过学生自主探索和协作学习完成的。本节课采用小组协作的形式,一般由4人组成,各小组按照探究活动进行分工(记录、掐表、搭建仪器、操作),由小组成员共同完成一个研究课题。在探究过程中,小组成员既有分工,又有合作。学生要积极主动地利用各种信息工具获取、分析、处理信息,并在活动中学会与人交流、合作共同完成学习任务。
5、发展学生的思维品质
传统课上,老师的演示实验或是学生实验其实变成了验证性的实验。而笔者在英国进修期间,留意到英国中学在处理这一部分内容时,首先通过计算机辅助手段让学生了解有关化学反应中的微粒碰撞理论,然后在具体研究每一种因素时,都是采用学生实验得出结论,再尝试用碰撞理论解释,最后迁移运用。这样一种方式是一种真正的探究模式,学生从实验中形象的感知,再从理论中抽象的概括,符合学生的认知规律。
教师从学科领域和现实生活中选择主题,创设一种类似科学研究的情境,运用类似科学研究的办法,使学生主动探究问题,获得知识、技能、情感、态度的发展,促进学生创新意识、创新能力的提高。通过实验之后的反思,培养了学生思维的严密性,并对物质探究由定性到定量,由宏观到微观的科学认识方法。
附【学案】
浓度对化学反应速率的影响
实验用品:
镁条 砂纸 100cm3锥形瓶 橡皮塞(带直角导管) 30cm3注射器 铁架台(带铁夹) 量筒(50mL) 秒表
0.5 mol/L HCl 1 mol/L HCl
实验步骤(如右图):
1、 截取3cm镁条,用砂纸打磨掉表面氧化物
2、 组装好实验装置
3、 量取50 mL 0.5 mol/L HCl倒入锥形瓶中
4、 将镁条投入锥形瓶中,立刻塞好橡皮塞
5、 每隔5秒记录收集到氢气的体积,至第60秒
6、 清洗锥形瓶
7、 量取50 mL 1 mol/L HCl倒入锥形瓶中,重复上述实验
8、 将所得数据绘成曲线(时间为横坐标,气体体积为纵坐标)
数据记录:
时间(s) 体积(mL) 时间(s) 体积(mL)
5 35
10 40
15 45
20 50
25 55
30 60
实验结论: ;
理论解释: ;
收获体会: 。
2006年全国实验区高中化学新课程实施成果交流大会成果征集 稿 件
PAGE
5
