电离平衡[上学期]
图片预览








文档简介
课件26张PPT。电离平衡南京市六合区瓜埠高级中学 陈大春电解质非电解质化合物纯净物物 质混合物单 质一、强、弱电解质与结构的关系强电解质
弱电解质1.电解质和非电解质:电解质:非电解质:在水溶液里或熔融状态下,能够导电的化合物。在水溶液里或熔融状态下,都不能导电的化合物。包括:多数有机物、非金属氧化物等。
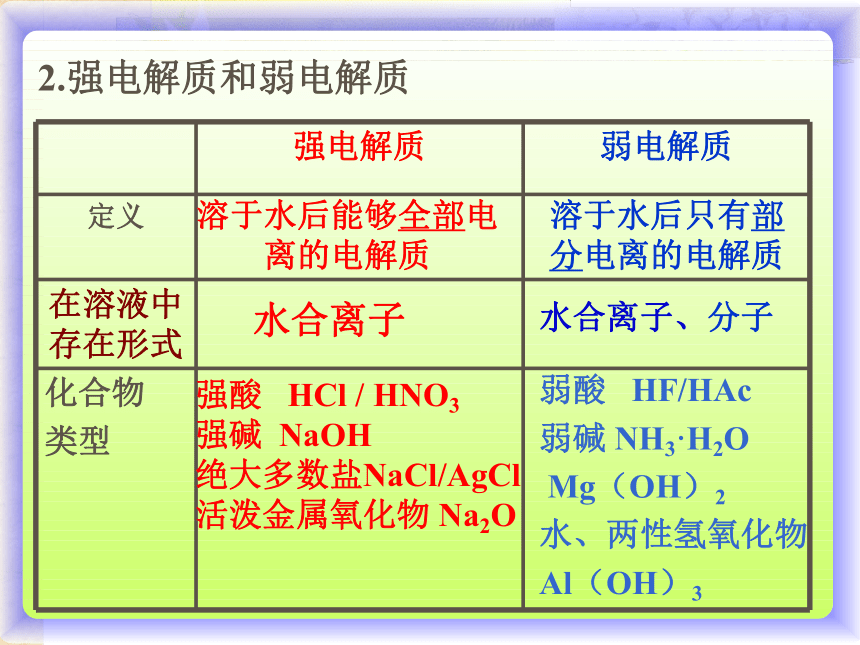
------ 蔗糖、酒精溶于水后能够全部电离的电解质溶于水后只有部分电离的电解质水合离子水合离子、分子强酸 HCl / HNO3
强碱 NaOH
绝大多数盐NaCl/AgCl
活泼金属氧化物 Na2O弱酸 HF/HAc
弱碱 NH3·H2O
Mg(OH)2
水、两性氢氧化物
Al(OH)32.强电解质和弱电解质离子化合物,某些含极性键的共价化合物另一部分含有极性键的共价化合物完全电离部分电离不可逆过程,无电离平衡可逆过程,存在电离平衡思考题1、SO2、NH3、Cl2的水溶液均能导电,它们是电解质吗?怎样区分电解质与非电解质?某些离子化合物(如Na2O、Na2O2、CaO)溶于水后电离出的离子并非其自身的,它们却属于电解质,为什么?电解质、非电解质的区分看水溶液或熔融状态下能否导电。(真正电离出自由移动的离子的物质才是电解质)强调与辨析思考题2、CaCO3、Fe(OH)3的溶解度都很小, CaCO3属于强电解质,而Fe(OH)3属于弱电解质;CH3COOH、HCl的溶解度都很大, HCl属于强电解质,而CH3COOH 属于弱电解质。电解质的强弱与其溶解性有何关系?怎样区分强弱电解质?强弱电解质的区分依据不是看该物质水溶性的大小,也不是看其水溶液导电能力的强弱,而是看电离的是否完全.3.强电解质在结构上属于共价化合物的,它所含有的共价键一定是强极性共价键,对吗?思考题不对 比如 HF4、溶液导电性强弱与电解质强弱的关系。下列物质能导电的是______,属于强电解质的是______,属于弱电解质的是________,属于非电解质的是_______.
a.铜丝 b.金刚石 c.石墨 d.NaCl e.盐酸 f.蔗糖 g.CO2 h.Na2O i.硬脂酸 j.醋酸 k.碳酸 l.碳酸氢铵 m.氢氧化铝 n.氯气 O. BaSO4 a.c.e.d.h.l.Oi.j.k.m.f.g.二、弱电解质的电离平衡1.定义: 在一定条件(如温度、浓度)下,当电解质分子电离成离子的速率和离子重新结合生成分子的速率相等时,电离过程就达到了平衡状态,这叫做电离平衡。电离速率=分子化速率逆、等、动、定、变2.弱电解质电离平衡的特征意义:特征:反应速率时间弱电解质分子电离成离子的速率离子结合成弱电解质分子的速率两种速率相等,处于电离平衡状态3.外界条件对电离平衡的影响:1)温度:电离是吸热过程温度升高,电离平衡正向移动2)浓度:在0.1mol/L氨水中存在电离平衡:NH3·H2O
NH4++OH-- —热,改变下列条件按要求填空:问题探讨弱电解质加水稀释时,离子浓度______? (填变大、变小、不变或不能确定) 不能确定 画出用水稀释冰醋酸时离子浓度随加水量的变化曲线。氢硫酸中存在的电离平衡是_____________;
1)当加入CuSO4溶液时,电离平衡____移动,c(S2-)____ c(H+)____;
2)当加入固体NaOH时,电离平衡____移动,c(S2-)____ c(H+)____;
3)若将溶液加热至沸腾,c(H2S)______4.电离方程式的正确书写 总结: 强等号、弱可逆、多元弱酸分步写
多元弱碱一步完(1)H2SO4(2)BaSO4(3) HClO
(4) Al(OH)3 (5) H3PO4
(6)NaHSO4 (7)NaHCO3练习一写出下列物质的电离方程式
(1) HClO
(2) KHSO4
(3) CaCO3
(4) Cu(OH)2H++ClO-=K++H++SO42-=Ca2++CO32-Cu2++2OH-练习二 下列电离方程式书写正确的是( )
A. BaSO4 Ba2++SO42-
B. H3PO4 3H++PO43-
C. Al(OH)3 H++AlO2-+H2O
D. NaHS = Na++H++S2-
C离子方程式书写练习:
1.醋酸和氨水:
2.氢氧化镁溶于硝酸:
3.碳酸氢钠溶液与过量氢氧化钡溶液:
4.磷酸与过量澄清石灰水:
5.氯化铝与过量烧碱溶液:
6.硫氢化钠溶液中加入硫酸铜溶液:1. 有H+浓度相同、体积相等的三种酸:a、盐酸 b、硫酸 c、醋酸,同时加入足量的锌,则开始反应时速率______,反应完全后生成H2的质量_________。(用<、=、> 表示)a=b=ca=b下列说法不正确的是( )
A.c(H+)相同时,物质的量浓度③ >①> ②
B. c(H+)相同时,分别稀释10倍, c(H+)仍相等
C .物质的量浓度相同时, c(H+)是 ② > ①> ③
D.c(酸)和体积V相同时,中和碱的能力② > ①> ③
BD3.0.1mol/L氢硫酸溶液中加水稀释至0.01 mol/L时,下列微粒的物质的量浓度减少最多的是( )
A.H2S B.HS-- C.H+ D.S2--A4.将体积都为10mL,c(H+)都等于10-2mol/L的醋酸和盐酸加水稀释至amL和bmL,测得稀释后的c(H+)都等于10-5mol/L,则稀释后的体积为( )A.a=b=100mL B.a=b=1000mL C.abD5.H3PO4溶液中存在的电离平衡有______________,离子浓度排序依次是_______________;当向H3PO4溶液中通入HCl,c(H+)_____,c(PO43-)______;
当向H3PO4溶液中加入少量固体烧碱时,c(H+)_____,c(PO43-)______6.把0.05molNaOH固体分别加入下列100mL液体中,溶液导电性变化最小的是( )
A.自来水 B.0.5mol/L盐酸
C . 0.5mol/L醋酸 D. 0.5mol/L氢氟酸
E. 0.5mol/LNH4ClB7.下图中能正确表示饱和H2S溶液中通入过量SO2后溶液导电情况的是( )DABCD再 见
弱电解质1.电解质和非电解质:电解质:非电解质:在水溶液里或熔融状态下,能够导电的化合物。在水溶液里或熔融状态下,都不能导电的化合物。包括:多数有机物、非金属氧化物等。
------ 蔗糖、酒精溶于水后能够全部电离的电解质溶于水后只有部分电离的电解质水合离子水合离子、分子强酸 HCl / HNO3
强碱 NaOH
绝大多数盐NaCl/AgCl
活泼金属氧化物 Na2O弱酸 HF/HAc
弱碱 NH3·H2O
Mg(OH)2
水、两性氢氧化物
Al(OH)32.强电解质和弱电解质离子化合物,某些含极性键的共价化合物另一部分含有极性键的共价化合物完全电离部分电离不可逆过程,无电离平衡可逆过程,存在电离平衡思考题1、SO2、NH3、Cl2的水溶液均能导电,它们是电解质吗?怎样区分电解质与非电解质?某些离子化合物(如Na2O、Na2O2、CaO)溶于水后电离出的离子并非其自身的,它们却属于电解质,为什么?电解质、非电解质的区分看水溶液或熔融状态下能否导电。(真正电离出自由移动的离子的物质才是电解质)强调与辨析思考题2、CaCO3、Fe(OH)3的溶解度都很小, CaCO3属于强电解质,而Fe(OH)3属于弱电解质;CH3COOH、HCl的溶解度都很大, HCl属于强电解质,而CH3COOH 属于弱电解质。电解质的强弱与其溶解性有何关系?怎样区分强弱电解质?强弱电解质的区分依据不是看该物质水溶性的大小,也不是看其水溶液导电能力的强弱,而是看电离的是否完全.3.强电解质在结构上属于共价化合物的,它所含有的共价键一定是强极性共价键,对吗?思考题不对 比如 HF4、溶液导电性强弱与电解质强弱的关系。下列物质能导电的是______,属于强电解质的是______,属于弱电解质的是________,属于非电解质的是_______.
a.铜丝 b.金刚石 c.石墨 d.NaCl e.盐酸 f.蔗糖 g.CO2 h.Na2O i.硬脂酸 j.醋酸 k.碳酸 l.碳酸氢铵 m.氢氧化铝 n.氯气 O. BaSO4 a.c.e.d.h.l.Oi.j.k.m.f.g.二、弱电解质的电离平衡1.定义: 在一定条件(如温度、浓度)下,当电解质分子电离成离子的速率和离子重新结合生成分子的速率相等时,电离过程就达到了平衡状态,这叫做电离平衡。电离速率=分子化速率逆、等、动、定、变2.弱电解质电离平衡的特征意义:特征:反应速率时间弱电解质分子电离成离子的速率离子结合成弱电解质分子的速率两种速率相等,处于电离平衡状态3.外界条件对电离平衡的影响:1)温度:电离是吸热过程温度升高,电离平衡正向移动2)浓度:在0.1mol/L氨水中存在电离平衡:NH3·H2O
NH4++OH-- —热,改变下列条件按要求填空:问题探讨弱电解质加水稀释时,离子浓度______? (填变大、变小、不变或不能确定) 不能确定 画出用水稀释冰醋酸时离子浓度随加水量的变化曲线。氢硫酸中存在的电离平衡是_____________;
1)当加入CuSO4溶液时,电离平衡____移动,c(S2-)____ c(H+)____;
2)当加入固体NaOH时,电离平衡____移动,c(S2-)____ c(H+)____;
3)若将溶液加热至沸腾,c(H2S)______4.电离方程式的正确书写 总结: 强等号、弱可逆、多元弱酸分步写
多元弱碱一步完(1)H2SO4(2)BaSO4(3) HClO
(4) Al(OH)3 (5) H3PO4
(6)NaHSO4 (7)NaHCO3练习一写出下列物质的电离方程式
(1) HClO
(2) KHSO4
(3) CaCO3
(4) Cu(OH)2H++ClO-=K++H++SO42-=Ca2++CO32-Cu2++2OH-练习二 下列电离方程式书写正确的是( )
A. BaSO4 Ba2++SO42-
B. H3PO4 3H++PO43-
C. Al(OH)3 H++AlO2-+H2O
D. NaHS = Na++H++S2-
C离子方程式书写练习:
1.醋酸和氨水:
2.氢氧化镁溶于硝酸:
3.碳酸氢钠溶液与过量氢氧化钡溶液:
4.磷酸与过量澄清石灰水:
5.氯化铝与过量烧碱溶液:
6.硫氢化钠溶液中加入硫酸铜溶液:1. 有H+浓度相同、体积相等的三种酸:a、盐酸 b、硫酸 c、醋酸,同时加入足量的锌,则开始反应时速率______,反应完全后生成H2的质量_________。(用<、=、> 表示)a=b=ca=b
A.c(H+)相同时,物质的量浓度③ >①> ②
B. c(H+)相同时,分别稀释10倍, c(H+)仍相等
C .物质的量浓度相同时, c(H+)是 ② > ①> ③
D.c(酸)和体积V相同时,中和碱的能力② > ①> ③
BD3.0.1mol/L氢硫酸溶液中加水稀释至0.01 mol/L时,下列微粒的物质的量浓度减少最多的是( )
A.H2S B.HS-- C.H+ D.S2--A4.将体积都为10mL,c(H+)都等于10-2mol/L的醋酸和盐酸加水稀释至amL和bmL,测得稀释后的c(H+)都等于10-5mol/L,则稀释后的体积为( )A.a=b=100mL B.a=b=1000mL C.abD5.H3PO4溶液中存在的电离平衡有______________,离子浓度排序依次是_______________;当向H3PO4溶液中通入HCl,c(H+)_____,c(PO43-)______;
当向H3PO4溶液中加入少量固体烧碱时,c(H+)_____,c(PO43-)______6.把0.05molNaOH固体分别加入下列100mL液体中,溶液导电性变化最小的是( )
A.自来水 B.0.5mol/L盐酸
C . 0.5mol/L醋酸 D. 0.5mol/L氢氟酸
E. 0.5mol/LNH4ClB7.下图中能正确表示饱和H2S溶液中通入过量SO2后溶液导电情况的是( )DABCD再 见
