化学能与电能[下学期]
图片预览





文档简介
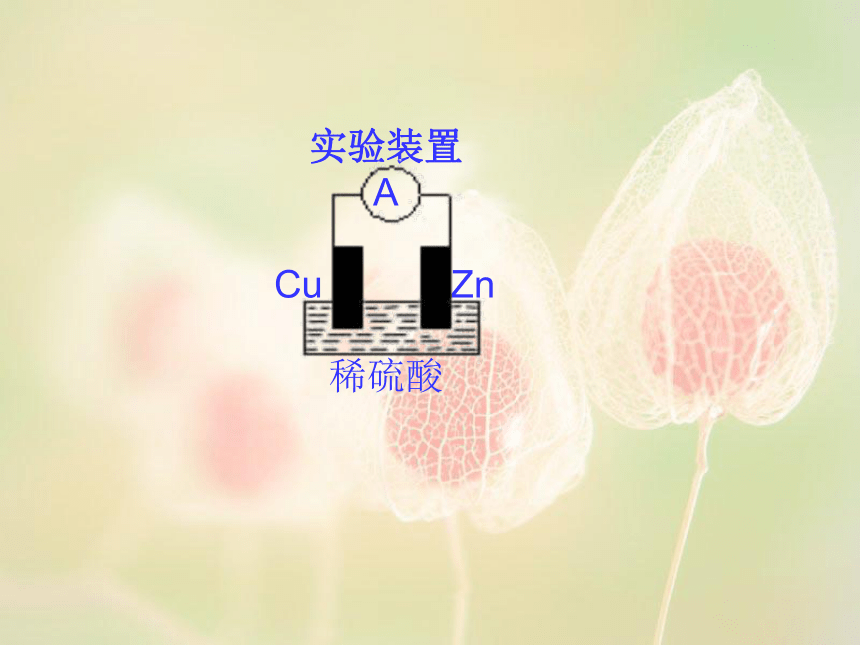
课件15张PPT。化 学 能 与 电 能揭东县第一中学 袁妙君化学反应常伴有能量的变化,能量有哪些转换(或传递)的形式?化学能可转化为热能、光能和电能等讨论:分析图2—8,谈谈火力发电的工作原理,并指出其利与弊;针对其存在的问题,你有什么新的想法?思考:1.火力发电有没有利用氧化还原反应,电子转移的情况怎样?2.电子的定向移动形成电流,我们能否在氧化剂与还原剂之间架设桥梁,将电子移动过程中产生的电流利用起来?3.若要实现上述想法,你能否用铜片、锌片、稀硫酸、电流表等设计一个看能否产生电流的装置,画出其装置图。实验装置
A
Cu Zn
稀硫酸
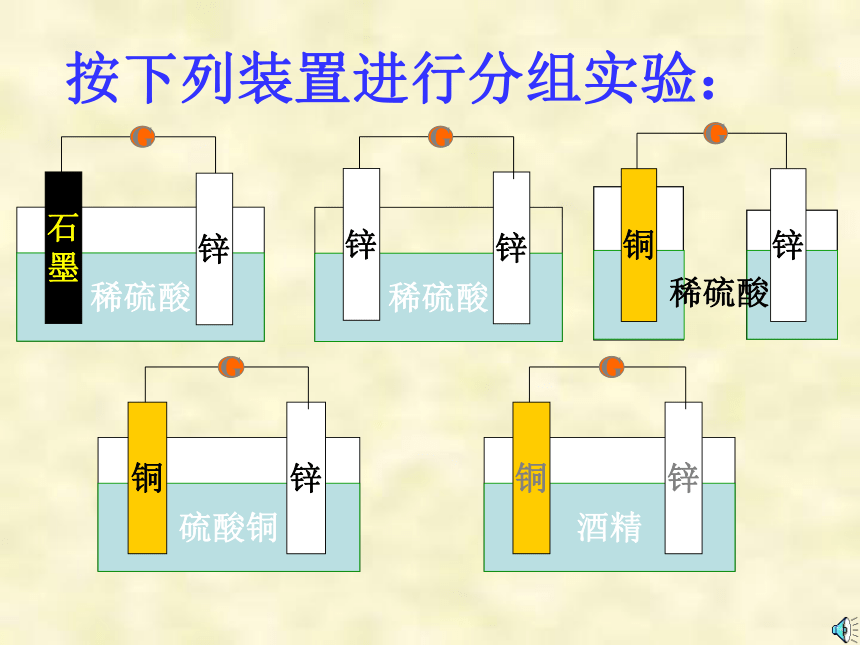
思考与交流:1.铜片表面有气泡产生,该气体是什么?如何检验?2.既然铜片上产生的是氢气,哪么H+得到的电子是铜失去的还是锌失去的?如何检验?请设计出你的实验方案。方案1:称量实验前后铜片或锌片的质量。方案2:观察溶液的颜色,看有无Cu2+生成按下列装置进行分组实验:稀硫酸1.原电池:将化学能转化为电能的装置。讨论:根据物理学的知识,如何确定Cu、Zn、稀硫酸组成原电池的正、负极?填表:Zn片Cu片Zn – 2e-=Zn2+2H+ + 2e-=H2↑氧 化
反 应还 原
反 应Zn片→Cu片Zn片→Cu片电 极负 极正 极电 极
材 料电 极 反 应反 应
类 型电 子 流
动 方 向思考与交流:从刚才的分组实验中,你能归纳出组成原电池的条件有哪些?2.组成原电池的条件:1.有两种活泼性不同的金属(或一种是非金属导体)作电极。2.电极材料均插入电解质溶液中。3.两电极相连形成闭合电路。活动设计:选用日常生活中你能找到的材料,自己设计并制作原电池,并探究你依据什么现象说明你的设计是成功的。练习:请结合组成原电池的条件,将氧化还原反应:
Fe + Cu2+ = Cu + Fe2+ 设计成一个原电池。1.电解液:____
2.电极材料: 负极____
正极____
3.电极反应式:
负极___________。
正极___________。
谢 谢 大 家
A
Cu Zn
稀硫酸
思考与交流:1.铜片表面有气泡产生,该气体是什么?如何检验?2.既然铜片上产生的是氢气,哪么H+得到的电子是铜失去的还是锌失去的?如何检验?请设计出你的实验方案。方案1:称量实验前后铜片或锌片的质量。方案2:观察溶液的颜色,看有无Cu2+生成按下列装置进行分组实验:稀硫酸1.原电池:将化学能转化为电能的装置。讨论:根据物理学的知识,如何确定Cu、Zn、稀硫酸组成原电池的正、负极?填表:Zn片Cu片Zn – 2e-=Zn2+2H+ + 2e-=H2↑氧 化
反 应还 原
反 应Zn片→Cu片Zn片→Cu片电 极负 极正 极电 极
材 料电 极 反 应反 应
类 型电 子 流
动 方 向思考与交流:从刚才的分组实验中,你能归纳出组成原电池的条件有哪些?2.组成原电池的条件:1.有两种活泼性不同的金属(或一种是非金属导体)作电极。2.电极材料均插入电解质溶液中。3.两电极相连形成闭合电路。活动设计:选用日常生活中你能找到的材料,自己设计并制作原电池,并探究你依据什么现象说明你的设计是成功的。练习:请结合组成原电池的条件,将氧化还原反应:
Fe + Cu2+ = Cu + Fe2+ 设计成一个原电池。1.电解液:____
2.电极材料: 负极____
正极____
3.电极反应式:
负极___________。
正极___________。
谢 谢 大 家
