化学能与热能[下学期]
图片预览



文档简介
课件13张PPT。第一节 化学能与热能第二章 化学反应与能量化学键:
相邻微粒间的强烈的相互作用。一、化学键与化学反应中能量变化的关系1、当物质发生化学反应时,断开反应物中的化学键要吸收能量;而形成生成物中的化学键要放出能量。
如:1mol H2中含有1molH-H,在250C 101kPa条件下,由H原子形成1molH-H要放出436kJ的能量,而断开1molH-H重新变为H原子要吸收436kJ的能量
又如:1mol CH4中含有4molC-H,在250C 101kPa条件下,断开1molC-H要吸收415kJ的能量,断开1molCH4要吸收4mol×415kJ/mol=1660kJ
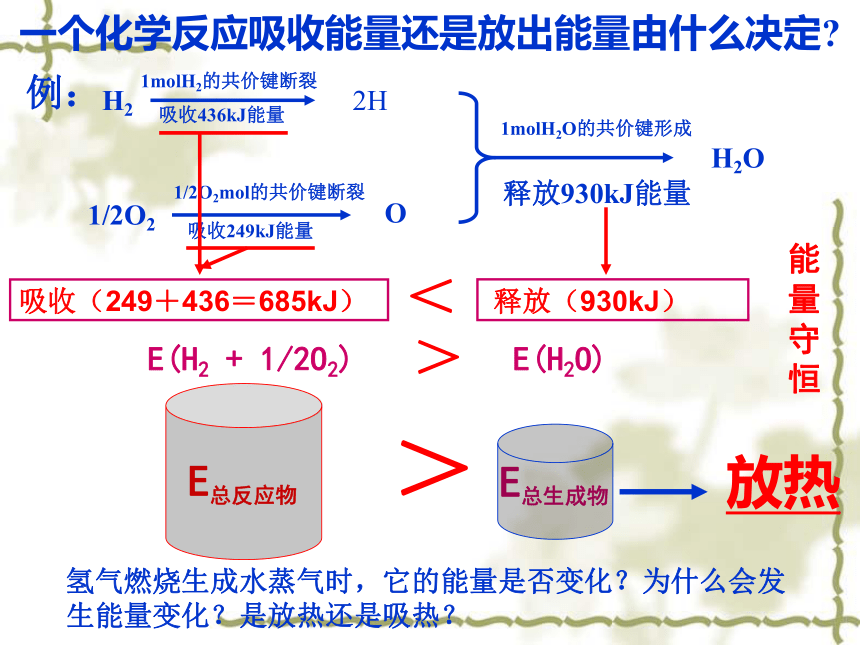
氢气燃烧生成水蒸气时,它的能量是否变化?为什么会发生能量变化?是放热还是吸热?一个化学反应吸收能量还是放出能量由什么决定?
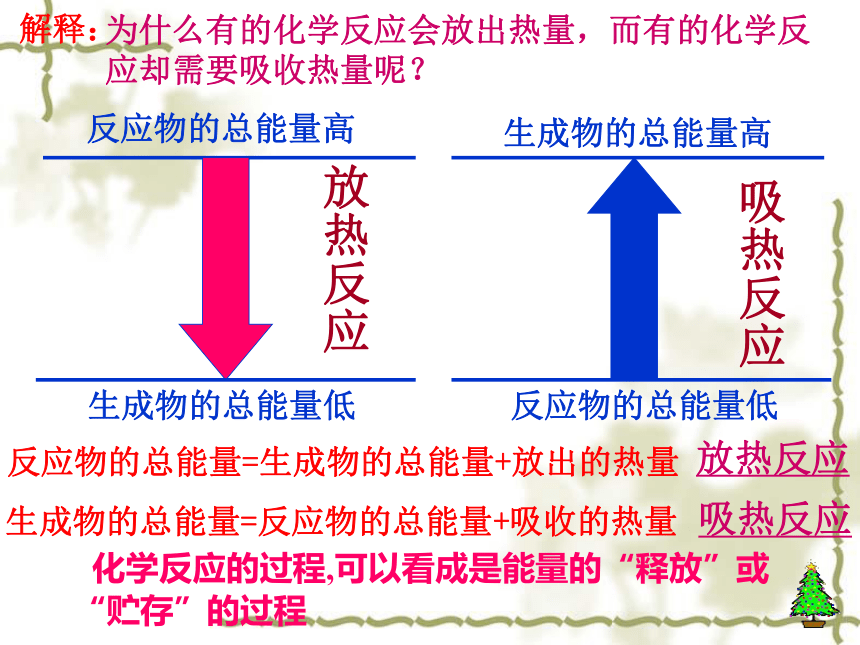
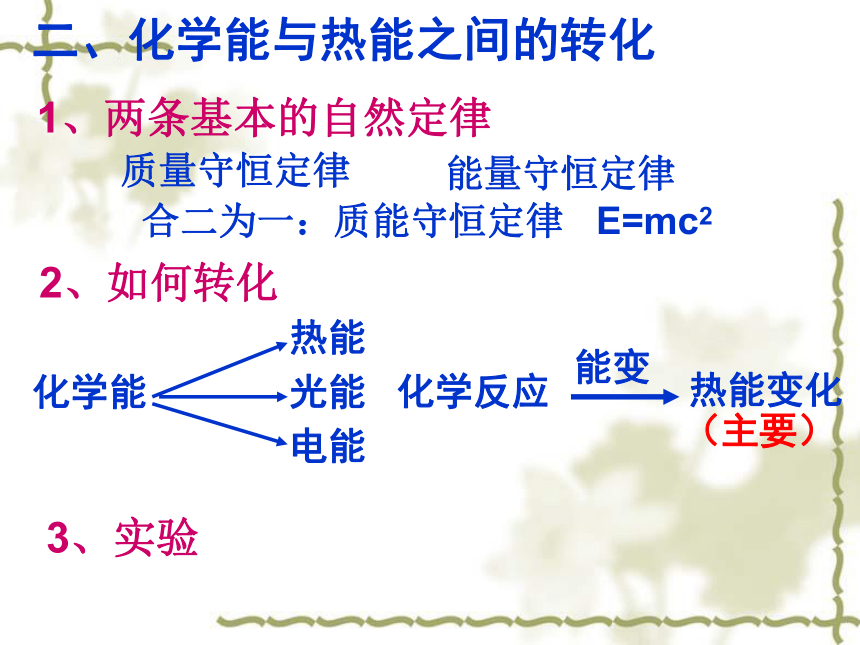
例:E(H2O)E(H2 + 1/2O2)>能量守恒<>放热放热反应吸热反应反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量 化学反应的过程,可以看成是能量的“释放”或“贮存”的过程放热反应吸热反应二、化学能与热能之间的转化1、两条基本的自然定律质量守恒定律能量守恒定律合二为一:质能守恒定律 E=mc22、如何转化化学能热能电能光能化学反应能变3、实验实验2-1锌与盐酸反应,放出大量气泡,
温度升高该反应是
放热反应现象:1、玻璃片会与小坩埚粘结在一起
2、有少许刺激性气味气体产生
3、混合物变成糊状
4、 小坩埚变凉了实验2-2结论:该反应是吸热反应实验2-3反应后温度升高结论:中和反应是放热反应。中和热:参考《三点一册》自学常见的吸热、放热反应:放热
反应酸碱中和:HCl+NaOH=NaCl+H2O所有的燃烧反应:C + O2 =CO2酸与金属反应:Zn+2HCl=ZnCl2+H2↑吸热
反应大多数分解反应:Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O一般能自发进行一般不能自发进行大多数的化合反应:CaO+H2O=Ca(OH)2以H2、CO、C为还原剂的还原金属氧化物的氧化还原反应科学视野2、社会发展与能源利用3、人类利用能源的三个阶段柴草时期化石能源时期多能源结构时期1、生物体内的能量转化小结练习1:下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了反应
结果是放热还是吸热
D.吸热反应在一定条件下也能发生反应CD12g石墨与O2反应生成CO2放出393.51kJ热量;
12g金刚石与O2反应生成CO2放出395.41kJ热量,试比较,石墨与金刚石哪个稳定?比较相同状态、相同数量的金刚石和石墨,与O2完全反应,生成相同状态、相同数量的CO2,金刚石释放出的热量更多,说明金刚石具有的总能量高,没有石墨稳定练习2:作业:1、P33 第1、2、3、4、6做在书上
2、第5、7题做在作业本上
3、《三点一册》
相邻微粒间的强烈的相互作用。一、化学键与化学反应中能量变化的关系1、当物质发生化学反应时,断开反应物中的化学键要吸收能量;而形成生成物中的化学键要放出能量。
如:1mol H2中含有1molH-H,在250C 101kPa条件下,由H原子形成1molH-H要放出436kJ的能量,而断开1molH-H重新变为H原子要吸收436kJ的能量
又如:1mol CH4中含有4molC-H,在250C 101kPa条件下,断开1molC-H要吸收415kJ的能量,断开1molCH4要吸收4mol×415kJ/mol=1660kJ
氢气燃烧生成水蒸气时,它的能量是否变化?为什么会发生能量变化?是放热还是吸热?一个化学反应吸收能量还是放出能量由什么决定?
例:E(H2O)E(H2 + 1/2O2)>能量守恒<>放热放热反应吸热反应反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量 化学反应的过程,可以看成是能量的“释放”或“贮存”的过程放热反应吸热反应二、化学能与热能之间的转化1、两条基本的自然定律质量守恒定律能量守恒定律合二为一:质能守恒定律 E=mc22、如何转化化学能热能电能光能化学反应能变3、实验实验2-1锌与盐酸反应,放出大量气泡,
温度升高该反应是
放热反应现象:1、玻璃片会与小坩埚粘结在一起
2、有少许刺激性气味气体产生
3、混合物变成糊状
4、 小坩埚变凉了实验2-2结论:该反应是吸热反应实验2-3反应后温度升高结论:中和反应是放热反应。中和热:参考《三点一册》自学常见的吸热、放热反应:放热
反应酸碱中和:HCl+NaOH=NaCl+H2O所有的燃烧反应:C + O2 =CO2酸与金属反应:Zn+2HCl=ZnCl2+H2↑吸热
反应大多数分解反应:Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O一般能自发进行一般不能自发进行大多数的化合反应:CaO+H2O=Ca(OH)2以H2、CO、C为还原剂的还原金属氧化物的氧化还原反应科学视野2、社会发展与能源利用3、人类利用能源的三个阶段柴草时期化石能源时期多能源结构时期1、生物体内的能量转化小结练习1:下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了反应
结果是放热还是吸热
D.吸热反应在一定条件下也能发生反应CD12g石墨与O2反应生成CO2放出393.51kJ热量;
12g金刚石与O2反应生成CO2放出395.41kJ热量,试比较,石墨与金刚石哪个稳定?比较相同状态、相同数量的金刚石和石墨,与O2完全反应,生成相同状态、相同数量的CO2,金刚石释放出的热量更多,说明金刚石具有的总能量高,没有石墨稳定练习2:作业:1、P33 第1、2、3、4、6做在书上
2、第5、7题做在作业本上
3、《三点一册》
