铝的化合物公开课[上学期]
文档属性
| 名称 | 铝的化合物公开课[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 868.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-03-13 00:00:00 | ||
图片预览











文档简介
课件31张PPT。铝的重要化合物长兴中学 王强洪水过后,为防止传染病流行,红十字会发给灾民进行水处理的两种药片,
你知道是什么吗?
你知道其中的化学原理吗?三、铝的重要化合物1、 硫酸铝钾 KAl(SO4)2
1) 复盐: 由两种金属阳离子(含NH4+离子)和一种酸根阴离子复合而成的盐。2)明矾:化学式 KAl(SO4)2.12H2O
KAl(SO4)2·12H2Oa 物理性质:无色晶体、易溶于水。b 化学性质:在水中完全电离。KAl(SO4)2 ==K++Al3++2SO42-Al3++3H2O(胶体)Al(OH)3+3H+明矾: c 用途: 作净水剂思考:Al(OH)3又如何制备呢?2、氢氧化铝 Al(OH)31) 物理性质:白色、胶状(絮状)难溶的物质
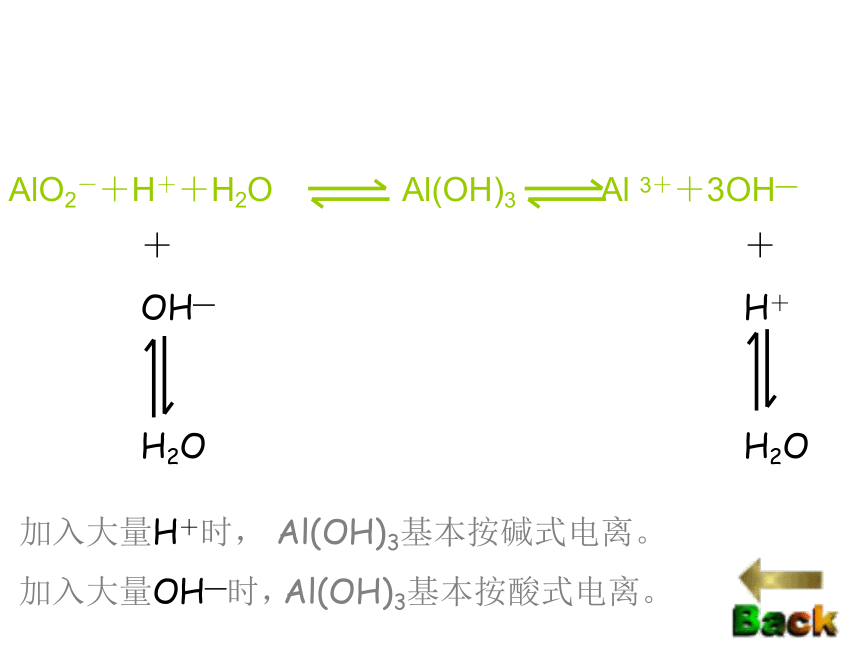
吸附性实验:探究氢氧化铝化学性质 a 两性:2)化学性质:Al(OH)3+3H+=Al3++3H2OAl(OH)3+3OH-=AlO2-+2H2OH+ + AlO2ˉ+ H20 Al(OH)3 Al3+ +3 OHˉ酸式电离碱式电离加酸,C(H+)加碱,C(OHˉ )一元弱酸 三元弱碱AlO2-+H++H2O Al(OH)3 Al 3++3OH—加入大量H+时,+
H+
H2O
Al(OH)3基本按碱式电离。+
OH—
H2O
加入大量OH—时,Al(OH)3基本按酸式电离。思考: 1 往AlCl3溶液中逐滴滴加NaOH溶液,会有什么现象?现象_______________解释 离子方程式 ______________
___________________白色沉淀生成→沉淀增多→沉淀不变建立数学模型
(横座标为后加入试剂的量,纵座标为沉淀量) 2 往NaAlO2溶液中逐滴滴加HCl溶液,会有
什么现象?现象_______________解释 离子方程式 ______________
___________________白色沉淀生成→沉淀增多→沉淀不变建立数学模型
(横座标为后加入试剂的量,纵座标为沉淀量) 将NaOH溶液中逐滴滴加AlCl3,现象如何?解释?建立数轴表示?
将HCl溶液中逐滴滴加NaAlO2,现象如何?解释?建立数轴表示?注意: 1、当Al3+和AlO2-在溶液中相遇,会发生双水解
Al3++3AlO2-+6H2O=4Al(OH)32、Al(OH)3是两性氢氧化物,可以和强酸、强碱发生反应,但是如果碰到弱酸如 H2CO3,弱碱如NH3.H2O,却不会发生反应 b 不稳定性2Al(OH)3 = Al2O3+3H2O探索: 3) Al(OH)3的制备 a 以碱与AlCl3反应,常用NH3.H2O
实验室制法 b 以酸与NaAlO2反应,常用弱酸 c 以Al3+和AlO2-反应--------利用双水解
2AlCl3+6NH3·H2O=2 Al(OH)3↓+3(NH4)2SO4
胃舒平来了!!我的胃又痛了!!胃不痛了,多亏了胃舒平!!!4). 氢氧化铝的用途
氧化铝的天然
存在形式铝土矿
由氧化铝的水合物和少量的氧化铁和二氧化硅杂质组成刚 玉
氧化铝的天然晶体,硬度大仅次于金刚石、金刚砂(SiC)(蓝宝石、红宝石是刚玉的一种)
3、氧化铝 Al2O3
1)、氧化铝的物理性质 2)、氧化铝的化学性质AlO2- Al2O3 Al3+HClNaOH白色、粉末状、难溶解、难熔化的固体两性氧化物的性质——既与酸又与强碱
反应但不与氨水反应
化学方程式离子方程式Al2O3+6HCl = 2AlCl3+3H2OAl2O3+6H+ = 2Al3+ +3H2OAl2O3+2NaOH = 2NaAlO2+ H2OAl2O3+ 2OHˉ = 2AlO2?+H2O 3) 用途 冶炼金属铝,做耐火材料
AlO2? Al(OH)3 Al3+ AlAl2O3O2OH_加热H+OH_H+H+OH_OH_H+小结:一、明矾的检验1、K+的检验2、Al3+的检验3、SO42- 的检验二、0.1mol/L的硫酸铝溶液100ml.需要加入0.5mol/L的氢氧化钠溶液多少ml可以得到沉淀质量最大?为多少克?三. 一定量的氯化铝和氯化镁混合物溶于200ml1mol/L的NaOH溶液中,请作出产生沉淀的物质的量(纵坐标)与加入NaOH体积关系草图?讨论四
用4mol 金属Al来制取4mol氢氧化铝有几条途径?哪种方法最为经济?为什么?(提供氢氧化钠溶液和盐酸溶液) 先加盐酸,再加NaOH溶液4molAl4molAlCl34molAl(OH)3方法一 先加NaOH溶液,再加盐酸4mol Al4mol NaAlO24mol Al(OH)3方法二
利用双水解原理Al3++AlO2-+H2O——3mol Al3mol NaAlO21mol Al1mol AlCl3方法三
你知道是什么吗?
你知道其中的化学原理吗?三、铝的重要化合物1、 硫酸铝钾 KAl(SO4)2
1) 复盐: 由两种金属阳离子(含NH4+离子)和一种酸根阴离子复合而成的盐。2)明矾:化学式 KAl(SO4)2.12H2O
KAl(SO4)2·12H2Oa 物理性质:无色晶体、易溶于水。b 化学性质:在水中完全电离。KAl(SO4)2 ==K++Al3++2SO42-Al3++3H2O(胶体)Al(OH)3+3H+明矾: c 用途: 作净水剂思考:Al(OH)3又如何制备呢?2、氢氧化铝 Al(OH)31) 物理性质:白色、胶状(絮状)难溶的物质
吸附性实验:探究氢氧化铝化学性质 a 两性:2)化学性质:Al(OH)3+3H+=Al3++3H2OAl(OH)3+3OH-=AlO2-+2H2OH+ + AlO2ˉ+ H20 Al(OH)3 Al3+ +3 OHˉ酸式电离碱式电离加酸,C(H+)加碱,C(OHˉ )一元弱酸 三元弱碱AlO2-+H++H2O Al(OH)3 Al 3++3OH—加入大量H+时,+
H+
H2O
Al(OH)3基本按碱式电离。+
OH—
H2O
加入大量OH—时,Al(OH)3基本按酸式电离。思考: 1 往AlCl3溶液中逐滴滴加NaOH溶液,会有什么现象?现象_______________解释 离子方程式 ______________
___________________白色沉淀生成→沉淀增多→沉淀不变建立数学模型
(横座标为后加入试剂的量,纵座标为沉淀量) 2 往NaAlO2溶液中逐滴滴加HCl溶液,会有
什么现象?现象_______________解释 离子方程式 ______________
___________________白色沉淀生成→沉淀增多→沉淀不变建立数学模型
(横座标为后加入试剂的量,纵座标为沉淀量) 将NaOH溶液中逐滴滴加AlCl3,现象如何?解释?建立数轴表示?
将HCl溶液中逐滴滴加NaAlO2,现象如何?解释?建立数轴表示?注意: 1、当Al3+和AlO2-在溶液中相遇,会发生双水解
Al3++3AlO2-+6H2O=4Al(OH)32、Al(OH)3是两性氢氧化物,可以和强酸、强碱发生反应,但是如果碰到弱酸如 H2CO3,弱碱如NH3.H2O,却不会发生反应 b 不稳定性2Al(OH)3 = Al2O3+3H2O探索: 3) Al(OH)3的制备 a 以碱与AlCl3反应,常用NH3.H2O
实验室制法 b 以酸与NaAlO2反应,常用弱酸 c 以Al3+和AlO2-反应--------利用双水解
2AlCl3+6NH3·H2O=2 Al(OH)3↓+3(NH4)2SO4
胃舒平来了!!我的胃又痛了!!胃不痛了,多亏了胃舒平!!!4). 氢氧化铝的用途
氧化铝的天然
存在形式铝土矿
由氧化铝的水合物和少量的氧化铁和二氧化硅杂质组成刚 玉
氧化铝的天然晶体,硬度大仅次于金刚石、金刚砂(SiC)(蓝宝石、红宝石是刚玉的一种)
3、氧化铝 Al2O3
1)、氧化铝的物理性质 2)、氧化铝的化学性质AlO2- Al2O3 Al3+HClNaOH白色、粉末状、难溶解、难熔化的固体两性氧化物的性质——既与酸又与强碱
反应但不与氨水反应
化学方程式离子方程式Al2O3+6HCl = 2AlCl3+3H2OAl2O3+6H+ = 2Al3+ +3H2OAl2O3+2NaOH = 2NaAlO2+ H2OAl2O3+ 2OHˉ = 2AlO2?+H2O 3) 用途 冶炼金属铝,做耐火材料
AlO2? Al(OH)3 Al3+ AlAl2O3O2OH_加热H+OH_H+H+OH_OH_H+小结:一、明矾的检验1、K+的检验2、Al3+的检验3、SO42- 的检验二、0.1mol/L的硫酸铝溶液100ml.需要加入0.5mol/L的氢氧化钠溶液多少ml可以得到沉淀质量最大?为多少克?三. 一定量的氯化铝和氯化镁混合物溶于200ml1mol/L的NaOH溶液中,请作出产生沉淀的物质的量(纵坐标)与加入NaOH体积关系草图?讨论四
用4mol 金属Al来制取4mol氢氧化铝有几条途径?哪种方法最为经济?为什么?(提供氢氧化钠溶液和盐酸溶液) 先加盐酸,再加NaOH溶液4molAl4molAlCl34molAl(OH)3方法一 先加NaOH溶液,再加盐酸4mol Al4mol NaAlO24mol Al(OH)3方法二
利用双水解原理Al3++AlO2-+H2O——3mol Al3mol NaAlO21mol Al1mol AlCl3方法三
