《新课标》高三化学(人教版)第一轮复习选修(5)单元讲座第一讲 脂肪烃[下学期]
文档属性
| 名称 | 《新课标》高三化学(人教版)第一轮复习选修(5)单元讲座第一讲 脂肪烃[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 92.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-01-09 00:00:00 | ||
图片预览



文档简介
PAGE
《新课标》高三化学(人教版)第一轮复习选修(5)单元讲座
第一讲 脂肪烃
复习目标:
1、掌握烷烃与氧气、卤素单质的反应等主要性质。
2、掌握烯(炔)烃与卤素单质、卤化氢、水的反应等主要性质。
3、了解有机化合物结构测定的一般程序和方法。能进行确定有机化合物分子式的简单计算。
4、能建立起脂肪烃(烷、烯、炔)的分类框架。
复习重点、难点:烷、烯、炔与氧气、卤素单质、卤化氢、水的反应等主要性质。
课时划分:两课时
教学过程
知识梳理
一.烷烃:
1.烷烃定义:_____________烷烃的通式:______。
2.烷烃的物理性质的递变性规律
(1)状态的变化:_____________(2)溶沸点的变化:_____________(3)密度的变化:_____________(4)溶解性的特点:_____________(5)含碳量的变化:_____________。
3.烷烃的化学性质的相似性
(1)取代反应(特征性质)
写出乙烷与溴单质生成溴乙烷的反应__________________________________。
烷烃取代反应的共同特征有:_____________。
(2)燃烧:
用通式表示烷烃燃烧的化学方程式:________________________________。
随着碳原子数的增加,往往燃烧越来越不充分,火焰明亮,并伴有黑烟。
(3)高温分解反应:甲烷高温下可分解成碳和氢气;长链烷烃高温下可分解成短链烷烃和烯烃,这在石油化工上有很重要的应用,称为__________________________。
二.烯烃:
1.烯烃:_______单烯烃::_______ 多烯烃:________。
2.单烯烃的通式及组成特点
(1)通式推导:_____________。
(2)组成特点归纳:_____________。
3.物理性质递变:
(1)状态的变化:_____________。(2)熔沸点的变化:_____________。(3)密度的变化:_____________。(4)溶解性的特点:_____________。
4.化学性质的相似性
(1)燃烧:
用通式表示烯烃的燃烧化学方程式__________________________________。
(2)氧化反应(双键的还原性,特征性质):
一个特征反应现象就是______________________________________。
[原理]在酸性溶液中被酸性高锰酸钾氧化,作用进行得更快,得到碳链断裂的氧化产物,氧化后CH2= 基变成CO2,RCH= 基变成羧酸(RCOOH),
[应用]现已知某烯烃的化学式为C5H10,它与酸性高锰酸钾溶液反应后得到的产物为乙酸和丙酸,你能推测出此烯烃的结构吗?若与酸性高锰酸钾溶液反应后得到的产物是二氧化碳和丁酮此烯烃的结构又是怎样的呢?
(3)加成反应(特征性质)
①写出下列反应的化学方程式:
乙烯通入溴水中____________________________________。
乙烯与水的反应_____________________________________。
乙烯与溴化氢反应___________________________________。
②丙稀与氯化氢反应后,会生成什么产物呢?试着写出反应方程式:
[拓展1]“马氏加成规则”: __________________________。
[拓展2]共轭二烯烃的不完全加成特点:竞争加成 __________________________。
[拓展3]烯烃的自身无限加成反应――加聚反应
归纳:单烯烃加聚反应的通式是_______________________。
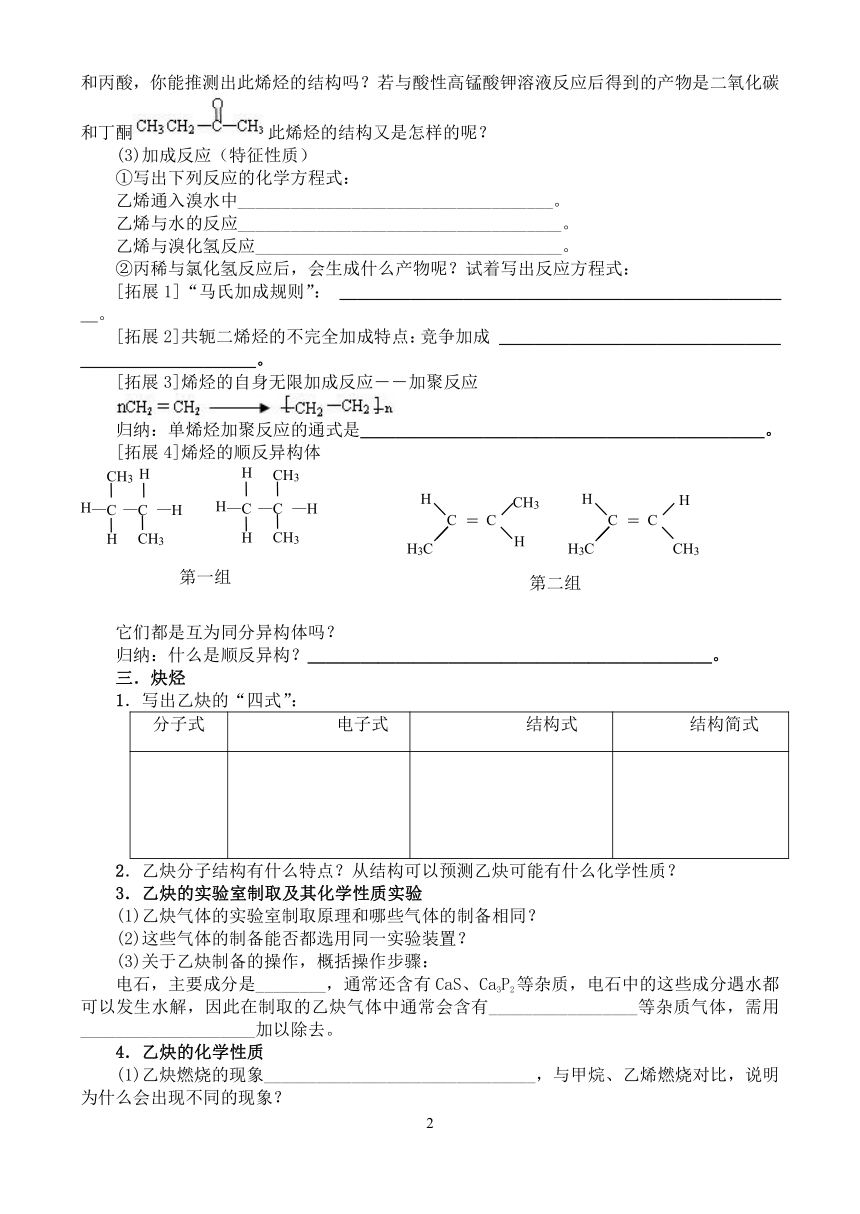
[拓展4]烯烃的顺反异构体
它们都是互为同分异构体吗?
归纳:什么是顺反异构?_______________________。
三.炔烃
1.写出乙炔的“四式”:
分子式 电子式 结构式 结构简式
2.乙炔分子结构有什么特点?从结构可以预测乙炔可能有什么化学性质?
3.乙炔的实验室制取及其化学性质实验
(1)乙炔气体的实验室制取原理和哪些气体的制备相同?
(2)这些气体的制备能否都选用同一实验装置?
(3)关于乙炔制备的操作,概括操作步骤:
电石,主要成分是________,通常还含有CaS、Ca3P2等杂质,电石中的这些成分遇水都可以发生水解,因此在制取的乙炔气体中通常会含有_________________等杂质气体,需用____________________加以除去。
4.乙炔的化学性质
(1)乙炔燃烧的现象_______________________________,与甲烷、乙烯燃烧对比,说明为什么会出现不同的现象?
写出乙炔燃烧反应的化学方程式________________________________
(2)已知乙炔的加成反应是分步进行的,试写出下列反应的化学方程式:
乙炔与氢气反应__________________________________________。
乙炔与氯化氢反应_____________________________________。
乙炔与水反应_________________________________________。
[总结1]
乙烷 乙烯 乙炔
分子式
结构式
电子式
分子结构特点
含碳质量分数
化学活动性
取代反应
加成反应
加聚反应
氧化反应
鉴别
[总结2] 乙烷、乙烯、乙炔分子结构和化学性质比较
四.确定分子式的几种方法
1.相对分子质量法:分别写出相对分子质量为128、72的烃的分子式。
2.实验式法:已知某气态烃含碳质量分数为80%,求该烃的分子式。
3.通式法:某气态不饱和烃对氢气的相对密度为27。0.54g该烃恰好与浓度为0.2mol·L-1的溴水100mL完全反应,使溴水完全褪色。求该烃的分子式。
4.烃燃烧规律法:在同温同压下,10mL某气态烃在50mLO2里充分燃烧,得到液态水和体积为35mL的混合气体,则该烃的分子式可能是( )
A.CH4 B.C2H6 C.C3H8 D.C3H6
疑难点拨
一、烯烃和炔烃被高锰酸钾溶液氧化的产物是什么?
高锰酸钾是强氧化剂,它能和许多有机物发生化学反应,但在不同介质中,高锰酸钾的还原产物是不同的。一般来说,在中性和弱碱性溶液中,高锰酸钾被还原为二氧化锰;在酸性溶液中,高锰酸钾被还原为二价锰盐。而且,高锰酸钾的氧化能力在酸性溶液中比在中性或碱性溶液中强得多。
(1)烯烃与高锰酸钾溶液的反应
中性或碱性的稀高锰酸钾冷溶液能使烯烃氧化成二元醇,反应式如下:
生成的二元醇可进一步被氧化,生成羧酸。
在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,CH2=基被氧化成CO2,RCH=基被氧化成羧酸, C=基被氧化成酮。
5CH2=CH2+12KMnO4+18H2SO4→10CO2+28H2O+6K2SO4+12MnSO4
(2)炔烃与高锰酸钾溶液的反应
炔烃被高锰酸钾氧化时,叁键断裂,RC≡基变成羧酸,CH≡基变成CO2。
在碱性溶液中:
3RC≡CH+8KMnO4+KOH→
3CH≡CH+10KMnO4+2KOH→6K2CO3+10MnO2+4H2O
其中K2CO3是由CO2与KOH作用而生成的。
在酸性溶液中:
5R-C≡CH+8KMnO4+12H2SO4→5RCOOH+5CO2+4K2SO4+8MnSO4+12H2O
CH≡CH+2KMnO4+3H2SO4→2CO2+4H2O+K2SO4+2MnSO4
二、烃完全燃烧时的耗氧规律?
1、等物质的量的烃(CxHy)完全燃烧时,其耗氧量的大小取决于(x+)的值,其值越大,耗氧量越大.?
2、等质量的烃完全燃烧时,其耗氧量的大小取决于该烃分子中氢的质量分数(或氢原子数与碳原子数的比值),其值越大,耗氧量越大.?
3、最简式相同的烃,不论它们以何种比例混合,只要总质量一定,完全燃烧时所消耗的氧气以及燃烧后生成的二氧化碳和水的量均为定值.满足上述条件的烃有C2H2与C6H6;烯烃与烯烃或烯烃与环烷烃等.
三、分子式、结构式的确定经验规律?
1、由相对分子质量求烃的分子式(设烃的相对分子质量为M).①得整数商和余数,商为可能的最大碳原子数,余数为最小的氢原子数.②的余数为0或碳原子数≥6时,将碳原子数依次减少一个即增加12个氢原子,直到饱和为止.?
2、由最简式求烃的分子式.首先由题意求出烃的最简式,设为CaHb,且=x,则有:
①若x<,该烃为烷烃.由烷烃通式CnH2n+2得=x,求出n值即可求出该烃的分子式.
②若x=,该烃为烯烃或环烷烃,要由相对分子质量才能确定其分子式.
③若<x<1,该烃可能是CnH2n-2或CnH2n-6,可由通式直接求出分子式.?
④若x=1,该烃可能为C2H2、C6H6或C8H8,由其相对分子质量或性质确定分子式.
典例剖析
例1、描述CH3—CH==CH—C≡C—CF3分子结构的下列叙述中,正确的是
A.6个碳原子有可能都在一条直线上
B.6个碳原子不可能都在一条直线上
C.6个碳原子有可能都在同一平面上
D.6个碳原子不可能都在同一平面上
解析:本题把甲烷的正四面体结构,乙烯的平面结构、乙炔的线型结构集中体现在一个特定的有机化合物中,并以该有机物中碳原子的几何形状来设问,考查空间概念和形象思维.分析时可以把该有机物中的6个碳原子依次进行编号,分为两组进行分析:
① ② ③ ④ ⑤ ⑥
CH3—CH==CH—C≡C—CF3
①②③④这4个碳原子具有乙烯平面型结构,它们在同一平面上,而不在同一直线上,键角120°;③④⑤⑥这4个碳原子具有乙炔的线型结构,它们在同一直线上,键角为180 °.由此可知,这6个碳原子不可能都在同一直线,有可能都在同一平面。答案: BC。
例2、某烷烃只能生成一种一氯化物,此烷烃的分子式可以是( )
A. B. C. D.
解析:由于CH4 分子具有空间对称性,故每个氢原子的位置相同,只有一种一氯取代物。 的一种同分异构体—新戊烷可以看作是由甲基取代了CH4 分子里的氢原子而形成的,同样具有空间对称性,故4个甲基上的每个氢原子的位置也相同,也只有一种一氯代物。
解答:AD选项符合题意
点评:运用空间结构对称性法则判断同分异构体的数目比较方便。例如,分子式符合 ,其一卤代物只有一种的烷烃可以是由最简单的 和 (H位置均相同)推理判断。即:
从理论上讲,可以写出无限种这类烷烃。
例3、下列有关烷烃的叙述不正确的是( )
A.在烷烃分子中,所有的化学键均为单键
B.所有的烷烃都一定互为同系物
C.烷烃中随碳原子数的增多,沸点逐渐升高
D.烷烃的通式为 ,符合该通式的不一定是烷烃
解析:因 已达到饱和,故符合该通式的一定是烷烃,答案为D。答案:D
例4、通常,烷烃可以由相应的烯烃经催化加氢得到.但是,有一种烷烃A,分子式C9H20,它却不能由任何C9H18的烯烃催化加氢得到.而另有A的三个同分异构体B1、B2、B3,却分别可由而且只能用1种自己相应的烯烃催化加氢得到.A、B1、B2、B3的结构简式为______、______、______、______.
解答: 一般情况下,烷烃可以由相应的烯烃催化加氢得到.烯键上加氢后的2个碳原子必定至少各带有1个氢原子,故连接有4个碳原子的碳原子(即季碳原子)是不可能由加氢得到的.现设想A中的所有碳原子,或者本身是季碳原子,或者直接连在季碳原子上,这样,它就不可能是由任何烯烃经催化加氢得到的,据此,可写出A的结构简式.又因为B1、B2、B3分子中都至少有2个不是季碳原子的碳原子相连,可推出B1、B2、B3的结构简式.
知能训练
一、选择题
1.下列事实、事件、事故中与甲烷有无关的是 ( )
A.天然气的主要成分 B.石油经过催化裂化及裂解后的产物
C.“西气东输”中气体 D.煤矿中的瓦斯爆炸
2.二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟里昂”产品,用作空调、冰箱和冷冻库等中的致冷剂。试判断二氟甲烷的结构简式( )
A.有4种 B.有3种 C.有2种 D.只有1种
3.下列烷烃的一氯取代物中没有同分异构体的是( )
A.丙烷 B.丁烷 C.异丁烷 D.新戊烷
4.关于炔烃的下列描述正确的是 ( )
A.分子里含有碳碳三键的不饱和链烃叫炔烃
B.炔烃分子里的所有碳原子都在同一直线上
C.炔烃易发生加成反应,也易发生取代反应
D.炔烃不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色
5.等物质的量的与Br2起加成反应,生成的主要产物是( )
6.据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:
HC≡C—C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是( )
A.不能使溴的四氯化碳溶液褪色 B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应 D.可由乙炔和含氮化合物加聚制得
7.若1 mol某气态烃CxHy完全燃烧,需用3 mol O2,则 ( )
A.x = 2,y =2 B.x = 2,y =4 C.x = 3,y =6 D.2=3,y=8
8.充分燃烧3 L由甲烷、乙烯和丙炔组成的混合气体,生成7 L CO2和4.82 g水(气体体积均在标准状况下测定),则原混合气体中甲烷、乙烯和乙炔的体积比可能是 ( )
A. 1∶1∶1 B.1∶2∶3 C.3∶2∶1 D.3∶1∶2
9.下列化工工艺可得到汽油的是 ( )
A.裂化 B.常压分馏 C.裂解 D.催化重整
10.下列各种物质中,碳氢质量比为一定值的是 ( )
A.甲烷和乙烷 B.乙烯和丙烯 C.苯和乙炔 D.乙炔和丙炔
11.有8种物质:①甲烷;②苯;③聚乙烯;④邻二甲苯; ⑤乙炔; 既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是:
A.③④⑤ B.④⑤ C.只有⑤ D.全部
12.某气态烃10 mL与50 mL氧气在一定条件下作用,刚好耗尽反应物,生成水蒸气
40 mL、一氧化碳和二氧化碳各20 mL各体积都是在同温同压下测得。该气态烃为 ( )
A.C3H8 B.C4H6 C.C3H6 D.C4H8
13.加成反应也是有机化学中的一类重要的反应类型,下列各组物质中不能全部发生加成反应的是( )
A.乙烷、乙烯 B.乙烯、乙炔
C.氯乙烯、溴乙烯 D.顺-2-丁烯、反-2-丁烯
二、实验题
14.图中的实验装置可用于制取乙炔。 请填空:
(1)图中,A管的作用是 。制取乙炔的化学方程式是 。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 , 乙炔发生了 反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象 是 , 乙炔发生了 反应。
(4)为了安全,点燃乙炔前应 ,乙炔燃烧时的实验现象是 。
三、填空题
15.有机化学中的反应类型较多,将下列反应归类(填序号)。
①由乙炔制氯乙烯 ②乙烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色
④乙烯使酸性高锰酸钾溶液褪色 ⑤由乙烯制聚乙烯
⑥甲烷与氯气在光照的条件下反应 ⑦溴乙烷和氢氧化钠乙醇溶液共热
⑧溴乙烷和氢氧化钠溶液共热
其中属于取代反应的是________;属于氧化反应的是.________;属于加成反应的是.________;属消去反应的是________;属于聚合反应的是__________ 。
16.有机物的结构可用“键线式”简化表示。CH3—CH=CH-CH3可简写为 。
有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,写出其反应的化学方程式:
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有 种。
参考答案
1.B 2.C 3.D 4.A 5.AB 6.B 7.B 8.B 9.AB 10.BC
11.C 12.D 13.A
14.⑴调节水面的高度以控制反应的发生和停止 CaC2+2H2O=C2H2↑+Ca(OH)2
⑵KMnO4溶液褪色 氧化
⑶溴的CCl4溶液褪色 加成
⑷检查乙炔的纯度 火焰明亮并伴有浓烈的黑烟
15.⑥⑧;②④;①③;⑦;⑤
16.(1)
(2)
(3)2
C
第一组
CH3
CH3
H
H
H
—H
—C
—C
CH3
CH3
H
H
H
—H
—C
—C
C
第二组
CH3
H3C
H
H
=
C
C
CH3
H3C
H
=
H
PAGE
3
《新课标》高三化学(人教版)第一轮复习选修(5)单元讲座
第一讲 脂肪烃
复习目标:
1、掌握烷烃与氧气、卤素单质的反应等主要性质。
2、掌握烯(炔)烃与卤素单质、卤化氢、水的反应等主要性质。
3、了解有机化合物结构测定的一般程序和方法。能进行确定有机化合物分子式的简单计算。
4、能建立起脂肪烃(烷、烯、炔)的分类框架。
复习重点、难点:烷、烯、炔与氧气、卤素单质、卤化氢、水的反应等主要性质。
课时划分:两课时
教学过程
知识梳理
一.烷烃:
1.烷烃定义:_____________烷烃的通式:______。
2.烷烃的物理性质的递变性规律
(1)状态的变化:_____________(2)溶沸点的变化:_____________(3)密度的变化:_____________(4)溶解性的特点:_____________(5)含碳量的变化:_____________。
3.烷烃的化学性质的相似性
(1)取代反应(特征性质)
写出乙烷与溴单质生成溴乙烷的反应__________________________________。
烷烃取代反应的共同特征有:_____________。
(2)燃烧:
用通式表示烷烃燃烧的化学方程式:________________________________。
随着碳原子数的增加,往往燃烧越来越不充分,火焰明亮,并伴有黑烟。
(3)高温分解反应:甲烷高温下可分解成碳和氢气;长链烷烃高温下可分解成短链烷烃和烯烃,这在石油化工上有很重要的应用,称为__________________________。
二.烯烃:
1.烯烃:_______单烯烃::_______ 多烯烃:________。
2.单烯烃的通式及组成特点
(1)通式推导:_____________。
(2)组成特点归纳:_____________。
3.物理性质递变:
(1)状态的变化:_____________。(2)熔沸点的变化:_____________。(3)密度的变化:_____________。(4)溶解性的特点:_____________。
4.化学性质的相似性
(1)燃烧:
用通式表示烯烃的燃烧化学方程式__________________________________。
(2)氧化反应(双键的还原性,特征性质):
一个特征反应现象就是______________________________________。
[原理]在酸性溶液中被酸性高锰酸钾氧化,作用进行得更快,得到碳链断裂的氧化产物,氧化后CH2= 基变成CO2,RCH= 基变成羧酸(RCOOH),
[应用]现已知某烯烃的化学式为C5H10,它与酸性高锰酸钾溶液反应后得到的产物为乙酸和丙酸,你能推测出此烯烃的结构吗?若与酸性高锰酸钾溶液反应后得到的产物是二氧化碳和丁酮此烯烃的结构又是怎样的呢?
(3)加成反应(特征性质)
①写出下列反应的化学方程式:
乙烯通入溴水中____________________________________。
乙烯与水的反应_____________________________________。
乙烯与溴化氢反应___________________________________。
②丙稀与氯化氢反应后,会生成什么产物呢?试着写出反应方程式:
[拓展1]“马氏加成规则”: __________________________。
[拓展2]共轭二烯烃的不完全加成特点:竞争加成 __________________________。
[拓展3]烯烃的自身无限加成反应――加聚反应
归纳:单烯烃加聚反应的通式是_______________________。
[拓展4]烯烃的顺反异构体
它们都是互为同分异构体吗?
归纳:什么是顺反异构?_______________________。
三.炔烃
1.写出乙炔的“四式”:
分子式 电子式 结构式 结构简式
2.乙炔分子结构有什么特点?从结构可以预测乙炔可能有什么化学性质?
3.乙炔的实验室制取及其化学性质实验
(1)乙炔气体的实验室制取原理和哪些气体的制备相同?
(2)这些气体的制备能否都选用同一实验装置?
(3)关于乙炔制备的操作,概括操作步骤:
电石,主要成分是________,通常还含有CaS、Ca3P2等杂质,电石中的这些成分遇水都可以发生水解,因此在制取的乙炔气体中通常会含有_________________等杂质气体,需用____________________加以除去。
4.乙炔的化学性质
(1)乙炔燃烧的现象_______________________________,与甲烷、乙烯燃烧对比,说明为什么会出现不同的现象?
写出乙炔燃烧反应的化学方程式________________________________
(2)已知乙炔的加成反应是分步进行的,试写出下列反应的化学方程式:
乙炔与氢气反应__________________________________________。
乙炔与氯化氢反应_____________________________________。
乙炔与水反应_________________________________________。
[总结1]
乙烷 乙烯 乙炔
分子式
结构式
电子式
分子结构特点
含碳质量分数
化学活动性
取代反应
加成反应
加聚反应
氧化反应
鉴别
[总结2] 乙烷、乙烯、乙炔分子结构和化学性质比较
四.确定分子式的几种方法
1.相对分子质量法:分别写出相对分子质量为128、72的烃的分子式。
2.实验式法:已知某气态烃含碳质量分数为80%,求该烃的分子式。
3.通式法:某气态不饱和烃对氢气的相对密度为27。0.54g该烃恰好与浓度为0.2mol·L-1的溴水100mL完全反应,使溴水完全褪色。求该烃的分子式。
4.烃燃烧规律法:在同温同压下,10mL某气态烃在50mLO2里充分燃烧,得到液态水和体积为35mL的混合气体,则该烃的分子式可能是( )
A.CH4 B.C2H6 C.C3H8 D.C3H6
疑难点拨
一、烯烃和炔烃被高锰酸钾溶液氧化的产物是什么?
高锰酸钾是强氧化剂,它能和许多有机物发生化学反应,但在不同介质中,高锰酸钾的还原产物是不同的。一般来说,在中性和弱碱性溶液中,高锰酸钾被还原为二氧化锰;在酸性溶液中,高锰酸钾被还原为二价锰盐。而且,高锰酸钾的氧化能力在酸性溶液中比在中性或碱性溶液中强得多。
(1)烯烃与高锰酸钾溶液的反应
中性或碱性的稀高锰酸钾冷溶液能使烯烃氧化成二元醇,反应式如下:
生成的二元醇可进一步被氧化,生成羧酸。
在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,CH2=基被氧化成CO2,RCH=基被氧化成羧酸, C=基被氧化成酮。
5CH2=CH2+12KMnO4+18H2SO4→10CO2+28H2O+6K2SO4+12MnSO4
(2)炔烃与高锰酸钾溶液的反应
炔烃被高锰酸钾氧化时,叁键断裂,RC≡基变成羧酸,CH≡基变成CO2。
在碱性溶液中:
3RC≡CH+8KMnO4+KOH→
3CH≡CH+10KMnO4+2KOH→6K2CO3+10MnO2+4H2O
其中K2CO3是由CO2与KOH作用而生成的。
在酸性溶液中:
5R-C≡CH+8KMnO4+12H2SO4→5RCOOH+5CO2+4K2SO4+8MnSO4+12H2O
CH≡CH+2KMnO4+3H2SO4→2CO2+4H2O+K2SO4+2MnSO4
二、烃完全燃烧时的耗氧规律?
1、等物质的量的烃(CxHy)完全燃烧时,其耗氧量的大小取决于(x+)的值,其值越大,耗氧量越大.?
2、等质量的烃完全燃烧时,其耗氧量的大小取决于该烃分子中氢的质量分数(或氢原子数与碳原子数的比值),其值越大,耗氧量越大.?
3、最简式相同的烃,不论它们以何种比例混合,只要总质量一定,完全燃烧时所消耗的氧气以及燃烧后生成的二氧化碳和水的量均为定值.满足上述条件的烃有C2H2与C6H6;烯烃与烯烃或烯烃与环烷烃等.
三、分子式、结构式的确定经验规律?
1、由相对分子质量求烃的分子式(设烃的相对分子质量为M).①得整数商和余数,商为可能的最大碳原子数,余数为最小的氢原子数.②的余数为0或碳原子数≥6时,将碳原子数依次减少一个即增加12个氢原子,直到饱和为止.?
2、由最简式求烃的分子式.首先由题意求出烃的最简式,设为CaHb,且=x,则有:
①若x<,该烃为烷烃.由烷烃通式CnH2n+2得=x,求出n值即可求出该烃的分子式.
②若x=,该烃为烯烃或环烷烃,要由相对分子质量才能确定其分子式.
③若<x<1,该烃可能是CnH2n-2或CnH2n-6,可由通式直接求出分子式.?
④若x=1,该烃可能为C2H2、C6H6或C8H8,由其相对分子质量或性质确定分子式.
典例剖析
例1、描述CH3—CH==CH—C≡C—CF3分子结构的下列叙述中,正确的是
A.6个碳原子有可能都在一条直线上
B.6个碳原子不可能都在一条直线上
C.6个碳原子有可能都在同一平面上
D.6个碳原子不可能都在同一平面上
解析:本题把甲烷的正四面体结构,乙烯的平面结构、乙炔的线型结构集中体现在一个特定的有机化合物中,并以该有机物中碳原子的几何形状来设问,考查空间概念和形象思维.分析时可以把该有机物中的6个碳原子依次进行编号,分为两组进行分析:
① ② ③ ④ ⑤ ⑥
CH3—CH==CH—C≡C—CF3
①②③④这4个碳原子具有乙烯平面型结构,它们在同一平面上,而不在同一直线上,键角120°;③④⑤⑥这4个碳原子具有乙炔的线型结构,它们在同一直线上,键角为180 °.由此可知,这6个碳原子不可能都在同一直线,有可能都在同一平面。答案: BC。
例2、某烷烃只能生成一种一氯化物,此烷烃的分子式可以是( )
A. B. C. D.
解析:由于CH4 分子具有空间对称性,故每个氢原子的位置相同,只有一种一氯取代物。 的一种同分异构体—新戊烷可以看作是由甲基取代了CH4 分子里的氢原子而形成的,同样具有空间对称性,故4个甲基上的每个氢原子的位置也相同,也只有一种一氯代物。
解答:AD选项符合题意
点评:运用空间结构对称性法则判断同分异构体的数目比较方便。例如,分子式符合 ,其一卤代物只有一种的烷烃可以是由最简单的 和 (H位置均相同)推理判断。即:
从理论上讲,可以写出无限种这类烷烃。
例3、下列有关烷烃的叙述不正确的是( )
A.在烷烃分子中,所有的化学键均为单键
B.所有的烷烃都一定互为同系物
C.烷烃中随碳原子数的增多,沸点逐渐升高
D.烷烃的通式为 ,符合该通式的不一定是烷烃
解析:因 已达到饱和,故符合该通式的一定是烷烃,答案为D。答案:D
例4、通常,烷烃可以由相应的烯烃经催化加氢得到.但是,有一种烷烃A,分子式C9H20,它却不能由任何C9H18的烯烃催化加氢得到.而另有A的三个同分异构体B1、B2、B3,却分别可由而且只能用1种自己相应的烯烃催化加氢得到.A、B1、B2、B3的结构简式为______、______、______、______.
解答: 一般情况下,烷烃可以由相应的烯烃催化加氢得到.烯键上加氢后的2个碳原子必定至少各带有1个氢原子,故连接有4个碳原子的碳原子(即季碳原子)是不可能由加氢得到的.现设想A中的所有碳原子,或者本身是季碳原子,或者直接连在季碳原子上,这样,它就不可能是由任何烯烃经催化加氢得到的,据此,可写出A的结构简式.又因为B1、B2、B3分子中都至少有2个不是季碳原子的碳原子相连,可推出B1、B2、B3的结构简式.
知能训练
一、选择题
1.下列事实、事件、事故中与甲烷有无关的是 ( )
A.天然气的主要成分 B.石油经过催化裂化及裂解后的产物
C.“西气东输”中气体 D.煤矿中的瓦斯爆炸
2.二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟里昂”产品,用作空调、冰箱和冷冻库等中的致冷剂。试判断二氟甲烷的结构简式( )
A.有4种 B.有3种 C.有2种 D.只有1种
3.下列烷烃的一氯取代物中没有同分异构体的是( )
A.丙烷 B.丁烷 C.异丁烷 D.新戊烷
4.关于炔烃的下列描述正确的是 ( )
A.分子里含有碳碳三键的不饱和链烃叫炔烃
B.炔烃分子里的所有碳原子都在同一直线上
C.炔烃易发生加成反应,也易发生取代反应
D.炔烃不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色
5.等物质的量的与Br2起加成反应,生成的主要产物是( )
6.据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:
HC≡C—C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是( )
A.不能使溴的四氯化碳溶液褪色 B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应 D.可由乙炔和含氮化合物加聚制得
7.若1 mol某气态烃CxHy完全燃烧,需用3 mol O2,则 ( )
A.x = 2,y =2 B.x = 2,y =4 C.x = 3,y =6 D.2=3,y=8
8.充分燃烧3 L由甲烷、乙烯和丙炔组成的混合气体,生成7 L CO2和4.82 g水(气体体积均在标准状况下测定),则原混合气体中甲烷、乙烯和乙炔的体积比可能是 ( )
A. 1∶1∶1 B.1∶2∶3 C.3∶2∶1 D.3∶1∶2
9.下列化工工艺可得到汽油的是 ( )
A.裂化 B.常压分馏 C.裂解 D.催化重整
10.下列各种物质中,碳氢质量比为一定值的是 ( )
A.甲烷和乙烷 B.乙烯和丙烯 C.苯和乙炔 D.乙炔和丙炔
11.有8种物质:①甲烷;②苯;③聚乙烯;④邻二甲苯; ⑤乙炔; 既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是:
A.③④⑤ B.④⑤ C.只有⑤ D.全部
12.某气态烃10 mL与50 mL氧气在一定条件下作用,刚好耗尽反应物,生成水蒸气
40 mL、一氧化碳和二氧化碳各20 mL各体积都是在同温同压下测得。该气态烃为 ( )
A.C3H8 B.C4H6 C.C3H6 D.C4H8
13.加成反应也是有机化学中的一类重要的反应类型,下列各组物质中不能全部发生加成反应的是( )
A.乙烷、乙烯 B.乙烯、乙炔
C.氯乙烯、溴乙烯 D.顺-2-丁烯、反-2-丁烯
二、实验题
14.图中的实验装置可用于制取乙炔。 请填空:
(1)图中,A管的作用是 。制取乙炔的化学方程式是 。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 , 乙炔发生了 反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象 是 , 乙炔发生了 反应。
(4)为了安全,点燃乙炔前应 ,乙炔燃烧时的实验现象是 。
三、填空题
15.有机化学中的反应类型较多,将下列反应归类(填序号)。
①由乙炔制氯乙烯 ②乙烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色
④乙烯使酸性高锰酸钾溶液褪色 ⑤由乙烯制聚乙烯
⑥甲烷与氯气在光照的条件下反应 ⑦溴乙烷和氢氧化钠乙醇溶液共热
⑧溴乙烷和氢氧化钠溶液共热
其中属于取代反应的是________;属于氧化反应的是.________;属于加成反应的是.________;属消去反应的是________;属于聚合反应的是__________ 。
16.有机物的结构可用“键线式”简化表示。CH3—CH=CH-CH3可简写为 。
有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,写出其反应的化学方程式:
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有 种。
参考答案
1.B 2.C 3.D 4.A 5.AB 6.B 7.B 8.B 9.AB 10.BC
11.C 12.D 13.A
14.⑴调节水面的高度以控制反应的发生和停止 CaC2+2H2O=C2H2↑+Ca(OH)2
⑵KMnO4溶液褪色 氧化
⑶溴的CCl4溶液褪色 加成
⑷检查乙炔的纯度 火焰明亮并伴有浓烈的黑烟
15.⑥⑧;②④;①③;⑦;⑤
16.(1)
(2)
(3)2
C
第一组
CH3
CH3
H
H
H
—H
—C
—C
CH3
CH3
H
H
H
—H
—C
—C
C
第二组
CH3
H3C
H
H
=
C
C
CH3
H3C
H
=
H
PAGE
3
同课章节目录
