铁及其化合物复习[上学期]
图片预览


文档简介
高三化学《铁及其化合物》复习课
1 教学内容及设计意图
1.1教学内容分析
元素及其化合物知识的复习,在高三总复习中占有很大的比重,如何提高其复习的效率与效果是每一位化学教师都应探讨的课题。铁及其化合物这一内容在元素化合物知识中很有代表性,探索这一内容的复习方法对其它元素及其化合物的复习有一定的借鉴作用。
这一部分内容的知识点主要包括:铁在元素周期表中的位置、原子结构和性质;铁的氧化物、氢氧化物的性质、制备、用途;Fe2+、Fe3+离子的性质、互相转化及检验。在复习中,要充分发挥这三个知识点的载体作用,通过对知识的复习来提高学生的素质,培养学生的能力。
1.2设计意图
(1)元素及其化合物的复习要避免传统教学中为“巩固知识”而设计教学步骤的做法,应从“能力立意”的教学新理念出发,将“巩固知识”当作提高学生素质、培养学生能力的手段。
(2)课堂教学从两条主线同步展开
知识主线:铁的位置、结构、性质→铁化合物的性质、转化、用途→铁及其化合物知识的应用
能力主线:透过现象看本质(思维方法)→建立并完善认知结构(思维形式)→科学地探索未知世界(思维态度)
(3)让学生成为课堂的主角。教学过程中克服教师讲学生听、教师问学生答、教师出题学生做题的被动局面。教师的作用是创设情景,提供向导,在适当的时候进行纠错、把舵。
2 教学过程设计及实施
2.1 铁的位置、结构、性质
多媒体投影 元素周期表(Fe闪烁)
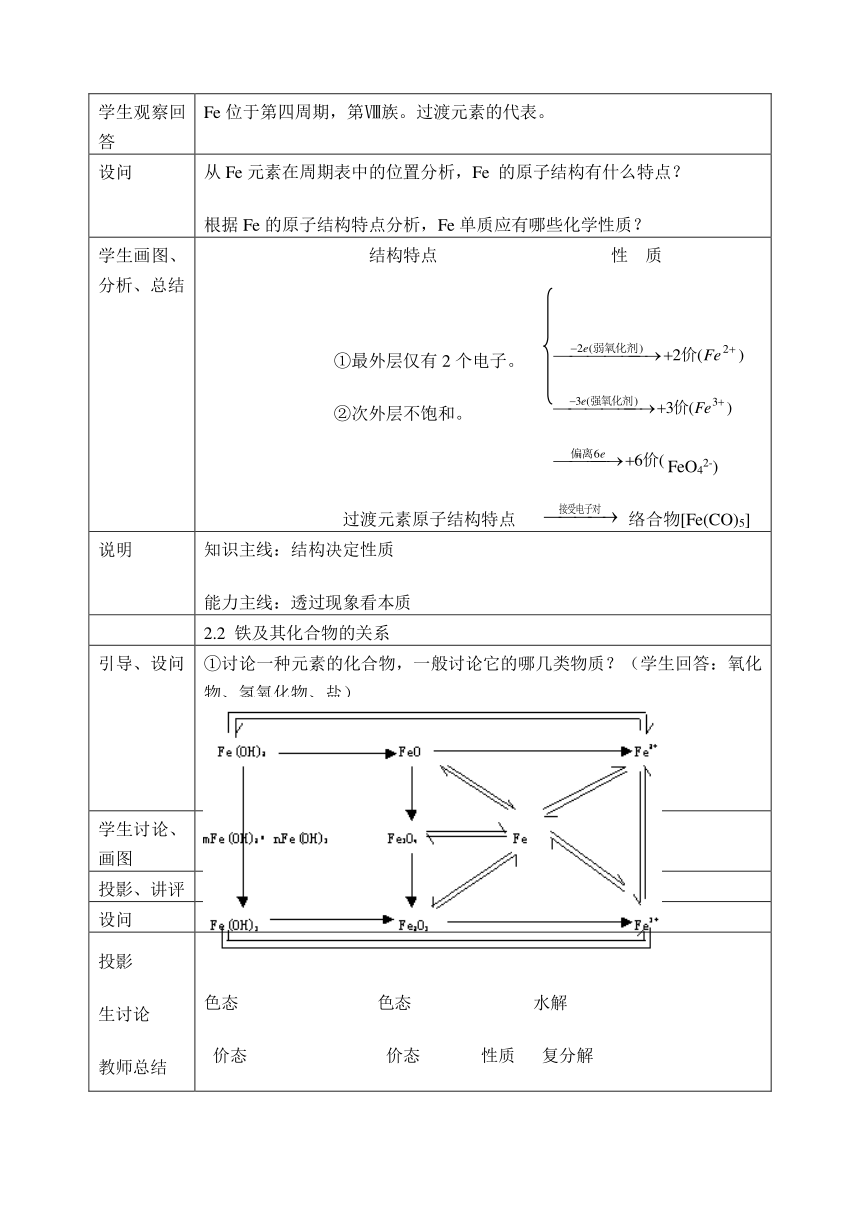
学生观察回答 Fe位于第四周期,第Ⅷ族。过渡元素的代表。
设问 从Fe元素在周期表中的位置分析,Fe 的原子结构有什么特点?根据Fe的原子结构特点分析,Fe单质应有哪些化学性质?
学生画图、分析、总结 结构特点 性 质 ①最外层仅有2个电子。 ②次外层不饱和。 FeO42-) 过渡元素原子结构特点 络合物[Fe(CO)5]
说明 知识主线:结构决定性质能力主线:透过现象看本质
2.2 铁及其化合物的关系
引导、设问 ①讨论一种元素的化合物,一般讨论它的哪几类物质?(学生回答:氧化物、氢氧化物、盐)②铁的氧化物、氢氧化物、盐有哪一些?(学生回答)③你能否用箭头科学地表示出它们之间的相互关系?
学生讨论、画图 要求注明各个箭头上的转化条件
投影、讲评 将学生画的图选3幅讨论,讲评,找出各自的优点。
设问 根据同学们画出的关系图,我们可以从哪些方面来复习呢?
投影生讨论教师总结 色态 色态 水解 价态 价态 性质 复分解 溶解性 溶解性 氧化—还原 制法 用途 络合
辅助教学 ①观察FeSO4溶液、FeCl3溶液颜色,并向其中滴加NaOH溶液;②观察废旧磁卡、牡丹卡、普通磁带,用磁铁试验其磁性。
说明 知识主线:Fe及其化合物的知识结构 横向——价态不变 纵向——价态变化能力主线:建立并完善认知结构(要求有序、科学)
2.3 知识应用
投影 (1)已知FeCl3的熔点为555K,沸点为588K,易溶于水,也易溶于乙醚、丙酮等有机溶剂中,据此分析,FeCl3应属于_____型化合物。
学生分析 从FeCl3的熔沸点、溶解性分析,它属于共价化合物。(它类似于AlCl3,气态时以Fe2Cl6分子形态存在。由性质推断结构是化学中常用的方法。)
投影 (2)常温下,1mol/L的FeCl3水溶性显_____性,离子反应方程式为____________________。常温下,有没有pH=7的FeCl3水溶液?化学实验室中应如何保存存FeCl3溶液?
学生实验并回答问题 学生测1mol/L的FeCl3溶液的pH值。书写离子方程式 Fe3++3H2O=Fe(OH)3+3H+,回答问题。
投影 (3)在Na2CO3溶液中滴加少量FeCl3溶液,可能看到什么现象?为什么?
学生实验分析原因 产生红褐色沉淀,有气泡冒出。分析原因:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑
投影、设问 在FeCl3溶液中滴加少量Na2CO3溶液,可能看到什么现象?分析原因。
学生实验并分析 产生红褐色沉淀,摇动后消失,有气泡冒出。原因:产生的Fe(OH)3溶解于过量的H+中(H+来自过量FeCl3的水解或为抑制其水解加入的少量HCl。
投影 (4)Na2S也是强碱弱酸盐,它和Na2CO3相似。在Na2S水溶液中滴入少量FeCl3溶液会看到什么现象?分析原因。 在FeCl3溶液中滴入少量的Na2S溶液,又会看到什么现象?请给出合理的解释。
学生实验 ③出现大量黑色沉淀②出现黑色沉淀,但很快就消失,溶液混浊。(这一结果大大出乎同学们的意料,大家非常兴奋)
设问 这黑色物质是何物?怎么生成的?如何证明你的想法?
学生讨论 ③大家思考并开展讨论。②请几位同学发言。
学生实验并解释 ③在产生黑色沉淀的试管中加入稀H2SO4,并闻气味。②现象:黑色沉淀消失,有淡黄色混浊,可以闻到臭鸡蛋味③解释:2Fe3++3S2-=2FeS↓+S↓ FeS+2H+=Fe2++H2S↑(有同学提出生成Fe2S3,则设问:Fe2S3能稳定地存在于水溶液中吗?)
投影 (5)FeCl3溶液中滴加KSCN溶液后,溶液呈现_____色,若再滴入NaCl溶液,溶液颜色变化为_____________。滴入NaF溶液后,溶液颜色变化为__________。分析原因。
学生实验 前者颜色几乎不变,后者明显变浅。
讨论分析 Fe3++6F-=[FeF6]3- ,生成的络合物[FeF6]3-稳定性比[Fe(SCN)]2+更强。使前一平衡向逆反应方向移动。
作业 已知某种硫酸盐可以用来治疗缺铁性贫血,制药厂在药片外包一层特制的糖衣,以防止它在空气中变质、失效。该药品的化学式为________________。①请你设计一个实验,以证明该药片是否变质。②请到附近医院调查一下,目前医院治疗缺铁性贫血主要有哪些药物?
说明 知识主线:铁及其化合物知识的应用能力主线:科学地探索未知世界
3.教学后记
3.1高三元素化合物的复习在知识处理上要做到:高屋建瓴,纵横联系。
高屋建瓴也就是在知识把握上必须大处着眼,对某一块知识,可先从知识分类上着手,对各类知识进行归纳总结。如铁及其化合物可从单质铁、铁的氧化物、铁的氢氧化物、铁的盐四个方面展开讨论。纵横联系就是在复习中要加强不同类知识间的横向联系和同类知识内的纵向联系。如铁及其化合物复习时,横向上强调四类物质间的转化规律(除铁外,其余三类转化价态不变),纵向上突出同一类物质间的价态变化规律。这样处理教学内容一方面使课的知识密度得到加大,而更重要的是使学生的认知结构得以完善。
3.2元素化合物复习在教学方法上应采用传统教学方法与现代教学方法的有机整合。
传统教学方法重视知识的巩固,在使用时易犯“炒冷饭”的毛病,而现代教学方法重视能力的培养,在使用时易犯“烧夹生饭”的毛病。只有两者有机整合,才能达到既巩固知识又培养能力的教学目标。本节课在知识复习上,十分重视双基的落实,如对Fe的性质的复习,从过渡元素的原子结构特征上作了深入的挖掘,对Fe2+ 、Fe3+的盐则从水解、氧化—还原、络合等方面作了理论分析。而本节课在落实这些基础知识的方法上则采用了创设情景、讨论、实验探究等能充分发挥学生主体作用的方式,围绕Fe3+的性质作了多角度、多层次、全方位的探索。
3.3化学复习课仍要具有鲜明的化学特色:
与生活实际的紧密联系和化学实验的灵活运用。紧密联系生活实际可使学生感到化学复习课仍然充满着新鲜感,从而提高学习化学的兴趣。
本节课在复习铁的氧化物时,让学生观察磁卡、磁带并检验其磁性,学生感到自己生活在化学世界中,从而觉得化学这门课很亲切;在课外作业中,布置了一道检验FeSO4药片是否变质及调查目前医院中治疗缺铁性贫血这种病的新药,让学生觉得化学与人类息息相关,学好化学可以造福人类,以及目前医药技术的突飞猛进,从中既进行了科学研究方法的渗透又培养了学生的社会责任感。本节课中对Fe3+的复习,通过精心的实验设计,让学生在观察多变的实验现象的乐趣中理解化学基础知识,并通过与思维定势的搏斗体会作为化学工作者应具有的实事求是的科学态度。
1 教学内容及设计意图
1.1教学内容分析
元素及其化合物知识的复习,在高三总复习中占有很大的比重,如何提高其复习的效率与效果是每一位化学教师都应探讨的课题。铁及其化合物这一内容在元素化合物知识中很有代表性,探索这一内容的复习方法对其它元素及其化合物的复习有一定的借鉴作用。
这一部分内容的知识点主要包括:铁在元素周期表中的位置、原子结构和性质;铁的氧化物、氢氧化物的性质、制备、用途;Fe2+、Fe3+离子的性质、互相转化及检验。在复习中,要充分发挥这三个知识点的载体作用,通过对知识的复习来提高学生的素质,培养学生的能力。
1.2设计意图
(1)元素及其化合物的复习要避免传统教学中为“巩固知识”而设计教学步骤的做法,应从“能力立意”的教学新理念出发,将“巩固知识”当作提高学生素质、培养学生能力的手段。
(2)课堂教学从两条主线同步展开
知识主线:铁的位置、结构、性质→铁化合物的性质、转化、用途→铁及其化合物知识的应用
能力主线:透过现象看本质(思维方法)→建立并完善认知结构(思维形式)→科学地探索未知世界(思维态度)
(3)让学生成为课堂的主角。教学过程中克服教师讲学生听、教师问学生答、教师出题学生做题的被动局面。教师的作用是创设情景,提供向导,在适当的时候进行纠错、把舵。
2 教学过程设计及实施
2.1 铁的位置、结构、性质
多媒体投影 元素周期表(Fe闪烁)
学生观察回答 Fe位于第四周期,第Ⅷ族。过渡元素的代表。
设问 从Fe元素在周期表中的位置分析,Fe 的原子结构有什么特点?根据Fe的原子结构特点分析,Fe单质应有哪些化学性质?
学生画图、分析、总结 结构特点 性 质 ①最外层仅有2个电子。 ②次外层不饱和。 FeO42-) 过渡元素原子结构特点 络合物[Fe(CO)5]
说明 知识主线:结构决定性质能力主线:透过现象看本质
2.2 铁及其化合物的关系
引导、设问 ①讨论一种元素的化合物,一般讨论它的哪几类物质?(学生回答:氧化物、氢氧化物、盐)②铁的氧化物、氢氧化物、盐有哪一些?(学生回答)③你能否用箭头科学地表示出它们之间的相互关系?
学生讨论、画图 要求注明各个箭头上的转化条件
投影、讲评 将学生画的图选3幅讨论,讲评,找出各自的优点。
设问 根据同学们画出的关系图,我们可以从哪些方面来复习呢?
投影生讨论教师总结 色态 色态 水解 价态 价态 性质 复分解 溶解性 溶解性 氧化—还原 制法 用途 络合
辅助教学 ①观察FeSO4溶液、FeCl3溶液颜色,并向其中滴加NaOH溶液;②观察废旧磁卡、牡丹卡、普通磁带,用磁铁试验其磁性。
说明 知识主线:Fe及其化合物的知识结构 横向——价态不变 纵向——价态变化能力主线:建立并完善认知结构(要求有序、科学)
2.3 知识应用
投影 (1)已知FeCl3的熔点为555K,沸点为588K,易溶于水,也易溶于乙醚、丙酮等有机溶剂中,据此分析,FeCl3应属于_____型化合物。
学生分析 从FeCl3的熔沸点、溶解性分析,它属于共价化合物。(它类似于AlCl3,气态时以Fe2Cl6分子形态存在。由性质推断结构是化学中常用的方法。)
投影 (2)常温下,1mol/L的FeCl3水溶性显_____性,离子反应方程式为____________________。常温下,有没有pH=7的FeCl3水溶液?化学实验室中应如何保存存FeCl3溶液?
学生实验并回答问题 学生测1mol/L的FeCl3溶液的pH值。书写离子方程式 Fe3++3H2O=Fe(OH)3+3H+,回答问题。
投影 (3)在Na2CO3溶液中滴加少量FeCl3溶液,可能看到什么现象?为什么?
学生实验分析原因 产生红褐色沉淀,有气泡冒出。分析原因:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑
投影、设问 在FeCl3溶液中滴加少量Na2CO3溶液,可能看到什么现象?分析原因。
学生实验并分析 产生红褐色沉淀,摇动后消失,有气泡冒出。原因:产生的Fe(OH)3溶解于过量的H+中(H+来自过量FeCl3的水解或为抑制其水解加入的少量HCl。
投影 (4)Na2S也是强碱弱酸盐,它和Na2CO3相似。在Na2S水溶液中滴入少量FeCl3溶液会看到什么现象?分析原因。 在FeCl3溶液中滴入少量的Na2S溶液,又会看到什么现象?请给出合理的解释。
学生实验 ③出现大量黑色沉淀②出现黑色沉淀,但很快就消失,溶液混浊。(这一结果大大出乎同学们的意料,大家非常兴奋)
设问 这黑色物质是何物?怎么生成的?如何证明你的想法?
学生讨论 ③大家思考并开展讨论。②请几位同学发言。
学生实验并解释 ③在产生黑色沉淀的试管中加入稀H2SO4,并闻气味。②现象:黑色沉淀消失,有淡黄色混浊,可以闻到臭鸡蛋味③解释:2Fe3++3S2-=2FeS↓+S↓ FeS+2H+=Fe2++H2S↑(有同学提出生成Fe2S3,则设问:Fe2S3能稳定地存在于水溶液中吗?)
投影 (5)FeCl3溶液中滴加KSCN溶液后,溶液呈现_____色,若再滴入NaCl溶液,溶液颜色变化为_____________。滴入NaF溶液后,溶液颜色变化为__________。分析原因。
学生实验 前者颜色几乎不变,后者明显变浅。
讨论分析 Fe3++6F-=[FeF6]3- ,生成的络合物[FeF6]3-稳定性比[Fe(SCN)]2+更强。使前一平衡向逆反应方向移动。
作业 已知某种硫酸盐可以用来治疗缺铁性贫血,制药厂在药片外包一层特制的糖衣,以防止它在空气中变质、失效。该药品的化学式为________________。①请你设计一个实验,以证明该药片是否变质。②请到附近医院调查一下,目前医院治疗缺铁性贫血主要有哪些药物?
说明 知识主线:铁及其化合物知识的应用能力主线:科学地探索未知世界
3.教学后记
3.1高三元素化合物的复习在知识处理上要做到:高屋建瓴,纵横联系。
高屋建瓴也就是在知识把握上必须大处着眼,对某一块知识,可先从知识分类上着手,对各类知识进行归纳总结。如铁及其化合物可从单质铁、铁的氧化物、铁的氢氧化物、铁的盐四个方面展开讨论。纵横联系就是在复习中要加强不同类知识间的横向联系和同类知识内的纵向联系。如铁及其化合物复习时,横向上强调四类物质间的转化规律(除铁外,其余三类转化价态不变),纵向上突出同一类物质间的价态变化规律。这样处理教学内容一方面使课的知识密度得到加大,而更重要的是使学生的认知结构得以完善。
3.2元素化合物复习在教学方法上应采用传统教学方法与现代教学方法的有机整合。
传统教学方法重视知识的巩固,在使用时易犯“炒冷饭”的毛病,而现代教学方法重视能力的培养,在使用时易犯“烧夹生饭”的毛病。只有两者有机整合,才能达到既巩固知识又培养能力的教学目标。本节课在知识复习上,十分重视双基的落实,如对Fe的性质的复习,从过渡元素的原子结构特征上作了深入的挖掘,对Fe2+ 、Fe3+的盐则从水解、氧化—还原、络合等方面作了理论分析。而本节课在落实这些基础知识的方法上则采用了创设情景、讨论、实验探究等能充分发挥学生主体作用的方式,围绕Fe3+的性质作了多角度、多层次、全方位的探索。
3.3化学复习课仍要具有鲜明的化学特色:
与生活实际的紧密联系和化学实验的灵活运用。紧密联系生活实际可使学生感到化学复习课仍然充满着新鲜感,从而提高学习化学的兴趣。
本节课在复习铁的氧化物时,让学生观察磁卡、磁带并检验其磁性,学生感到自己生活在化学世界中,从而觉得化学这门课很亲切;在课外作业中,布置了一道检验FeSO4药片是否变质及调查目前医院中治疗缺铁性贫血这种病的新药,让学生觉得化学与人类息息相关,学好化学可以造福人类,以及目前医药技术的突飞猛进,从中既进行了科学研究方法的渗透又培养了学生的社会责任感。本节课中对Fe3+的复习,通过精心的实验设计,让学生在观察多变的实验现象的乐趣中理解化学基础知识,并通过与思维定势的搏斗体会作为化学工作者应具有的实事求是的科学态度。
同课章节目录
