理综高三化学模拟(一)[下学期]
图片预览

文档简介
理综高三化学模拟(一)
6. 据报导我国科学家近年来研制出一种新型“连续纤维增韧”航空材料,其主要成分是由碳化硅、陶瓷和碳纤维复合而成。下列相关叙述不正确的是( )
A. 它耐高温抗氧化 B. 它比钢铁轻、硬,但质地较脆
C. 它没有固定熔点 D. 它是一种新型无机非金属材料
7. 下列事实不属于盐类水解应用的是( )
A. 明矾净水
B. 使用热的纯碱溶液去除油污
C. 实验室配制FeCl3溶液时加人少量稀盐酸
D. 实验室制氢气时加入少量CuSO4可加快反应速率
8. 对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了8个电子的结构。则一个三硫化四磷分子中含有的共价键个数是( )
A. 7个 B. 9个 C. 19个 D. 不能确定
9 A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物显碱性,且碱性B>A;C、D两种元素对应的气态氢化物的稳定性C>D;E是这五种元素的简单离子中半径最小的。则它们的原子序数由小到大的顺序是( )
A. B,A,C,D,E B. A,E,B,C,D
C. E,B,A,C,D D. B,A,E,D,C
10. 某溶液中只含有四种离子,下列说法正确的是( )
A. 若溶液中,则溶液一定呈中性
B. 溶液中不可能存在:
C. 若,溶液中不可能存在:
D. 若溶质为NaA、HA,则一定存在:
11. 已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)
主要:
次要:
(2)
主要:
次要:
则以下几种物质溶解度大小比较中,正确的是( )
A. B.
C. D.
12. 某有机物结构简式为,有关它的说法正确的是( )
A. 它属于芳香烃 B. 分子中最多有22个原子共面
C. 分子式为 D. 1mol该物质能与6mol H2加成
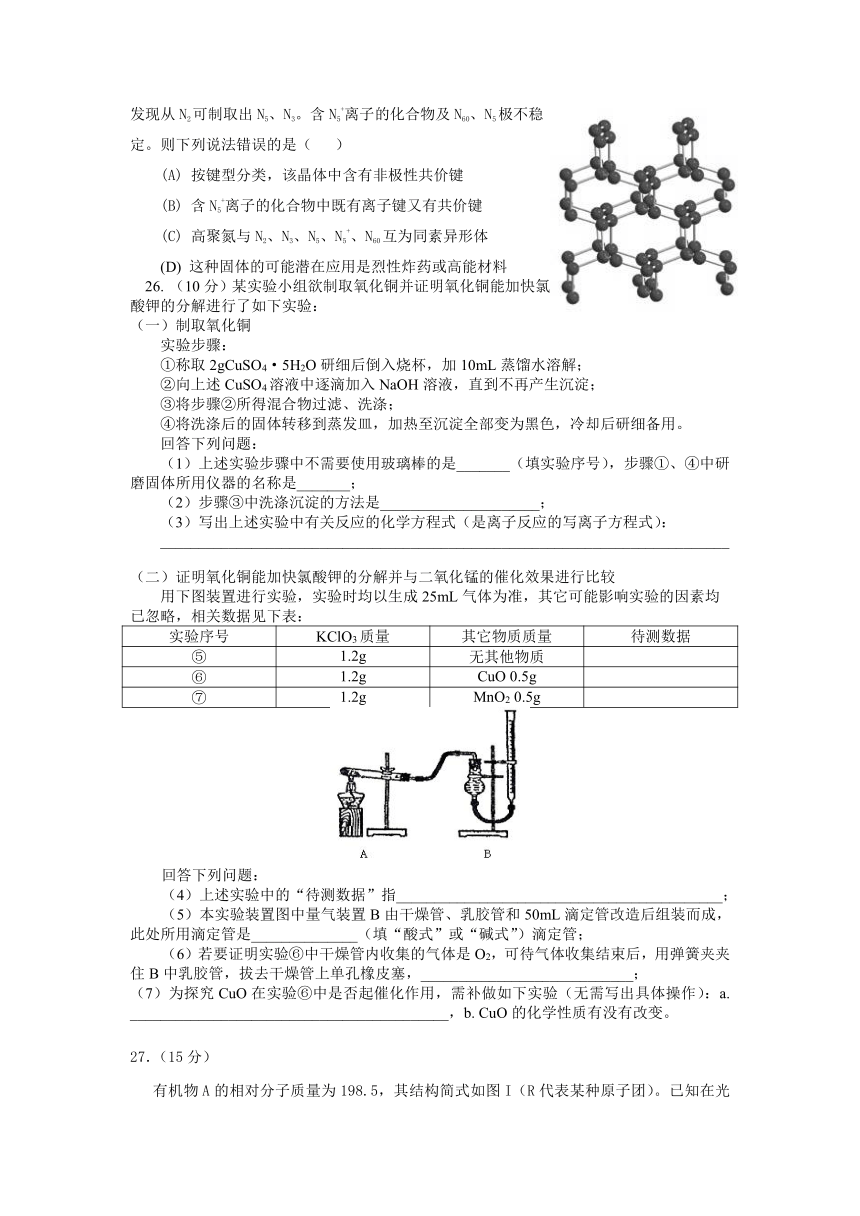
13.2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如右图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是( )
(A) 按键型分类,该晶体中含有非极性共价键
(B) 含N5+离子的化合物中既有离子键又有共价键
(C) 高聚氮与N2、N3、N5、N5+、N60互为同素异形体
(D) 这种固体的可能潜在应用是烈性炸药或高能材料
26. (10分)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解进行了如下实验:
(一)制取氧化铜
实验步骤:
①称取2gCuSO4·5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀;
③将步骤②所得混合物过滤、洗涤;
④将洗涤后的固体转移到蒸发皿,加热至沉淀全部变为黑色,冷却后研细备用。
回答下列问题:
(1)上述实验步骤中不需要使用玻璃棒的是_______(填实验序号),步骤①、④中研磨固体所用仪器的名称是_______;
(2)步骤③中洗涤沉淀的方法是_____________________;
(3)写出上述实验中有关反应的化学方程式(是离子反应的写离子方程式):
___________________________________________________________________________
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
用下图装置进行实验,实验时均以生成25mL气体为准,其它可能影响实验的因素均
已忽略,相关数据见下表:
实验序号 KClO3质量 其它物质质量 待测数据
⑤ 1.2g 无其他物质
⑥ 1.2g CuO 0.5g
⑦ 1.2g MnO2 0.5g
回答下列问题:
(4)上述实验中的“待测数据”指___________________________________________;
(5)本实验装置图中量气装置B由干燥管、乳胶管和50mL滴定管改造后组装而成,此处所用滴定管是______________(填“酸式”或“碱式”)滴定管;
(6)若要证明实验⑥中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,____________________________;
(7)为探究CuO在实验⑥中是否起催化作用,需补做如下实验(无需写出具体操作):a. __________________________________________,b. CuO的化学性质有没有改变。
27.(15分)
有机物A的相对分子质量为198.5,其结构简式如图I(R代表某种原子团)。已知在光照条件下,A分子中一个氢原子被氯原子取代只得到一种产物。A在一定条件下还有图II反应关系:
(1)请写出下列物质的结构简式
A______________________________ B_____________________________
(2)写出下列反应的化学方程式和指出其反应类型
C→D:________________________________________________________________;
反应类型:___________________________________
C→E:________________________________________________________________;
反应类型:___________________________________
E→F:________________________________________________________________;
反应类型:___________________________________
28. (9分)
A、B、C是中学化学中常见的三种元素的单质。A、B、C及其他物质之间的关系如下图所示,其中B、D、E、F溶液显酸性,又知常温下B为气态。
请回答下列问题:
(1)A、B、C三种单质的化学式(分子式)分别是A___________,B___________,C___________,其中A、C单质的晶体类型属于______________________。
(2)B与C反应生成E时观察到的现象是_________________________________。
(3)D和C反应生成E和F的离子方程式:______________________。
(4)在测定C的硫酸盐晶体结晶水含量实验中。若坩埚质量为m,坩埚与C的硫酸盐晶体总质量为,加热后称量坩埚与C的无水硫酸盐总质量为,则晶体中结晶水的质量分数ω=__________________(写计算式)。如果实验中加热温度过高致使固体出现黑色,则测定结果___________(填“偏高”,“偏低”,“不变”)。
29. (12分)
如下图装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。
(1)a为_________极,C极的电极反应式为:_____________________________。
(2)电解开始时,在B烧杯中央滴几滴淀粉溶液,你能观察到的现象为:___________
____________________________________________。
(3)当d极上产生标准状况下448mL气体时停止电解,a极上放出了___________ mol气体,若b极上沉积金属M的质量为4.32g,则金属M的摩尔质量为___________。
答案:6、B 7、D 8、B 9、D 10、A 11、D 12、D 13、C
26. (15分)
(1)②(2分) 研钵(2分)
(2)用少量水多次冲洗(2分)
(3)(2分)
(2分)
(4)生成25mL气体所用的时间(3分)
(5)碱式(2分)
(6)把带有余烬的木条放在干燥管口,木条复燃(2分)
(7)CuO的质量有没有改变(2分)
27.(15分)(1)A: B:
C→D:方程式略,缩聚反应;C→E:消去反应;E→F:加聚反应。
28. (18分,方程式3分,其余每空2分)
(1)A: B: C:;金属晶体
(2)铜丝在氯气中剧烈燃烧,有棕黄色烟。
(3)
(4)(3分) 偏高
29 (12分)
(1)阳(2分) (2分)
(2)c极附近的溶液首先变蓝色(2分)
(3)0.01 mol(3分) 108g/mol(3分)
6. 据报导我国科学家近年来研制出一种新型“连续纤维增韧”航空材料,其主要成分是由碳化硅、陶瓷和碳纤维复合而成。下列相关叙述不正确的是( )
A. 它耐高温抗氧化 B. 它比钢铁轻、硬,但质地较脆
C. 它没有固定熔点 D. 它是一种新型无机非金属材料
7. 下列事实不属于盐类水解应用的是( )
A. 明矾净水
B. 使用热的纯碱溶液去除油污
C. 实验室配制FeCl3溶液时加人少量稀盐酸
D. 实验室制氢气时加入少量CuSO4可加快反应速率
8. 对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了8个电子的结构。则一个三硫化四磷分子中含有的共价键个数是( )
A. 7个 B. 9个 C. 19个 D. 不能确定
9 A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物显碱性,且碱性B>A;C、D两种元素对应的气态氢化物的稳定性C>D;E是这五种元素的简单离子中半径最小的。则它们的原子序数由小到大的顺序是( )
A. B,A,C,D,E B. A,E,B,C,D
C. E,B,A,C,D D. B,A,E,D,C
10. 某溶液中只含有四种离子,下列说法正确的是( )
A. 若溶液中,则溶液一定呈中性
B. 溶液中不可能存在:
C. 若,溶液中不可能存在:
D. 若溶质为NaA、HA,则一定存在:
11. 已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)
主要:
次要:
(2)
主要:
次要:
则以下几种物质溶解度大小比较中,正确的是( )
A. B.
C. D.
12. 某有机物结构简式为,有关它的说法正确的是( )
A. 它属于芳香烃 B. 分子中最多有22个原子共面
C. 分子式为 D. 1mol该物质能与6mol H2加成
13.2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如右图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是( )
(A) 按键型分类,该晶体中含有非极性共价键
(B) 含N5+离子的化合物中既有离子键又有共价键
(C) 高聚氮与N2、N3、N5、N5+、N60互为同素异形体
(D) 这种固体的可能潜在应用是烈性炸药或高能材料
26. (10分)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解进行了如下实验:
(一)制取氧化铜
实验步骤:
①称取2gCuSO4·5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀;
③将步骤②所得混合物过滤、洗涤;
④将洗涤后的固体转移到蒸发皿,加热至沉淀全部变为黑色,冷却后研细备用。
回答下列问题:
(1)上述实验步骤中不需要使用玻璃棒的是_______(填实验序号),步骤①、④中研磨固体所用仪器的名称是_______;
(2)步骤③中洗涤沉淀的方法是_____________________;
(3)写出上述实验中有关反应的化学方程式(是离子反应的写离子方程式):
___________________________________________________________________________
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
用下图装置进行实验,实验时均以生成25mL气体为准,其它可能影响实验的因素均
已忽略,相关数据见下表:
实验序号 KClO3质量 其它物质质量 待测数据
⑤ 1.2g 无其他物质
⑥ 1.2g CuO 0.5g
⑦ 1.2g MnO2 0.5g
回答下列问题:
(4)上述实验中的“待测数据”指___________________________________________;
(5)本实验装置图中量气装置B由干燥管、乳胶管和50mL滴定管改造后组装而成,此处所用滴定管是______________(填“酸式”或“碱式”)滴定管;
(6)若要证明实验⑥中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,____________________________;
(7)为探究CuO在实验⑥中是否起催化作用,需补做如下实验(无需写出具体操作):a. __________________________________________,b. CuO的化学性质有没有改变。
27.(15分)
有机物A的相对分子质量为198.5,其结构简式如图I(R代表某种原子团)。已知在光照条件下,A分子中一个氢原子被氯原子取代只得到一种产物。A在一定条件下还有图II反应关系:
(1)请写出下列物质的结构简式
A______________________________ B_____________________________
(2)写出下列反应的化学方程式和指出其反应类型
C→D:________________________________________________________________;
反应类型:___________________________________
C→E:________________________________________________________________;
反应类型:___________________________________
E→F:________________________________________________________________;
反应类型:___________________________________
28. (9分)
A、B、C是中学化学中常见的三种元素的单质。A、B、C及其他物质之间的关系如下图所示,其中B、D、E、F溶液显酸性,又知常温下B为气态。
请回答下列问题:
(1)A、B、C三种单质的化学式(分子式)分别是A___________,B___________,C___________,其中A、C单质的晶体类型属于______________________。
(2)B与C反应生成E时观察到的现象是_________________________________。
(3)D和C反应生成E和F的离子方程式:______________________。
(4)在测定C的硫酸盐晶体结晶水含量实验中。若坩埚质量为m,坩埚与C的硫酸盐晶体总质量为,加热后称量坩埚与C的无水硫酸盐总质量为,则晶体中结晶水的质量分数ω=__________________(写计算式)。如果实验中加热温度过高致使固体出现黑色,则测定结果___________(填“偏高”,“偏低”,“不变”)。
29. (12分)
如下图装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。
(1)a为_________极,C极的电极反应式为:_____________________________。
(2)电解开始时,在B烧杯中央滴几滴淀粉溶液,你能观察到的现象为:___________
____________________________________________。
(3)当d极上产生标准状况下448mL气体时停止电解,a极上放出了___________ mol气体,若b极上沉积金属M的质量为4.32g,则金属M的摩尔质量为___________。
答案:6、B 7、D 8、B 9、D 10、A 11、D 12、D 13、C
26. (15分)
(1)②(2分) 研钵(2分)
(2)用少量水多次冲洗(2分)
(3)(2分)
(2分)
(4)生成25mL气体所用的时间(3分)
(5)碱式(2分)
(6)把带有余烬的木条放在干燥管口,木条复燃(2分)
(7)CuO的质量有没有改变(2分)
27.(15分)(1)A: B:
C→D:方程式略,缩聚反应;C→E:消去反应;E→F:加聚反应。
28. (18分,方程式3分,其余每空2分)
(1)A: B: C:;金属晶体
(2)铜丝在氯气中剧烈燃烧,有棕黄色烟。
(3)
(4)(3分) 偏高
29 (12分)
(1)阳(2分) (2分)
(2)c极附近的溶液首先变蓝色(2分)
(3)0.01 mol(3分) 108g/mol(3分)
同课章节目录
