物质的量课件[上学期]
图片预览






文档简介
课件16张PPT。想一想?1.你知道古代曹冲称象的故事吗?曹冲在称象时的主导思想是什么? 化整为零,化大为小2.已知托盘天平的最小刻度为0.1克,你能用它称量一粒大米的质量吗?你的主导思想又是什么?
积小成大,聚微为宏 微 观(分子数) 宏 观(质量)?2Na+2H2O=2NaOH+H2↑质 量: 46g 36g 40g 2g微粒数:2个 2个 2个 1个 化学反应中量的关系 科学上采用“物质的量”这个物理量把一定数目的原子、分子或离子等微观粒子与可称量的物质联系起来 。 宏 观(质量) 微 观(分子数)物质的量要想找到微观粒子的个数与宏观质量之间的关系,应该用什么指导思想?(阅读)课本P44页第1~2段回答下列问题:第三章 物质的量第一节 物质的量1.用什么微粒集体作为标准来衡量微观粒子的质量?
2.这个微粒集体的个数是多少?
3.表示这个微粒集体的物理量名称及其单位? 0.012kg12C中所含的碳原子数约6.02 × 1023个物质的量,其单位是摩尔第三章 物质的量第一节 物质的量一、物质的量
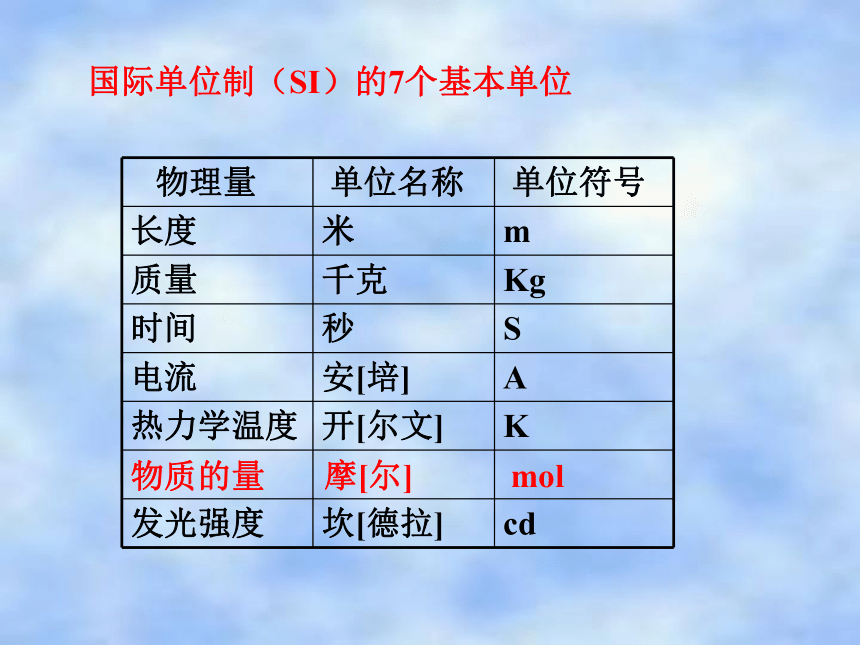
1.是一个物理量,是表示含有一定数目粒子的集合。符号是n,其单位是摩尔,简称(mol)。国际单位制(SI)的7个基本单位物质的量摩[尔]mol1.下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位【课堂练习】(阅读)课本P44页第3段回答下列问题:
1.什么叫阿伏加德罗常数?
2.1mol任何粒子含有多少个微粒数?第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-1【课堂练习】 2.判断正误,并说明理由。
A.1mol氢
B. 1mol CO2
C. 1mol大米错误。没有指出是分子、原子或离子正确。错误。大米不是微观粒子第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-14.使用摩尔时,必须指明粒子的种类,可以是分子、原子、离子、电子等微观粒子。【课堂练习】
3.填空:
(1)1mol O中含有 个O;
(2)1mol H2O中约含有 个H2O;
(3)1mol H+中约含有 个H+。4.根据摩尔的有关知识,进行下列计算:
(1)1.204 × 1024个H,合多少mol?
(2)5mol的O2中有多少个氧分子?
(3)N个水分子的物质的量是多少?(已知阿伏加
德罗常数为NA)2 mol3.01 × 1024N/NA6.02 × 10236.02 × 10236.02 × 1023第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-14.使用摩尔时,必须指明粒子的种类,可以是分子、原子、离子、电子等微观粒子。5.N=n × NA【课堂练习】
5.填空:
(1)0.5mol水中含有 个水分子。
(2)2mol水中含有 个水分子,
含有 个氢原子。
(3)1mol NaOH中含有 个NaOH分子,
含有 个氢氧根离子。
(4)1个水分子中有 个电子,
1molH2O中含有 个电子。3.01 × 10231.204 × 10242.408 × 10246.02 × 10236.02 × 1023106.02 × 1024第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-14.使用摩尔时,必须指明粒子的种类,可以是分子、原子、离子、电子等微观粒子。5.N=n × NA[小结]物质的量是一个基本物理量,单位为摩尔,它表示含有一定数目的粒子集体,1 mol物质含有阿伏加德罗常数个粒子。[推论]若微粒数相同,物质的量就相同,因此微粒数之比等于物质的量之比.【课堂练习】
6.在0.5molO2中含有的氧分子数目是多少?氧原子是多少?电子数目是多少?解:氧分子数目为
N1=n × NA
=0.5 ×6.02 ×1023 =3.01×1023
氧原子数目为
N2=2 n × NA =2 × 0.5 ×6.02 ×1023
= 6.02 ×1023
电子数目为
N3=16 × n × NA = 16 × 0.5 ×6.02 ×1023
= 4.816×1024【课堂练习】
1. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
2. 与0.3 mol H2O 含有相同氢原子数的是( )
A. 0.3 mol HNO3 B. 3.612 X 10 23个 HNO3分子
C. 0.2 mol H3PO4 D. 0.1mol NH3【课后思考】1mol12C的质量是0.012kg,那么1mol其他物质的质量又是多少呢?
【作业布置】《课课达标》P41
积小成大,聚微为宏 微 观(分子数) 宏 观(质量)?2Na+2H2O=2NaOH+H2↑质 量: 46g 36g 40g 2g微粒数:2个 2个 2个 1个 化学反应中量的关系 科学上采用“物质的量”这个物理量把一定数目的原子、分子或离子等微观粒子与可称量的物质联系起来 。 宏 观(质量) 微 观(分子数)物质的量要想找到微观粒子的个数与宏观质量之间的关系,应该用什么指导思想?(阅读)课本P44页第1~2段回答下列问题:第三章 物质的量第一节 物质的量1.用什么微粒集体作为标准来衡量微观粒子的质量?
2.这个微粒集体的个数是多少?
3.表示这个微粒集体的物理量名称及其单位? 0.012kg12C中所含的碳原子数约6.02 × 1023个物质的量,其单位是摩尔第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。符号是n,其单位是摩尔,简称(mol)。国际单位制(SI)的7个基本单位物质的量摩[尔]mol1.下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位【课堂练习】(阅读)课本P44页第3段回答下列问题:
1.什么叫阿伏加德罗常数?
2.1mol任何粒子含有多少个微粒数?第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-1【课堂练习】 2.判断正误,并说明理由。
A.1mol氢
B. 1mol CO2
C. 1mol大米错误。没有指出是分子、原子或离子正确。错误。大米不是微观粒子第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-14.使用摩尔时,必须指明粒子的种类,可以是分子、原子、离子、电子等微观粒子。【课堂练习】
3.填空:
(1)1mol O中含有 个O;
(2)1mol H2O中约含有 个H2O;
(3)1mol H+中约含有 个H+。4.根据摩尔的有关知识,进行下列计算:
(1)1.204 × 1024个H,合多少mol?
(2)5mol的O2中有多少个氧分子?
(3)N个水分子的物质的量是多少?(已知阿伏加
德罗常数为NA)2 mol3.01 × 1024N/NA6.02 × 10236.02 × 10236.02 × 1023第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-14.使用摩尔时,必须指明粒子的种类,可以是分子、原子、离子、电子等微观粒子。5.N=n × NA【课堂练习】
5.填空:
(1)0.5mol水中含有 个水分子。
(2)2mol水中含有 个水分子,
含有 个氢原子。
(3)1mol NaOH中含有 个NaOH分子,
含有 个氢氧根离子。
(4)1个水分子中有 个电子,
1molH2O中含有 个电子。3.01 × 10231.204 × 10242.408 × 10246.02 × 10236.02 × 1023106.02 × 1024第三章 物质的量第一节 物质的量一、物质的量
1.是一个物理量,是表示含有一定数目粒子的集合。
符号是n,其单位是摩尔,简称摩(mol)。2.1mol粒子的数目是0.012kg12C中所含的碳原子数目,约为6.02 × 1023 个
3. 1mol粒子的数目又叫阿伏加德罗常数,符号为NA,单位mol-14.使用摩尔时,必须指明粒子的种类,可以是分子、原子、离子、电子等微观粒子。5.N=n × NA[小结]物质的量是一个基本物理量,单位为摩尔,它表示含有一定数目的粒子集体,1 mol物质含有阿伏加德罗常数个粒子。[推论]若微粒数相同,物质的量就相同,因此微粒数之比等于物质的量之比.【课堂练习】
6.在0.5molO2中含有的氧分子数目是多少?氧原子是多少?电子数目是多少?解:氧分子数目为
N1=n × NA
=0.5 ×6.02 ×1023 =3.01×1023
氧原子数目为
N2=2 n × NA =2 × 0.5 ×6.02 ×1023
= 6.02 ×1023
电子数目为
N3=16 × n × NA = 16 × 0.5 ×6.02 ×1023
= 4.816×1024【课堂练习】
1. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
2. 与0.3 mol H2O 含有相同氢原子数的是( )
A. 0.3 mol HNO3 B. 3.612 X 10 23个 HNO3分子
C. 0.2 mol H3PO4 D. 0.1mol NH3【课后思考】1mol12C的质量是0.012kg,那么1mol其他物质的质量又是多少呢?
【作业布置】《课课达标》P41
