物质的量第一课时[上学期]
文档属性
| 名称 | 物质的量第一课时[上学期] |  | |
| 格式 | rar | ||
| 文件大小 | 377.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2005-12-21 10:14:00 | ||
图片预览







文档简介
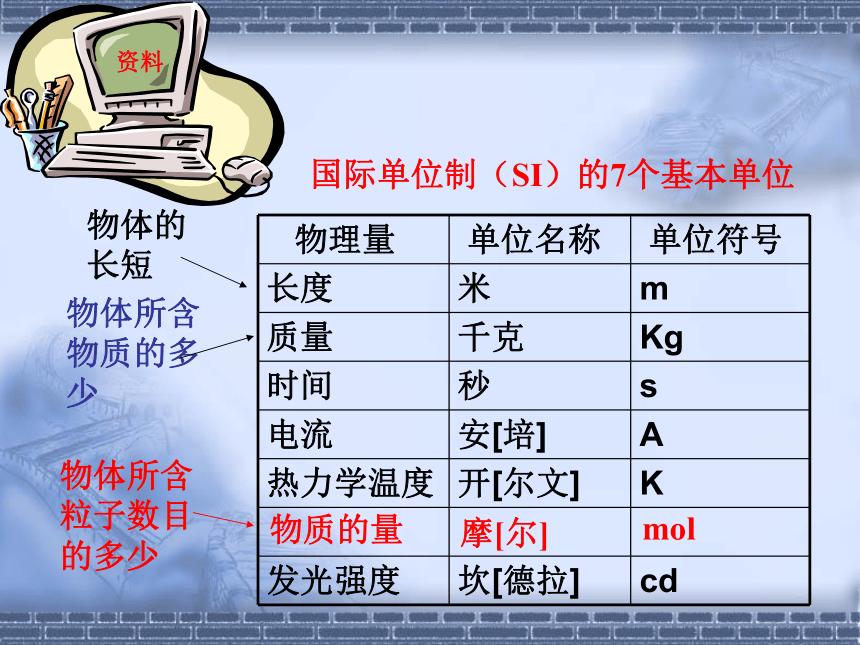
课件23张PPT。第一节 物质的量给你足够多的米和一台托盘天平,假设每一粒米都相同,如何称取一粒米的质量?取一些大米称其质量,并数出大米粒数,再计算每一粒大米的质量。 宏 观(质量) 微 观(粒子数)物质的量对较小的物质扩大倍数形成一定数目的集体,我们就可以称量了回顾:我们学过哪些物理量?它们的单位是什么?物理量 单位质量 千克长度 米时间 秒电流强度 安培资料国际单位制(SI)的7个基本单位物质的量摩[尔]mol是国际单位制七个基本物理量之一。 是表示含有一定数目微观粒子的集体,符号为n 。{分子、原子、离子、电子、质子等 “物质的量”是一个整体,不可拆开 物质的量的单位是 摩尔物质的量下列叙述中,正确的是( )
A.物质的量就是物质的质量,也是指物质
的数量
B.物质的量可以改为物质量
C.物质的量是国际单位制中的一个物理量
D.物质的量是描述物质所含粒子数目多少
的单位C思考题 摩 尔* 是物质的量的单位,符号为mol 。注 意 使用时必须指明是哪一种粒子仅用于计量微观粒子 判断下列说法是否正确。
(A)1 mol氧
(B)1 mol氧原子
(C)3 mol 水
(D)1mol小米
(E)1 mol氧元素思考:错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子正确 ,表示为1mol O正确,表示为 3mol H2O错误,物质的量仅用于计量微观粒子错误,元素是表示宏观的[疑问]
1mol的标准是什么?
(既1mol表示的粒子数目多少?)生活小常识12支一打铅笔 阿伏加德罗常数:12克12C中含有的碳原子数。1摩尔任何粒子的粒子数叫做阿伏加德罗常数。单位:mol-16个质子和6个中子意大利物理学家符号:NA规定:12克 12CC原子数?已知:一个12C的质量为 1.993 × 10-26kg
求: 0.012Kg 12C 中所含的碳原子数?[思考]解:≈ 6.02×1023 0.012Kg1.993 × 10-26Kg碳原子数=[思考]6.02 × 1023 等于阿伏加德罗常数吗?[归纳]阿伏加徳罗常数:规定: 12克12C中所含的碳原子的个数。近似值: 6.02ㄨ1023个微粒。1摩尔任何粒子的粒子数下列关于阿伏加德罗常数的说法正确的是
( )
A、阿伏加德罗常数是一个纯数,没有单位
B、阿伏加德罗常数就是6.02×1023个粒子
C、阿伏加德罗常数是指1 mol的任何粒子
的粒子数
D、阿伏加德罗常数的近似值:
6.02×1023 mol-1CD1mol粒子的粒子数0.012Kg12C中所含原子数阿伏加德罗常数6.02×1023约为约为约为对于0.012Kg 12C,下列说法错误的是( )
A.含有阿伏加德罗常数个碳原子
B.含有1摩尔12C原子
C.含6.02×1023个12C原子
D.摩尔的标准是0.012Kg12C中所含的原子数目C问题探究(1)1molO2中约含有多少个氧气分子?
(2)2molO2中约含有多少个氧气分子?
(3)a molO2中约含有多少个氧气分子?
6.02 × 1023 2 × 6.02 × 1023a × 6.02 × 1023阿伏加德罗常数微粒个数物质的量NNA n× = 1 摩尔水分子中有多少摩尔氢原子,多少摩尔氧原子? H2O 11 molNA2HO212NANA1 mol2 mol 结论:微粒之间的个数之比也就是物质的量之比微粒个数微粒集团物质的量 1mol H2O中含有 mol水分子,
含有 mol氧原子,
含有 mol氢原子,
含有 mol原子,
含有 mol电子。112103练习练习21mol O2中含有 个氧原子,
约含有 个氧原子;
1mol H2O中约含有 个水分子,
约含有 个氧原子,
约含有 个氢原子,
约含有 个原子,
约含有 个电子。
2NA1.204×10246.02×10231.204×10246.02×10236.02×10241.806×1024巩固练习下列物质所含有的原子个数为阿伏加德罗常数的是 ( )
A、1mol Cl2
B、0.5 mol CO2
C、0.5 mol H2
D、0.25mol SO3 CD小结物质的量(n)摩尔阿伏加德罗常数(NA):表示含有一定数目粒子集体的物理量:是物质的量的单位,符号为mol:是0.012 千克12C所含的碳原子数
约为6.02 × 1023换算公式
A.物质的量就是物质的质量,也是指物质
的数量
B.物质的量可以改为物质量
C.物质的量是国际单位制中的一个物理量
D.物质的量是描述物质所含粒子数目多少
的单位C思考题 摩 尔* 是物质的量的单位,符号为mol 。注 意 使用时必须指明是哪一种粒子仅用于计量微观粒子 判断下列说法是否正确。
(A)1 mol氧
(B)1 mol氧原子
(C)3 mol 水
(D)1mol小米
(E)1 mol氧元素思考:错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子正确 ,表示为1mol O正确,表示为 3mol H2O错误,物质的量仅用于计量微观粒子错误,元素是表示宏观的[疑问]
1mol的标准是什么?
(既1mol表示的粒子数目多少?)生活小常识12支一打铅笔 阿伏加德罗常数:12克12C中含有的碳原子数。1摩尔任何粒子的粒子数叫做阿伏加德罗常数。单位:mol-16个质子和6个中子意大利物理学家符号:NA规定:12克 12CC原子数?已知:一个12C的质量为 1.993 × 10-26kg
求: 0.012Kg 12C 中所含的碳原子数?[思考]解:≈ 6.02×1023 0.012Kg1.993 × 10-26Kg碳原子数=[思考]6.02 × 1023 等于阿伏加德罗常数吗?[归纳]阿伏加徳罗常数:规定: 12克12C中所含的碳原子的个数。近似值: 6.02ㄨ1023个微粒。1摩尔任何粒子的粒子数下列关于阿伏加德罗常数的说法正确的是
( )
A、阿伏加德罗常数是一个纯数,没有单位
B、阿伏加德罗常数就是6.02×1023个粒子
C、阿伏加德罗常数是指1 mol的任何粒子
的粒子数
D、阿伏加德罗常数的近似值:
6.02×1023 mol-1CD1mol粒子的粒子数0.012Kg12C中所含原子数阿伏加德罗常数6.02×1023约为约为约为对于0.012Kg 12C,下列说法错误的是( )
A.含有阿伏加德罗常数个碳原子
B.含有1摩尔12C原子
C.含6.02×1023个12C原子
D.摩尔的标准是0.012Kg12C中所含的原子数目C问题探究(1)1molO2中约含有多少个氧气分子?
(2)2molO2中约含有多少个氧气分子?
(3)a molO2中约含有多少个氧气分子?
6.02 × 1023 2 × 6.02 × 1023a × 6.02 × 1023阿伏加德罗常数微粒个数物质的量NNA n× = 1 摩尔水分子中有多少摩尔氢原子,多少摩尔氧原子? H2O 11 molNA2HO212NANA1 mol2 mol 结论:微粒之间的个数之比也就是物质的量之比微粒个数微粒集团物质的量 1mol H2O中含有 mol水分子,
含有 mol氧原子,
含有 mol氢原子,
含有 mol原子,
含有 mol电子。112103练习练习21mol O2中含有 个氧原子,
约含有 个氧原子;
1mol H2O中约含有 个水分子,
约含有 个氧原子,
约含有 个氢原子,
约含有 个原子,
约含有 个电子。
2NA1.204×10246.02×10231.204×10246.02×10236.02×10241.806×1024巩固练习下列物质所含有的原子个数为阿伏加德罗常数的是 ( )
A、1mol Cl2
B、0.5 mol CO2
C、0.5 mol H2
D、0.25mol SO3 CD小结物质的量(n)摩尔阿伏加德罗常数(NA):表示含有一定数目粒子集体的物理量:是物质的量的单位,符号为mol:是0.012 千克12C所含的碳原子数
约为6.02 × 1023换算公式
