1.4 常见的碱 (第1课时)(课件 29张ppt)
文档属性
| 名称 | 1.4 常见的碱 (第1课时)(课件 29张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2018-12-04 00:00:00 | ||
图片预览








文档简介
第4节
常见的碱
浙教版科学九年级上册第一章
第1课时
学习目标:
1.通过氢氧化钠和氢氧化钙的物理性质和化学性质推
导碱的共性。
2.学会用碱的有关性质解释有关生活现象。
碱有哪些性质呢?
提示:对一类物质中的典型物质进行分析,归纳共性。
例如:研究酸的性质时,分析盐酸、硫酸得出。
提示:用对比实验的方法寻找物质的特性,得出个性。
例如:盐酸中的氯离子、硫酸中硫酸根离子。
物质的变 化
物质的
性 质
归纳
物质的
用 途
推测
一、碱的共性
1.用酸碱指示剂
滴定氢氧化钠
溶液和石灰水,
观察颜色变化?
2.用pH试纸试验,
氢氧化钠溶液和
石灰水的pH值?
变红色
变蓝色
变红色
变蓝色
蓝色pH > 7
蓝色pH > 7
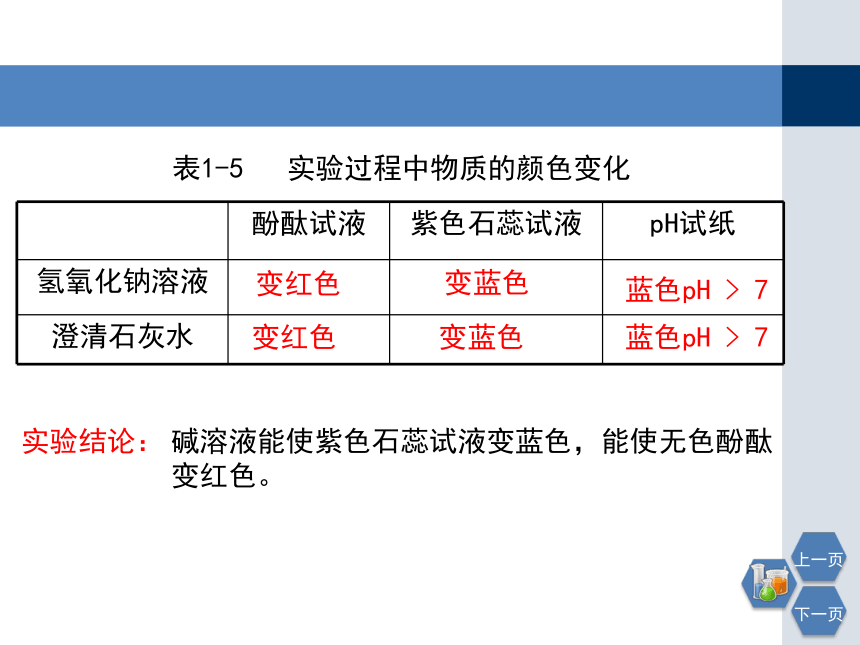
表1-5 实验过程中物质的颜色变化
实验结论:
碱溶液能使紫色石蕊试液变蓝色,能使无色酚酞变红色。
酚酞试液 紫色石蕊试液 pH试纸
氢氧化钠溶液
澄清石灰水
这里为什么要说成“碱溶液”,而不直接说成“碱”?
因为有些碱不能溶于水,如氢氧化铜、氢氧化铁,由于不溶于水,它们不能使紫色石蕊试液、无色酚酞试液变色。
1.碱溶液与酸碱指示剂作用
生产硫酸的工厂排放的废气里含有污染环境的二氧化硫,如果将废气通过氢氧化钠溶液,可大大减少二氧化硫的含量。
化学方程式:
2.可溶性碱与酸性气体(非金属氧化物)反应
SO2
+
NaOH
Na2SO3
=
H2O
+
2
亚硫酸钠
工业上常用碱溶液来吸收酸性气体。如:SO3
二氧化碳通入澄清石灰水,石灰水变浑浊。
化学方程式:
CO2
+
Ca(OH)2
CaCO3
=
H2O
+
化学方程式:
SO3
+
NaOH
Na2SO4
=
H2O
+
2
盛放氢氧化钠溶液的试剂瓶不能用玻璃瓶盖,要用橡胶瓶盖或木塞。已知玻璃的主要成分是二氧化硅。你知道这是为什么吗?
SiO2
+
NaOH
Na2SiO3
=
H2O
+
2
硅酸钠
如果用玻璃瓶盖,玻璃的主要成分是二氧化硅要与氢氧化钠溶液反应,久置会与瓶子粘连。
化学方程式:
氢氧化钠固体或氢氧化钠溶液不能敞口放置,这是为什么?
CO2
+
NaOH
Na2CO3
=
H2O
+
2
氢氧化钠会与空气中的CO2发生反应
3.可溶性碱与某些盐溶液反应
1.在2支试管中分别注入2~3毫升氯化铜溶液和氯化铁溶液,它们各显什么颜色?
氯化铜溶液呈蓝色;
氯化铁溶液呈黄色。
2.在上述2支试管中分别加入1~2毫升氢氧化钠溶液,试
管中发生了什么变化?
盛有氯化铜溶液的试管中产生了蓝色絮状沉淀;
盛有氯化铁溶液的试管中产生了红褐色沉淀。
化学方程式:
CuCl2
+
NaOH
Cu(OH)2
=
NaCl
+
2
2
FeCl3
+
NaOH
Fe(OH)3
=
NaCl
+
3
3
3.在2支试管中各加入3毫升氢氧化钙溶液,然后分别滴加数滴碳酸钠溶液和氯化铁溶液,观察有什么变化发生。
加碳酸钠溶液的试管中有白色沉淀生成;
加氯化铁溶液的试管中有红褐色沉淀生成。
化学方程式:
Na2CO3
+
Ca(OH)2
CaCO3
=
NaOH
+
2
FeCl3
+
Ca(OH)2
CaCl2
=
Fe(OH)3
+
3
2
2
3
1. 在2支试管中各加入3毫升氢氧化钙溶液,滴加无色酚酞试液,观察颜色变化?然后分别滴加盐酸和硫酸,观察有什么变化?
无色酚酞试液变红色;
滴加盐酸和硫酸后,红色逐渐消失;
4.碱与酸溶液发生反应
化学方程式:
HCl
+
Ca(OH)2
CaCl2
=
H2O
+
2
2
H2SO4
+
Ca(OH)2
CaSO4
=
H2O
+
2
可以用复方氢氧化铝的药片治疗胃酸过多
Al(OH)3
+
HCl
H2O
=
AlCl3
+
3
3
2. 把前面反应中生成的氢氧化铜及氢氧化铁沉淀分成2份,分别滴加盐酸和硫酸,观察有什么变化?
氢氧化铜蓝色絮状沉淀逐渐消失,溶液变蓝色;
氢氧化铁红棕色沉淀逐渐消失,溶液变黄色;
化学方程式:
HCl
+
Cu(OH)2
CuCl2
=
H2O
+
2
2
H2SO4
+
Cu(OH)2
CuSO4
=
H2O
+
2
HCl
+
Fe(OH)3
FeCl3
=
H2O
+
2
6
H2SO4
+
Fe(OH)3
Fe2(SO4)3
=
H2O
+
2
2
3
3
3
为什么氢氧化钠、氢氧化钙具有相似的性质?
氢氧化钠、氢氧化钙及其他可溶性碱,因为都含有氢氧根离子(OH-),所以具有相似的性质。
你能总结出可溶性碱的化学性质了吗?
(一)可溶性碱的通性
1.可溶性碱与酸碱指示剂作用
2.可溶性碱与非金属氧化物反应
能使紫色石蕊试液变蓝色,
能使无色酚酞变红色。
可溶性碱
+
非金属氧化物
盐
+
水
3.碱与酸溶液发生反应
(所有)碱
+
酸
盐
+
水
4.可溶性碱与某些盐溶液反应
可溶性碱
+
(可溶性)盐
新盐
+
新碱
以氢氧化钡为例,用化学方程式表示可溶性碱的化学性质。
CO2
+
Ba(OH)2
BaCO3
=
H2O
+
H2SO4
+
Ba(OH)2
BaSO4
=
H2O
+
2
Na2CO3
+
Ba(OH)2
BaCO3
=
NaOH
+
2
(二)不溶性碱的共性
1.不溶性碱与酸溶液发生反应
H2SO4
+
Cu(OH)2
CuSO4
=
H2O
+
2
HCl
+
Fe(OH)3
FeCl3
=
H2O
+
2
6
2
3
2.不溶性碱受热分解
Cu(OH)2
=
CuO
H2O
+
Fe(OH)3
=
Fe2O3
H2O
+
2
3
不可溶性碱
金属氧化物
+
水
2. 盛石灰水的试剂瓶存放的时间久了,内壁常附有一层白膜,要洗去这层白膜最好的方法是( )
A.用水洗 B.用氢氧化钠溶液洗
C.用盐酸洗 D.先用盐酸,再用水洗
1. 用一种试剂就能区分盐酸、食盐溶液、澄清石灰水,这种试剂是( )
A.酚酞 B.石蕊试液
C.氯化铁溶液 D.氢氧化钠溶液
B
D
3. 下列物质露置在空气中,会发生反应且质量增加的是( )
A、氢氧化钠 B、浓盐酸
C、浓硫酸 D、氯化钠晶体
A
4. 氨水是一种碱,它的化学式为NH3·H2O(NH4OH)它能与二氧化碳反应生成碳酸氢铵,请写出该反应的化学方程式。有人称它为“气肥”,你知道这是为什么吗?
NH3·H2O
+
CO2
=
NH4HCO3
NH4HCO3
=
NH3
+
CO2
+
H2O
5.将集满CO2的大试管倒插入滴有酚酞的石灰水中,看到的现象是什么?原因是什么?
红色逐渐消失,石灰水变浑浊,试管液面上升。
生成CaCO3沉淀,且管内体积减少气压降低
End
Thank
you
常见的碱
浙教版科学九年级上册第一章
第1课时
学习目标:
1.通过氢氧化钠和氢氧化钙的物理性质和化学性质推
导碱的共性。
2.学会用碱的有关性质解释有关生活现象。
碱有哪些性质呢?
提示:对一类物质中的典型物质进行分析,归纳共性。
例如:研究酸的性质时,分析盐酸、硫酸得出。
提示:用对比实验的方法寻找物质的特性,得出个性。
例如:盐酸中的氯离子、硫酸中硫酸根离子。
物质的变 化
物质的
性 质
归纳
物质的
用 途
推测
一、碱的共性
1.用酸碱指示剂
滴定氢氧化钠
溶液和石灰水,
观察颜色变化?
2.用pH试纸试验,
氢氧化钠溶液和
石灰水的pH值?
变红色
变蓝色
变红色
变蓝色
蓝色pH > 7
蓝色pH > 7
表1-5 实验过程中物质的颜色变化
实验结论:
碱溶液能使紫色石蕊试液变蓝色,能使无色酚酞变红色。
酚酞试液 紫色石蕊试液 pH试纸
氢氧化钠溶液
澄清石灰水
这里为什么要说成“碱溶液”,而不直接说成“碱”?
因为有些碱不能溶于水,如氢氧化铜、氢氧化铁,由于不溶于水,它们不能使紫色石蕊试液、无色酚酞试液变色。
1.碱溶液与酸碱指示剂作用
生产硫酸的工厂排放的废气里含有污染环境的二氧化硫,如果将废气通过氢氧化钠溶液,可大大减少二氧化硫的含量。
化学方程式:
2.可溶性碱与酸性气体(非金属氧化物)反应
SO2
+
NaOH
Na2SO3
=
H2O
+
2
亚硫酸钠
工业上常用碱溶液来吸收酸性气体。如:SO3
二氧化碳通入澄清石灰水,石灰水变浑浊。
化学方程式:
CO2
+
Ca(OH)2
CaCO3
=
H2O
+
化学方程式:
SO3
+
NaOH
Na2SO4
=
H2O
+
2
盛放氢氧化钠溶液的试剂瓶不能用玻璃瓶盖,要用橡胶瓶盖或木塞。已知玻璃的主要成分是二氧化硅。你知道这是为什么吗?
SiO2
+
NaOH
Na2SiO3
=
H2O
+
2
硅酸钠
如果用玻璃瓶盖,玻璃的主要成分是二氧化硅要与氢氧化钠溶液反应,久置会与瓶子粘连。
化学方程式:
氢氧化钠固体或氢氧化钠溶液不能敞口放置,这是为什么?
CO2
+
NaOH
Na2CO3
=
H2O
+
2
氢氧化钠会与空气中的CO2发生反应
3.可溶性碱与某些盐溶液反应
1.在2支试管中分别注入2~3毫升氯化铜溶液和氯化铁溶液,它们各显什么颜色?
氯化铜溶液呈蓝色;
氯化铁溶液呈黄色。
2.在上述2支试管中分别加入1~2毫升氢氧化钠溶液,试
管中发生了什么变化?
盛有氯化铜溶液的试管中产生了蓝色絮状沉淀;
盛有氯化铁溶液的试管中产生了红褐色沉淀。
化学方程式:
CuCl2
+
NaOH
Cu(OH)2
=
NaCl
+
2
2
FeCl3
+
NaOH
Fe(OH)3
=
NaCl
+
3
3
3.在2支试管中各加入3毫升氢氧化钙溶液,然后分别滴加数滴碳酸钠溶液和氯化铁溶液,观察有什么变化发生。
加碳酸钠溶液的试管中有白色沉淀生成;
加氯化铁溶液的试管中有红褐色沉淀生成。
化学方程式:
Na2CO3
+
Ca(OH)2
CaCO3
=
NaOH
+
2
FeCl3
+
Ca(OH)2
CaCl2
=
Fe(OH)3
+
3
2
2
3
1. 在2支试管中各加入3毫升氢氧化钙溶液,滴加无色酚酞试液,观察颜色变化?然后分别滴加盐酸和硫酸,观察有什么变化?
无色酚酞试液变红色;
滴加盐酸和硫酸后,红色逐渐消失;
4.碱与酸溶液发生反应
化学方程式:
HCl
+
Ca(OH)2
CaCl2
=
H2O
+
2
2
H2SO4
+
Ca(OH)2
CaSO4
=
H2O
+
2
可以用复方氢氧化铝的药片治疗胃酸过多
Al(OH)3
+
HCl
H2O
=
AlCl3
+
3
3
2. 把前面反应中生成的氢氧化铜及氢氧化铁沉淀分成2份,分别滴加盐酸和硫酸,观察有什么变化?
氢氧化铜蓝色絮状沉淀逐渐消失,溶液变蓝色;
氢氧化铁红棕色沉淀逐渐消失,溶液变黄色;
化学方程式:
HCl
+
Cu(OH)2
CuCl2
=
H2O
+
2
2
H2SO4
+
Cu(OH)2
CuSO4
=
H2O
+
2
HCl
+
Fe(OH)3
FeCl3
=
H2O
+
2
6
H2SO4
+
Fe(OH)3
Fe2(SO4)3
=
H2O
+
2
2
3
3
3
为什么氢氧化钠、氢氧化钙具有相似的性质?
氢氧化钠、氢氧化钙及其他可溶性碱,因为都含有氢氧根离子(OH-),所以具有相似的性质。
你能总结出可溶性碱的化学性质了吗?
(一)可溶性碱的通性
1.可溶性碱与酸碱指示剂作用
2.可溶性碱与非金属氧化物反应
能使紫色石蕊试液变蓝色,
能使无色酚酞变红色。
可溶性碱
+
非金属氧化物
盐
+
水
3.碱与酸溶液发生反应
(所有)碱
+
酸
盐
+
水
4.可溶性碱与某些盐溶液反应
可溶性碱
+
(可溶性)盐
新盐
+
新碱
以氢氧化钡为例,用化学方程式表示可溶性碱的化学性质。
CO2
+
Ba(OH)2
BaCO3
=
H2O
+
H2SO4
+
Ba(OH)2
BaSO4
=
H2O
+
2
Na2CO3
+
Ba(OH)2
BaCO3
=
NaOH
+
2
(二)不溶性碱的共性
1.不溶性碱与酸溶液发生反应
H2SO4
+
Cu(OH)2
CuSO4
=
H2O
+
2
HCl
+
Fe(OH)3
FeCl3
=
H2O
+
2
6
2
3
2.不溶性碱受热分解
Cu(OH)2
=
CuO
H2O
+
Fe(OH)3
=
Fe2O3
H2O
+
2
3
不可溶性碱
金属氧化物
+
水
2. 盛石灰水的试剂瓶存放的时间久了,内壁常附有一层白膜,要洗去这层白膜最好的方法是( )
A.用水洗 B.用氢氧化钠溶液洗
C.用盐酸洗 D.先用盐酸,再用水洗
1. 用一种试剂就能区分盐酸、食盐溶液、澄清石灰水,这种试剂是( )
A.酚酞 B.石蕊试液
C.氯化铁溶液 D.氢氧化钠溶液
B
D
3. 下列物质露置在空气中,会发生反应且质量增加的是( )
A、氢氧化钠 B、浓盐酸
C、浓硫酸 D、氯化钠晶体
A
4. 氨水是一种碱,它的化学式为NH3·H2O(NH4OH)它能与二氧化碳反应生成碳酸氢铵,请写出该反应的化学方程式。有人称它为“气肥”,你知道这是为什么吗?
NH3·H2O
+
CO2
=
NH4HCO3
NH4HCO3
=
NH3
+
CO2
+
H2O
5.将集满CO2的大试管倒插入滴有酚酞的石灰水中,看到的现象是什么?原因是什么?
红色逐渐消失,石灰水变浑浊,试管液面上升。
生成CaCO3沉淀,且管内体积减少气压降低
End
Thank
you
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
