来自石油和煤的两种基本化工原料[下学期]
文档属性
| 名称 | 来自石油和煤的两种基本化工原料[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-05-24 00:00:00 | ||
图片预览










文档简介
课件55张PPT。来自石油和煤的两种基本化工原料揭西县棉湖中学
林喜信
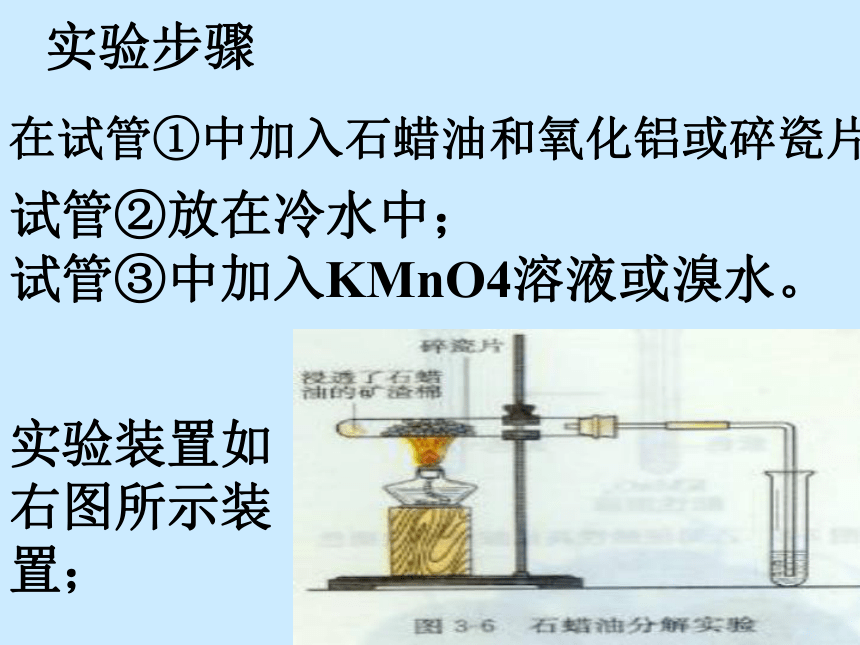
2006年5月第三章 有机化合物第一课时 教学目标 1.烯烃的概念; 2.乙烯的分子结构及性质、用途; 3.强化学生对“结构─性质”关系的认识,培养学生的比较思维能力。思考与交流1.乙烯的用途一、乙烯水果催熟剂乙烯的产量是衡量一个国家的石油化工水平2.乙烯的供求状况总投资193亿元年产乙烯600万吨科学探究---用石蜡油制备乙烯实验步骤在试管①中加入石蜡油和氧化铝或碎瓷片;试管②放在冷水中;试管③中加入KMnO4溶液或溴水。实验装置如右图所示装置;实验要点:(1)石棉要尽量多吸收石蜡油。(2)石蜡油分解反应的温度要在500 ℃以上。(3)实验中要注意防止倒吸;(4)KMnO4用稀溶液,3 mL该溶液中一般加入
2~3滴稀H2SO4溶液,增加KMnO4溶液的氧化性。(5)配制溴的四氯化碳溶液时,20 mL
四氯化碳加1~2滴溴即可。用石蜡油制备乙烯探究实验:石蜡油分解实验
(1)加热分解石蜡油,观察现象;
(2)将产生的气体分别通入溴的四氯化碳溶液、高锰酸钾溶液,观察现象;
(3)用排水集气法收集一试管气体,点燃,观察燃烧的情况。 现象1)加热石蜡油分解产生无色气体3)气体通入溴的四氯化碳溶液溶液红棕色褪去2)、气体通酸性高锰酸钾溶液溶液紫色褪去4)将收集到的气体产物点燃火焰明亮并伴有黑烟思考 产生的气体是烷烃吗?为什么溴的四氯化碳溶液、高锰酸钾溶液会褪色?这种物质与烷烃的结构有什么差异性? 产生的气体不完全为烷烃,有与烷烃性质不同的烃,因为烷烃不能使溴的四氯化碳溶液、高锰酸钾溶液会褪色。石蜡油分解产物主要是烷烃和乙烯CCH H H H ....::.:.乙烯的分子的形成乙烯分子模型任何键之间的键
均角为:1200空间结构:平面(矩形)学与问3.乙烯分子的结构
4、烯烃同:含C=C,链状不同:分子组成相差一个 或多个CH21)、烯烃同系物的结构特点CH3CH2=CH2含有碳碳双键的烃类
乙烯是最简单的烯烃P59CH2=CH2乙烯丙烯CH3CH2CH1=CH2CH3(CH2 )4CH1=CH2丁烯庚烯思考:
还有哪类物质的通式和烯烃相同?他们是否互为同系物?是否互为同分异构体?
2)、通式CnH2n (n≥2整数)环烷烃不是同系物但是同分异构体*不饱和烃:分子里含有碳碳双键或碳碳三键,碳原子所结合的氢原子数少于饱和链烃里的氢原子数,这样的烃叫做不饱和烃。CH2=CH2CH3CH=CH2CH2=CH-CH=CH2乙烯丙烯1,3-丁二烯乙炔丙炔5、乙烯的性质1)、物理性质无色稍有气味的气体密度比空气小(1.25g/L)难溶于水2)、化学性质(比较活泼)(1)氧化反应 ①燃烧 现象: 发出明亮的蓝色火焰,冒黑烟,产生水雾和能使澄清的石灰水变浑浊的气体 ②使紫色的KMnO4(H+)溶液褪色(易被氧化思考:
可否用KMnO4(H+)溶液除掉C2H6中的C2H4?可以,同时这个方法可以鉴别C2H6和C2H4(2)加成反应 ① CH2=CH2使橙黄色的Br2水褪色1,2-二溴乙烷(无色液体)(溴水)加成反应: 有机物分子中双键(或三键)两端的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。P60 (乙烯水化法制乙醇) ②乙烯与水加成制乙醇思考:
工业上如何制取氯乙烷? 可否利用乙烷与Cl2反应?(氯乙烷)CH3-CH3 CH3-CH2Cl③乙烯与H-H和H-Cl的加成不可以因为产物太多比较:取代与加成的区别替换直接结合二种一种饱和不饱和(3)聚合反应聚乙烯(塑料,性质稳定) 聚合反应: 小分子结合成高分子的反应 不饱和化合物通过不饱和键断裂再加成而聚合的反应练习:
书写CH2=CHCl加聚的化学方程式。 加聚反应:?这种气体是: 如果把青桔子和熟苹果放在同一个塑料袋里,系紧袋口,这样一段时间后青桔子就可以变黄、成熟。 乙 烯实践活动:乙烯的用途植物生长调节剂练习
1.工业上的乙烯主要来源于 ,它是一种无 色、 味的气体, 溶于水。2.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )。
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气瓶3.下列物质不可能是乙烯加成产物的是( )。
A.CH3CH3 ??B.CH3CHCl2 ?C.CH3CH2OH
?D.CH3CH2Br石油稍有气味难溶于水BB来自石油的两种基本化工原料
第二课时
教学目标
1.了解苯的组成和结构特征,掌握苯的主要性质;
2.进一步强化学生对“结构─性质”关系的认识;
3.培养学生的逻辑思维能力。
苯有人说我笨,其实并不笨,
脱去竹笠换草帽,化工生产逞英雄。来自石油的两种基本化工原料19世纪欧洲许多国家都使用煤气照明,煤气通常是压缩在桶里贮运的,人们发现这种桶里总有一种油状液体,但长时间无人问津。1825年英国科学家法拉第对这种液体产生了浓厚兴趣,他花了整整五年时间提取这种液体,从中得到了苯—一种无色油状液体。日拉尔等化学家测定该烃的分子式为C6H6,这种烃就是苯。但苯分子结构是十九世纪化学一大谜。二、苯例题1:发现苯后,经过法国化学家日拉尔等人的精确测定,发现这种液体的相对分子质量为78,而含碳量却高达92.3%,请计算该物质的分子式。 解析:78X92.3%÷12=6
78X(1—92.3%)÷1=6
所以苯的分子式为C6H6。
一、苯的分子结构1、苯的分子式猜想与假设:
(1)苯的分子式为C6H6,试根据苯的分子式写出原子可能的连接方式。
(2)若苯分子为上述结构之一,则其应具有什么重要化学性质?可设计怎样的实验来证明?
(1)苯(链状)可能的结构有:
CH≡C-CH2-CH2-C≡CH
CH≡C-CH=CH-CH=CH2
CH2=C=CH-CH=C=CH2(2)可设计如下实验证明:
① 能否使溴的四氯化碳溶液褪色(发生加成反应);
② 能否使酸性高锰酸钾溶液褪色。
实验3-1:
1.往试管中加入少量苯,再加入溴的四氯化碳溶液,振荡后,观察现象。
2.往试管中加入少量苯,再加入酸性高锰酸钾溶液,振荡后,观察现象。 结论:苯不能使酸性KMnO4溶液、溴水之褪色?2.苯的结构分子式为C6H6极不饱和苯不与溴的四氯化碳溶液和酸性高锰酸钾溶液反应,说明苯分子中没有与乙烯类似的双键,进一步的研究表明,苯分子6个碳原子之间形成的是一种介于单键和双键之间的独特的键。其结构式为:
凯库勒式苯分子模型结构特点: (1)苯分子是平面六边形的稳定结构;
(2)苯分子中碳碳之间的键是介于碳碳单键与碳碳双键之间的一种独特的键;
(3)苯分子中六个碳原子等效,六个氢原子等效。
1.苯是没有颜色带有特殊气味的液体
2.密度比水小,不溶于水。
3.苯的沸点是80.1℃,熔点是5.5℃。如果有冰来冷却, 苯 可以凝结成无色的晶体。
4.苯是一种良好的有机溶剂,Br2、I2易溶于苯二、苯的物理性质:三.苯的化学性质⒈氧化反应现象:明亮的火焰、浓烟(含碳量等于乙炔)⒉取代反应①卤代(氯苯)(溴苯)C6H6 + Br2 C6H6 + Cl2 + HBr+ HCl⒈铁粉的作用是什么?
⒉长导管的作用是什么?
⒊为什么锥形瓶中导管末端不插入液面以下?
⒋什么现象说明发生了取代反应?
⒌实验后得到的褐色液体是什么?如何才能得到无色的溴苯?催化剂冷凝回流、导气锥形瓶中产生白雾及淡黄色沉淀溶有Br2的溴苯、用NaOH溶液洗HBr极易溶于水,会发生倒吸现象-Br+ HBr吸收溴化氢中的溴和溴苯②硝化 (苯分子中的H原子被硝基取代的反应)+ H2O(硝基苯)淡黄色油状液体,密度比水大实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
③在50~60℃下发生反应,直至反应结束;
④除去混合酸后,粗产品依次用蒸馏水和5% NaOH溶液洗涤,最后再用蒸馏水洗涤;
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯。实验室制备硝基苯的主要步骤请填写下列空白:
(1)配制一定比例浓H2SO4和浓HNO3混合酸时,操作的注意事项是:________。
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是______。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是_ __。
(4)步骤④中粗产品用5% NaOH溶液洗涤的目的是__ __。
水浴加热往浓HNO3中加入浓H2SO4分液漏斗除去多余的浓H2SO4和浓HNO3③磺化 (苯分子中的H原子被磺酸基取代的反应)+ HO-SO3H-SO3H⒊加成反应小结:易取代、
难加成、难氧化+ 3H2+ H2O (苯磺酸)四、说明苯的重要用途。 练习:
1.苯是一种 色、 气味的 体, 溶于水,其分子式为 ,结构式为 。
2.下列反应中,属于加成反应的是( )。
A.乙烯使酸性KMnO4溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使溴水褪色
D.甲烷与氯气混合,光照一段时间后黄绿色消失把下列反应方程式写完整作业6)C6H6 + Br2 7)8)+ H2比较乙烷和乙烯C2H6C2H4CH3CH3CH2=CH2C-CC=C109°28′120 °不在同一平面上在同一平面上1、????? *烯烃的命名 步骤: 选主链:含C=C的最长C链 编碳号:使C=C的编号最小定名称:
取代基位置 - 取代基个数 - 取代基名称-双键位置-主链名称 *烯烃的同分异构体 注: 同分异构体可在不同类别物质之间存在;同系物只在同一类别物质之间存在。同分异构体的类型: 碳链异构 位置异构 异类异构思路:先定碳链,再移动双键 (注意对称轴),最后考虑异类练习: 找出下列各物质的同分异构体 C3H6 C4H8 C5H10再见
林喜信
2006年5月第三章 有机化合物第一课时 教学目标 1.烯烃的概念; 2.乙烯的分子结构及性质、用途; 3.强化学生对“结构─性质”关系的认识,培养学生的比较思维能力。思考与交流1.乙烯的用途一、乙烯水果催熟剂乙烯的产量是衡量一个国家的石油化工水平2.乙烯的供求状况总投资193亿元年产乙烯600万吨科学探究---用石蜡油制备乙烯实验步骤在试管①中加入石蜡油和氧化铝或碎瓷片;试管②放在冷水中;试管③中加入KMnO4溶液或溴水。实验装置如右图所示装置;实验要点:(1)石棉要尽量多吸收石蜡油。(2)石蜡油分解反应的温度要在500 ℃以上。(3)实验中要注意防止倒吸;(4)KMnO4用稀溶液,3 mL该溶液中一般加入
2~3滴稀H2SO4溶液,增加KMnO4溶液的氧化性。(5)配制溴的四氯化碳溶液时,20 mL
四氯化碳加1~2滴溴即可。用石蜡油制备乙烯探究实验:石蜡油分解实验
(1)加热分解石蜡油,观察现象;
(2)将产生的气体分别通入溴的四氯化碳溶液、高锰酸钾溶液,观察现象;
(3)用排水集气法收集一试管气体,点燃,观察燃烧的情况。 现象1)加热石蜡油分解产生无色气体3)气体通入溴的四氯化碳溶液溶液红棕色褪去2)、气体通酸性高锰酸钾溶液溶液紫色褪去4)将收集到的气体产物点燃火焰明亮并伴有黑烟思考 产生的气体是烷烃吗?为什么溴的四氯化碳溶液、高锰酸钾溶液会褪色?这种物质与烷烃的结构有什么差异性? 产生的气体不完全为烷烃,有与烷烃性质不同的烃,因为烷烃不能使溴的四氯化碳溶液、高锰酸钾溶液会褪色。石蜡油分解产物主要是烷烃和乙烯CCH H H H ....::.:.乙烯的分子的形成乙烯分子模型任何键之间的键
均角为:1200空间结构:平面(矩形)学与问3.乙烯分子的结构
4、烯烃同:含C=C,链状不同:分子组成相差一个 或多个CH21)、烯烃同系物的结构特点CH3CH2=CH2含有碳碳双键的烃类
乙烯是最简单的烯烃P59CH2=CH2乙烯丙烯CH3CH2CH1=CH2CH3(CH2 )4CH1=CH2丁烯庚烯思考:
还有哪类物质的通式和烯烃相同?他们是否互为同系物?是否互为同分异构体?
2)、通式CnH2n (n≥2整数)环烷烃不是同系物但是同分异构体*不饱和烃:分子里含有碳碳双键或碳碳三键,碳原子所结合的氢原子数少于饱和链烃里的氢原子数,这样的烃叫做不饱和烃。CH2=CH2CH3CH=CH2CH2=CH-CH=CH2乙烯丙烯1,3-丁二烯乙炔丙炔5、乙烯的性质1)、物理性质无色稍有气味的气体密度比空气小(1.25g/L)难溶于水2)、化学性质(比较活泼)(1)氧化反应 ①燃烧 现象: 发出明亮的蓝色火焰,冒黑烟,产生水雾和能使澄清的石灰水变浑浊的气体 ②使紫色的KMnO4(H+)溶液褪色(易被氧化思考:
可否用KMnO4(H+)溶液除掉C2H6中的C2H4?可以,同时这个方法可以鉴别C2H6和C2H4(2)加成反应 ① CH2=CH2使橙黄色的Br2水褪色1,2-二溴乙烷(无色液体)(溴水)加成反应: 有机物分子中双键(或三键)两端的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。P60 (乙烯水化法制乙醇) ②乙烯与水加成制乙醇思考:
工业上如何制取氯乙烷? 可否利用乙烷与Cl2反应?(氯乙烷)CH3-CH3 CH3-CH2Cl③乙烯与H-H和H-Cl的加成不可以因为产物太多比较:取代与加成的区别替换直接结合二种一种饱和不饱和(3)聚合反应聚乙烯(塑料,性质稳定) 聚合反应: 小分子结合成高分子的反应 不饱和化合物通过不饱和键断裂再加成而聚合的反应练习:
书写CH2=CHCl加聚的化学方程式。 加聚反应:?这种气体是: 如果把青桔子和熟苹果放在同一个塑料袋里,系紧袋口,这样一段时间后青桔子就可以变黄、成熟。 乙 烯实践活动:乙烯的用途植物生长调节剂练习
1.工业上的乙烯主要来源于 ,它是一种无 色、 味的气体, 溶于水。2.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )。
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气瓶3.下列物质不可能是乙烯加成产物的是( )。
A.CH3CH3 ??B.CH3CHCl2 ?C.CH3CH2OH
?D.CH3CH2Br石油稍有气味难溶于水BB来自石油的两种基本化工原料
第二课时
教学目标
1.了解苯的组成和结构特征,掌握苯的主要性质;
2.进一步强化学生对“结构─性质”关系的认识;
3.培养学生的逻辑思维能力。
苯有人说我笨,其实并不笨,
脱去竹笠换草帽,化工生产逞英雄。来自石油的两种基本化工原料19世纪欧洲许多国家都使用煤气照明,煤气通常是压缩在桶里贮运的,人们发现这种桶里总有一种油状液体,但长时间无人问津。1825年英国科学家法拉第对这种液体产生了浓厚兴趣,他花了整整五年时间提取这种液体,从中得到了苯—一种无色油状液体。日拉尔等化学家测定该烃的分子式为C6H6,这种烃就是苯。但苯分子结构是十九世纪化学一大谜。二、苯例题1:发现苯后,经过法国化学家日拉尔等人的精确测定,发现这种液体的相对分子质量为78,而含碳量却高达92.3%,请计算该物质的分子式。 解析:78X92.3%÷12=6
78X(1—92.3%)÷1=6
所以苯的分子式为C6H6。
一、苯的分子结构1、苯的分子式猜想与假设:
(1)苯的分子式为C6H6,试根据苯的分子式写出原子可能的连接方式。
(2)若苯分子为上述结构之一,则其应具有什么重要化学性质?可设计怎样的实验来证明?
(1)苯(链状)可能的结构有:
CH≡C-CH2-CH2-C≡CH
CH≡C-CH=CH-CH=CH2
CH2=C=CH-CH=C=CH2(2)可设计如下实验证明:
① 能否使溴的四氯化碳溶液褪色(发生加成反应);
② 能否使酸性高锰酸钾溶液褪色。
实验3-1:
1.往试管中加入少量苯,再加入溴的四氯化碳溶液,振荡后,观察现象。
2.往试管中加入少量苯,再加入酸性高锰酸钾溶液,振荡后,观察现象。 结论:苯不能使酸性KMnO4溶液、溴水之褪色?2.苯的结构分子式为C6H6极不饱和苯不与溴的四氯化碳溶液和酸性高锰酸钾溶液反应,说明苯分子中没有与乙烯类似的双键,进一步的研究表明,苯分子6个碳原子之间形成的是一种介于单键和双键之间的独特的键。其结构式为:
凯库勒式苯分子模型结构特点: (1)苯分子是平面六边形的稳定结构;
(2)苯分子中碳碳之间的键是介于碳碳单键与碳碳双键之间的一种独特的键;
(3)苯分子中六个碳原子等效,六个氢原子等效。
1.苯是没有颜色带有特殊气味的液体
2.密度比水小,不溶于水。
3.苯的沸点是80.1℃,熔点是5.5℃。如果有冰来冷却, 苯 可以凝结成无色的晶体。
4.苯是一种良好的有机溶剂,Br2、I2易溶于苯二、苯的物理性质:三.苯的化学性质⒈氧化反应现象:明亮的火焰、浓烟(含碳量等于乙炔)⒉取代反应①卤代(氯苯)(溴苯)C6H6 + Br2 C6H6 + Cl2 + HBr+ HCl⒈铁粉的作用是什么?
⒉长导管的作用是什么?
⒊为什么锥形瓶中导管末端不插入液面以下?
⒋什么现象说明发生了取代反应?
⒌实验后得到的褐色液体是什么?如何才能得到无色的溴苯?催化剂冷凝回流、导气锥形瓶中产生白雾及淡黄色沉淀溶有Br2的溴苯、用NaOH溶液洗HBr极易溶于水,会发生倒吸现象-Br+ HBr吸收溴化氢中的溴和溴苯②硝化 (苯分子中的H原子被硝基取代的反应)+ H2O(硝基苯)淡黄色油状液体,密度比水大实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
③在50~60℃下发生反应,直至反应结束;
④除去混合酸后,粗产品依次用蒸馏水和5% NaOH溶液洗涤,最后再用蒸馏水洗涤;
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯。实验室制备硝基苯的主要步骤请填写下列空白:
(1)配制一定比例浓H2SO4和浓HNO3混合酸时,操作的注意事项是:________。
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是______。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是_ __。
(4)步骤④中粗产品用5% NaOH溶液洗涤的目的是__ __。
水浴加热往浓HNO3中加入浓H2SO4分液漏斗除去多余的浓H2SO4和浓HNO3③磺化 (苯分子中的H原子被磺酸基取代的反应)+ HO-SO3H-SO3H⒊加成反应小结:易取代、
难加成、难氧化+ 3H2+ H2O (苯磺酸)四、说明苯的重要用途。 练习:
1.苯是一种 色、 气味的 体, 溶于水,其分子式为 ,结构式为 。
2.下列反应中,属于加成反应的是( )。
A.乙烯使酸性KMnO4溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使溴水褪色
D.甲烷与氯气混合,光照一段时间后黄绿色消失把下列反应方程式写完整作业6)C6H6 + Br2 7)8)+ H2比较乙烷和乙烯C2H6C2H4CH3CH3CH2=CH2C-CC=C109°28′120 °不在同一平面上在同一平面上1、????? *烯烃的命名 步骤: 选主链:含C=C的最长C链 编碳号:使C=C的编号最小定名称:
取代基位置 - 取代基个数 - 取代基名称-双键位置-主链名称 *烯烃的同分异构体 注: 同分异构体可在不同类别物质之间存在;同系物只在同一类别物质之间存在。同分异构体的类型: 碳链异构 位置异构 异类异构思路:先定碳链,再移动双键 (注意对称轴),最后考虑异类练习: 找出下列各物质的同分异构体 C3H6 C4H8 C5H10再见
