质量守恒定律[下学期]
图片预览







文档简介
课件25张PPT。欢迎各位老师光临指导第四章 化学方程式复习课知识链接质量守恒定律是化学方程式的理论准备,这是本章的基础。化学方程式是本章的中心。根据化学方程式的计算是化学方程式的具体应用。中考导航:1.理解质量守恒定律和化学方程式的涵义
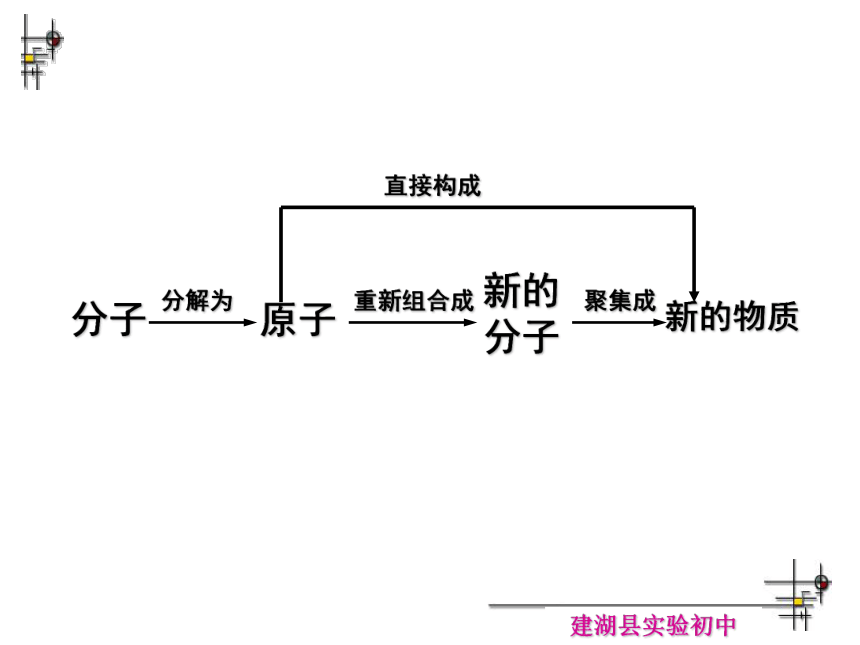
2.能正确书写并配平简单的化学方程式参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律就叫质量守恒定律。一、质量守恒定律1.内容:2.原因:在一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。一、质量守恒定律分子分解为原子重新组合成新的分子聚集成新的物质直接构成1 、物质发生化学反应前后,不发生变化的是( ):
①物质的质量总和;②物质的质量;③物质的种类;④元素的种类;⑤原子的数目;⑥原子的种类;⑦物质的分子总数。2、判断下列说法是否正确:
(1)100克干冰升华变成100克二氧化碳气体符合质量守恒定律
(2)燃烧的镁带和生成的白色粉末质量相等。
(3)3gC在10gO2中充分燃烧,生成13gC02。
(4)水在催化剂的作用下可变成燃油(主要含C、H)1、西班牙的瑞奥汀托河是一条酸河。经调查发现是由于上游河床含有的某种物质R,在水中氧的作用下发生下列反应所致:
2R+2H2O+7O2=2FeSO4+2H2SO4
则R的化学式是( )
A、FeS B、Fe2S3 C、FeO D、FeS2D2、某反应A+B=C+D,若有30克A和15克B恰好完全反应生成10克C,那么要得到7克D,参加反应A的质量是 ( )
A、6克 B、12克 C、15克 D、20克3、将A、B、C三物质各5克混合加热进行化合反应,其中B为催化剂。当A完全反应后,生成D的质量为8克,则反应后混合物中B与C的质量比为 ( )
A、4:1 B、5:1 C、5:3 D、5:2AD3.实验探究:一、质量守恒定律化 学 方 程 式概念:涵义书写原则书写步骤应用用化学式来表示化学反应的式子表示反应物,生成物和反应条件表示反应物,生成物之间的质量比以客观事实为基础遵守质量守恒定律1、写2、配3、等二、化学方程式3.配平下列化学方程式:比较,归纳,概括出一些规律,并根据这些规律解决实际问题是化学学习中必须掌握的科学方法。某学生在配平下列化学方程式时,发现其中存在某种规律。
(1)□FeO+□CO—□Fe+□CO2
(2)□Fe2O3+□CO—□Fe +□CO2
(3)□Fe3O4+□CO—□Fe +□CO2
请你概括出这类反应的配平规律是__________.
并运用这规律配平下列化学方程式:
□FexOy+□CO—□ Fe + □CO24.按要求完成下列反应的化学方程式。
(1)白磷自燃
(2)气体打火机中充入的燃料是丁烷(C4H10), 它充分燃烧生成水和二氧化碳
(3)用含氢氧化铝的药片治疗胃酸过多
(4)用稀硫酸除铁锈
(5)目前,我国运送飞船的火箭所用的燃料是 偏二甲肼(C2H8N2),火箭发射时该燃料与四氧化二氮剧烈反应,生成二氧化碳、水和一种常见的气体单质。 根据刚才的练习请同学们思考:在书写方程式时应该注意哪几个问题?思考题1.判断下列化学方程式书写正误(2) Fe + 6HClFeCl3 + 3H2↑2.航天飞机曾用金属铝粉和高氯酸铵(NH4ClO4)的混合物作固体燃料,加热铝粉使其被氧气氧化,放出大量的热,促使混合物中高氯酸铵受热分解,同时生成四种气体:两种是空气中的主要成分,一种气体是氯气(Cl2),还有一种气体是水蒸气,因而产生巨大的推动力,试写出其中涉及的化学反应方程式:
①铝粉被氧气氧化成三氧化二铝_____________________________________;??
②高氯酸铵受热分解_____________________________________.效果检测谢谢各位,再见试一试说出下面化学方程式表示的意义:?迁移练习科学家正研究在太空建一座把太阳光变成激光的装置,然后用激光照射添加了催化剂二氧化钛的水,水就能有效分解产生氢气和氧气,即某同学看到化学方程式,即想到了以下两点:
(1)水在激光和催化剂TiO2的作用下,能分解产生氢气和氧气;
(2)每36克水可以分解生成4克氢气和32克氧气你还能想到更多的信息吗?
2.能正确书写并配平简单的化学方程式参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律就叫质量守恒定律。一、质量守恒定律1.内容:2.原因:在一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。一、质量守恒定律分子分解为原子重新组合成新的分子聚集成新的物质直接构成1 、物质发生化学反应前后,不发生变化的是( ):
①物质的质量总和;②物质的质量;③物质的种类;④元素的种类;⑤原子的数目;⑥原子的种类;⑦物质的分子总数。2、判断下列说法是否正确:
(1)100克干冰升华变成100克二氧化碳气体符合质量守恒定律
(2)燃烧的镁带和生成的白色粉末质量相等。
(3)3gC在10gO2中充分燃烧,生成13gC02。
(4)水在催化剂的作用下可变成燃油(主要含C、H)1、西班牙的瑞奥汀托河是一条酸河。经调查发现是由于上游河床含有的某种物质R,在水中氧的作用下发生下列反应所致:
2R+2H2O+7O2=2FeSO4+2H2SO4
则R的化学式是( )
A、FeS B、Fe2S3 C、FeO D、FeS2D2、某反应A+B=C+D,若有30克A和15克B恰好完全反应生成10克C,那么要得到7克D,参加反应A的质量是 ( )
A、6克 B、12克 C、15克 D、20克3、将A、B、C三物质各5克混合加热进行化合反应,其中B为催化剂。当A完全反应后,生成D的质量为8克,则反应后混合物中B与C的质量比为 ( )
A、4:1 B、5:1 C、5:3 D、5:2AD3.实验探究:一、质量守恒定律化 学 方 程 式概念:涵义书写原则书写步骤应用用化学式来表示化学反应的式子表示反应物,生成物和反应条件表示反应物,生成物之间的质量比以客观事实为基础遵守质量守恒定律1、写2、配3、等二、化学方程式3.配平下列化学方程式:比较,归纳,概括出一些规律,并根据这些规律解决实际问题是化学学习中必须掌握的科学方法。某学生在配平下列化学方程式时,发现其中存在某种规律。
(1)□FeO+□CO—□Fe+□CO2
(2)□Fe2O3+□CO—□Fe +□CO2
(3)□Fe3O4+□CO—□Fe +□CO2
请你概括出这类反应的配平规律是__________.
并运用这规律配平下列化学方程式:
□FexOy+□CO—□ Fe + □CO24.按要求完成下列反应的化学方程式。
(1)白磷自燃
(2)气体打火机中充入的燃料是丁烷(C4H10), 它充分燃烧生成水和二氧化碳
(3)用含氢氧化铝的药片治疗胃酸过多
(4)用稀硫酸除铁锈
(5)目前,我国运送飞船的火箭所用的燃料是 偏二甲肼(C2H8N2),火箭发射时该燃料与四氧化二氮剧烈反应,生成二氧化碳、水和一种常见的气体单质。 根据刚才的练习请同学们思考:在书写方程式时应该注意哪几个问题?思考题1.判断下列化学方程式书写正误(2) Fe + 6HClFeCl3 + 3H2↑2.航天飞机曾用金属铝粉和高氯酸铵(NH4ClO4)的混合物作固体燃料,加热铝粉使其被氧气氧化,放出大量的热,促使混合物中高氯酸铵受热分解,同时生成四种气体:两种是空气中的主要成分,一种气体是氯气(Cl2),还有一种气体是水蒸气,因而产生巨大的推动力,试写出其中涉及的化学反应方程式:
①铝粉被氧气氧化成三氧化二铝_____________________________________;??
②高氯酸铵受热分解_____________________________________.效果检测谢谢各位,再见试一试说出下面化学方程式表示的意义:?迁移练习科学家正研究在太空建一座把太阳光变成激光的装置,然后用激光照射添加了催化剂二氧化钛的水,水就能有效分解产生氢气和氧气,即某同学看到化学方程式,即想到了以下两点:
(1)水在激光和催化剂TiO2的作用下,能分解产生氢气和氧气;
(2)每36克水可以分解生成4克氢气和32克氧气你还能想到更多的信息吗?
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
