选修3 原子结构(4)-新课标[下学期]
文档属性
| 名称 | 选修3 原子结构(4)-新课标[下学期] |
|
|
| 格式 | rar | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-04-02 00:00:00 | ||
图片预览



文档简介
课件23张PPT。广东肇庆中学 曾凯芳原子结构原子结构与元素周期表温故知新原子实
原子中,原子核及除价电子以外的内层电子组成原子实。例如,钠Na的该外电子排布为:1s22s22p63s1,其中第1、2电子层与原子核组成原子实,此原子实与氖Ne(1s22s22p6)的结构相同,钠的核外电子排布也可写作[Ne]3s1。钾K的电子排布为:1s22s22p63s23p64s1,也可写作[Ar]4s1。铜Cu为:1s22s22p63s23p63d104s1,也可写作[Ar]3d104s1。问题:写出下列元素的电子排布式:
Na
K
Rb
Cs 1s22s2p63s1
1s22s2p63s23p64s1
1s22s2p63s23p63d104s24p65s1
1s22s2p63s23p63d104s24p64d105s25p66s1 或 [Xe]6s1周
期
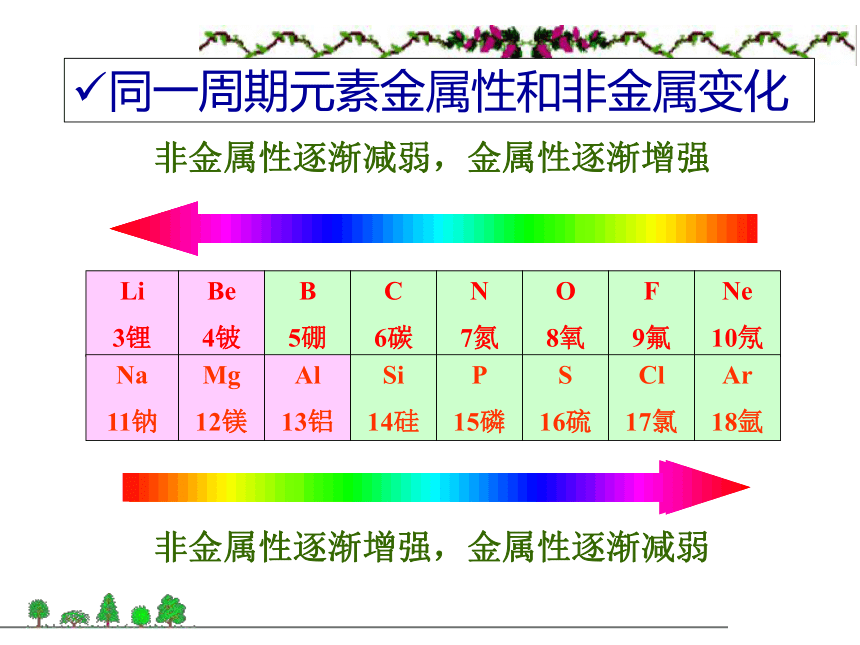
表7个周期(三短、三长、一不完全)7个副族:仅由长周期构成的族
(ⅠB~ⅦB)Ⅷ族(3个纵行):Fe、Co、Ni等
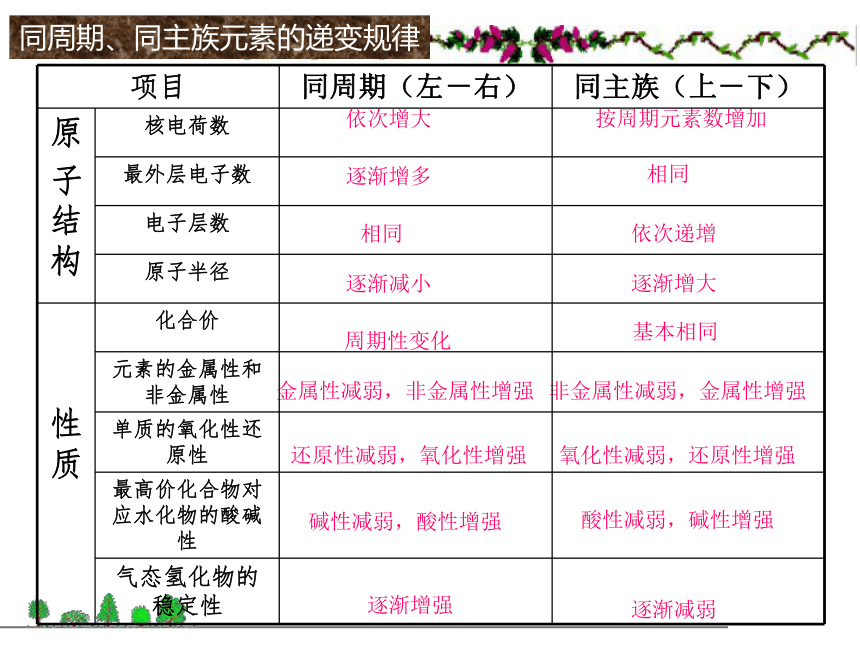
9种元素零族:稀有气体元素元素周期律复习同一周期元素金属性和非金属变化非金属性逐渐增强,金属性逐渐减弱非金属性逐渐减弱,金属性逐渐增强同一主族元素 金属性和非金属变化预测:从上到下,失电子能力逐渐增强,得电子能力逐渐减弱。∴元素金属性逐渐增强,非金属性逐渐减弱。
以碱金属和卤族元素为例:
碱金属:从上到下,金属性逐渐增强
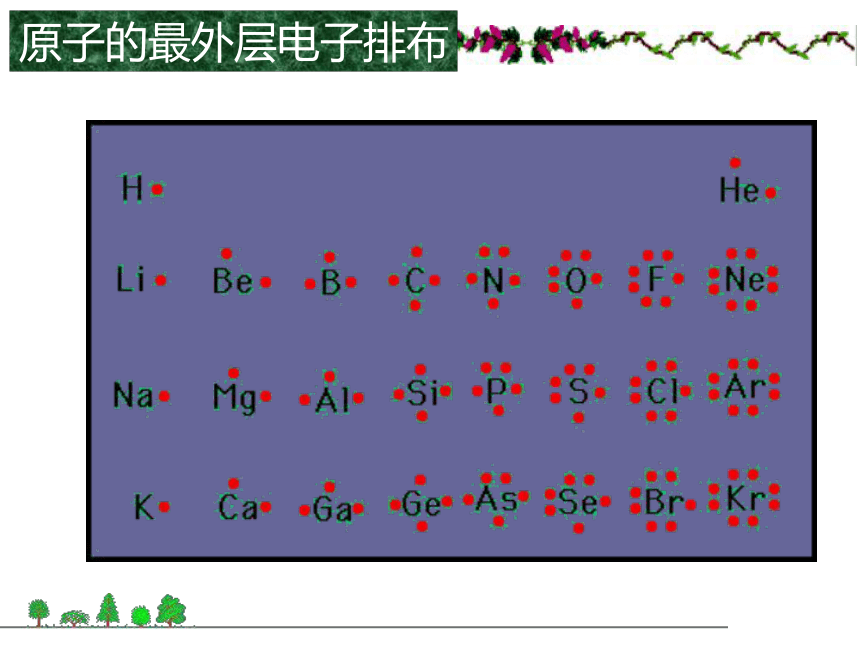
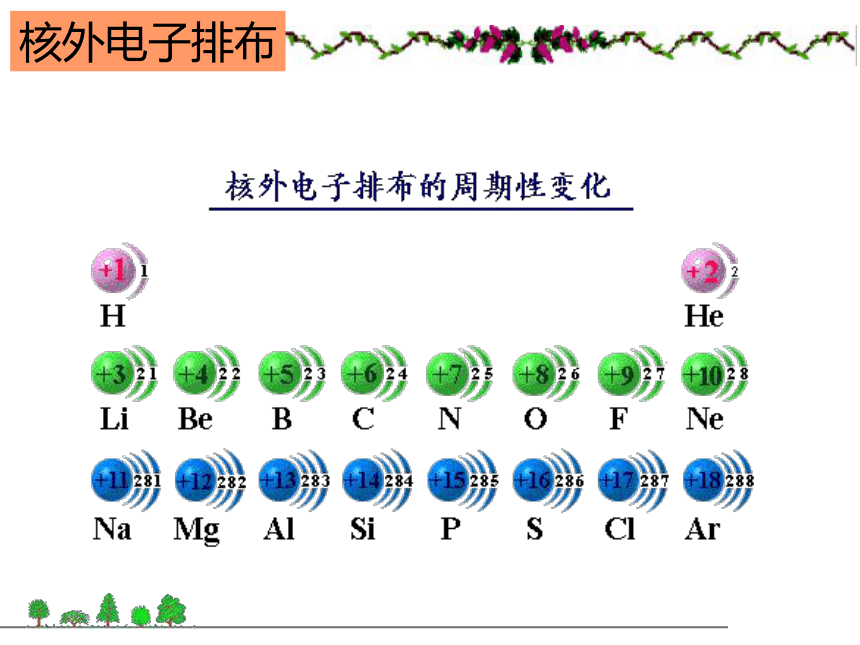
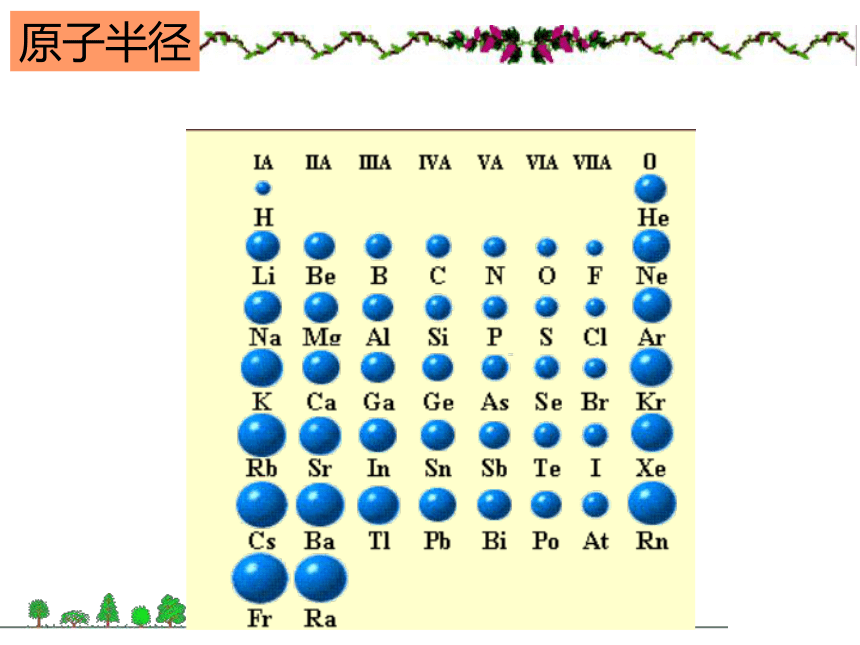
卤素:从上到下,非金属性逐渐减弱,金属性逐渐增强。同周期、同主族元素的递变规律依次增大逐渐增多相同逐渐减小周期性变化金属性减弱,非金属性增强还原性减弱,氧化性增强碱性减弱,酸性增强逐渐增强按周期元素数增加相同依次递增逐渐增大基本相同非金属性减弱,金属性增强氧化性减弱,还原性增强酸性减弱,碱性增强逐渐减弱原子的最外层电子排布核外电子排布原子半径原子半径元素化合价元素主要化合价的周期性变化原子结构元素性质元素在表中位置位、构、性三者关系这个人你认识吗?棱台型元素周期表各种元素周期表各种元素周期表扇形元素周期表各种元素周期表螺旋型周期表科学探索1、写出元素周期表中每个周期开头的第一个元素和结尾的元素的电子排布式的通式
2、什么是外围电子,价电子,价电子层
3、你从下列的元素分区图中悟出了元素分区的道理了吗?
P24 5、6、7题
(以上三项均写在作业本上)作 业
老曾学做课件之
肇中版
2005-31
再 见
原子中,原子核及除价电子以外的内层电子组成原子实。例如,钠Na的该外电子排布为:1s22s22p63s1,其中第1、2电子层与原子核组成原子实,此原子实与氖Ne(1s22s22p6)的结构相同,钠的核外电子排布也可写作[Ne]3s1。钾K的电子排布为:1s22s22p63s23p64s1,也可写作[Ar]4s1。铜Cu为:1s22s22p63s23p63d104s1,也可写作[Ar]3d104s1。问题:写出下列元素的电子排布式:
Na
K
Rb
Cs 1s22s2p63s1
1s22s2p63s23p64s1
1s22s2p63s23p63d104s24p65s1
1s22s2p63s23p63d104s24p64d105s25p66s1 或 [Xe]6s1周
期
表7个周期(三短、三长、一不完全)7个副族:仅由长周期构成的族
(ⅠB~ⅦB)Ⅷ族(3个纵行):Fe、Co、Ni等
9种元素零族:稀有气体元素元素周期律复习同一周期元素金属性和非金属变化非金属性逐渐增强,金属性逐渐减弱非金属性逐渐减弱,金属性逐渐增强同一主族元素 金属性和非金属变化预测:从上到下,失电子能力逐渐增强,得电子能力逐渐减弱。∴元素金属性逐渐增强,非金属性逐渐减弱。
以碱金属和卤族元素为例:
碱金属:从上到下,金属性逐渐增强
卤素:从上到下,非金属性逐渐减弱,金属性逐渐增强。同周期、同主族元素的递变规律依次增大逐渐增多相同逐渐减小周期性变化金属性减弱,非金属性增强还原性减弱,氧化性增强碱性减弱,酸性增强逐渐增强按周期元素数增加相同依次递增逐渐增大基本相同非金属性减弱,金属性增强氧化性减弱,还原性增强酸性减弱,碱性增强逐渐减弱原子的最外层电子排布核外电子排布原子半径原子半径元素化合价元素主要化合价的周期性变化原子结构元素性质元素在表中位置位、构、性三者关系这个人你认识吗?棱台型元素周期表各种元素周期表各种元素周期表扇形元素周期表各种元素周期表螺旋型周期表科学探索1、写出元素周期表中每个周期开头的第一个元素和结尾的元素的电子排布式的通式
2、什么是外围电子,价电子,价电子层
3、你从下列的元素分区图中悟出了元素分区的道理了吗?
P24 5、6、7题
(以上三项均写在作业本上)作 业
老曾学做课件之
肇中版
2005-31
再 见
