选修3 原子结构(5)-新课标[下学期]
文档属性
| 名称 | 选修3 原子结构(5)-新课标[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 907.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-04-02 00:00:00 | ||
图片预览


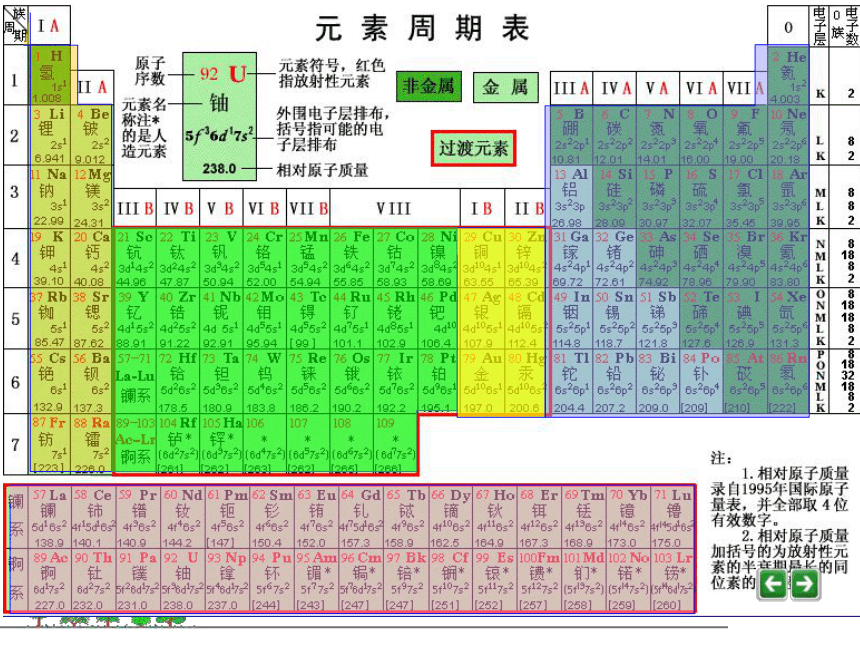

文档简介
课件8张PPT。广东肇庆中学 曾凯芳原子结构元素周期表与元素周期律(1)科学探索1、写出元素周期表中每个周期开头的第一个元素和结尾的元素的电子排布式的通式?
2、什么是外围电子,价电子,价电子层
3、你从下列的元素分区图中悟出了元素分区的道理了吗?
4、为什么副族元素又称为过渡元素?
5、为什么非金属位于元素周期表中右上角的三角区内?
6、处于非金属三角区边缘的元素常被称为半金属或准金属,为什么? IA族 0族
ns1 ns2np6
其中He元素的最外层就是第一电子层所以是1s2外围电子即价电子,一般地说,外围电子是指:
主族元素:最外层电子
副族元素:最外层S电子和次外层的d电子理解:新增加的电子填充在什么能级,这个元素就属于什么区。原子半径电离能 气态电中性原子在基态时失去最外层第一个电子成为+1价气态离子所需的能量叫做第一电离能。 电离能反映了原子失去电子倾向的大小。电离能越大,越难失去电子。 阅读课本P19第2题,回答:
为什么原子的逐级电离能越来越大?
这些数据跟钠、镁、铝的化合价有什么关系? 观察下图回答:碱金属的电离能与碱金属的活泼性存在什么关系?学与问 P24 8、9、10题
(以上三项均写在作业本上)作 业
老曾学做课件之
肇中版
2005-32
再 见
2、什么是外围电子,价电子,价电子层
3、你从下列的元素分区图中悟出了元素分区的道理了吗?
4、为什么副族元素又称为过渡元素?
5、为什么非金属位于元素周期表中右上角的三角区内?
6、处于非金属三角区边缘的元素常被称为半金属或准金属,为什么? IA族 0族
ns1 ns2np6
其中He元素的最外层就是第一电子层所以是1s2外围电子即价电子,一般地说,外围电子是指:
主族元素:最外层电子
副族元素:最外层S电子和次外层的d电子理解:新增加的电子填充在什么能级,这个元素就属于什么区。原子半径电离能 气态电中性原子在基态时失去最外层第一个电子成为+1价气态离子所需的能量叫做第一电离能。 电离能反映了原子失去电子倾向的大小。电离能越大,越难失去电子。 阅读课本P19第2题,回答:
为什么原子的逐级电离能越来越大?
这些数据跟钠、镁、铝的化合价有什么关系? 观察下图回答:碱金属的电离能与碱金属的活泼性存在什么关系?学与问 P24 8、9、10题
(以上三项均写在作业本上)作 业
老曾学做课件之
肇中版
2005-32
再 见
