选修5 第一章第2节 有机化合物的结构特点[上学期]
文档属性
| 名称 | 选修5 第一章第2节 有机化合物的结构特点[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 369.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-08-20 00:00:00 | ||
图片预览



文档简介
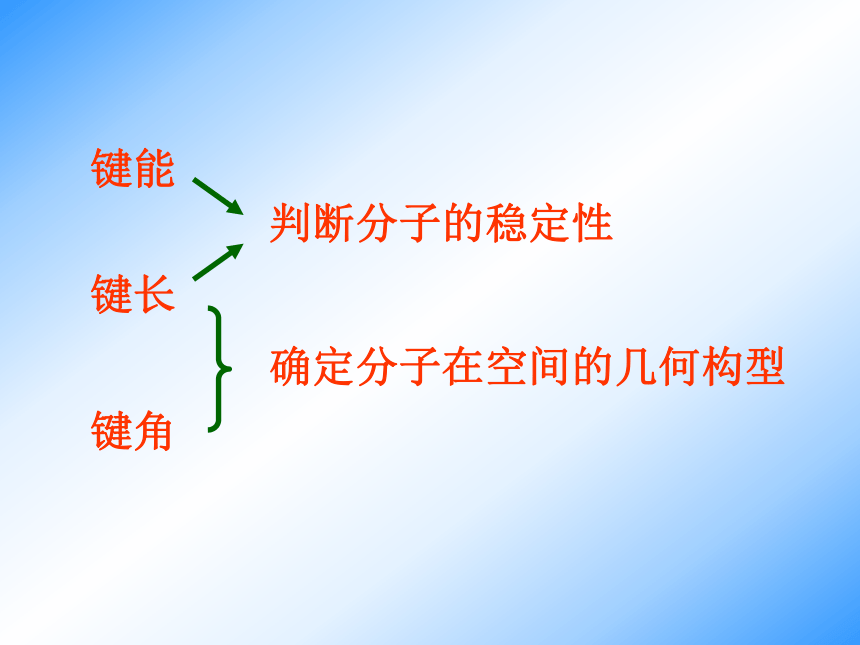
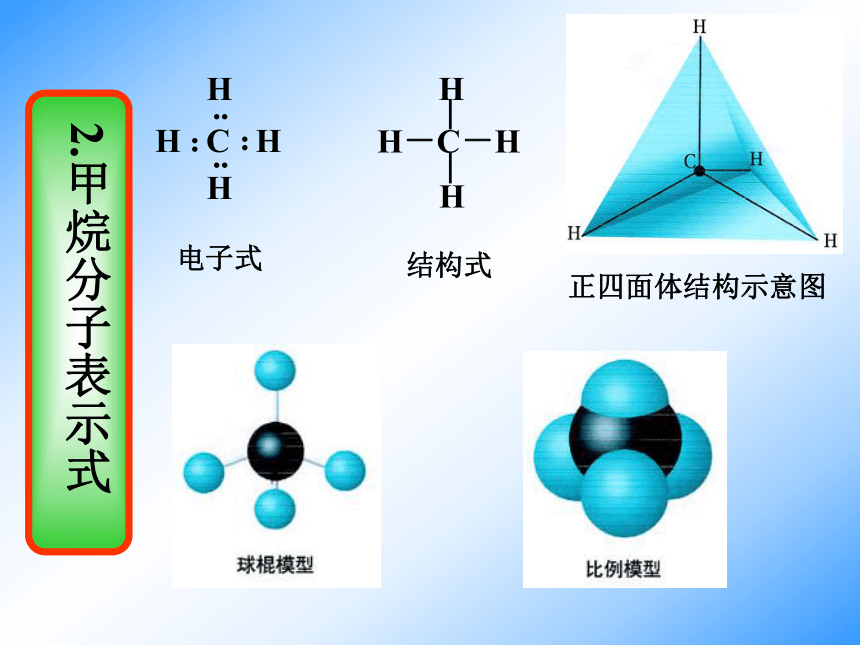
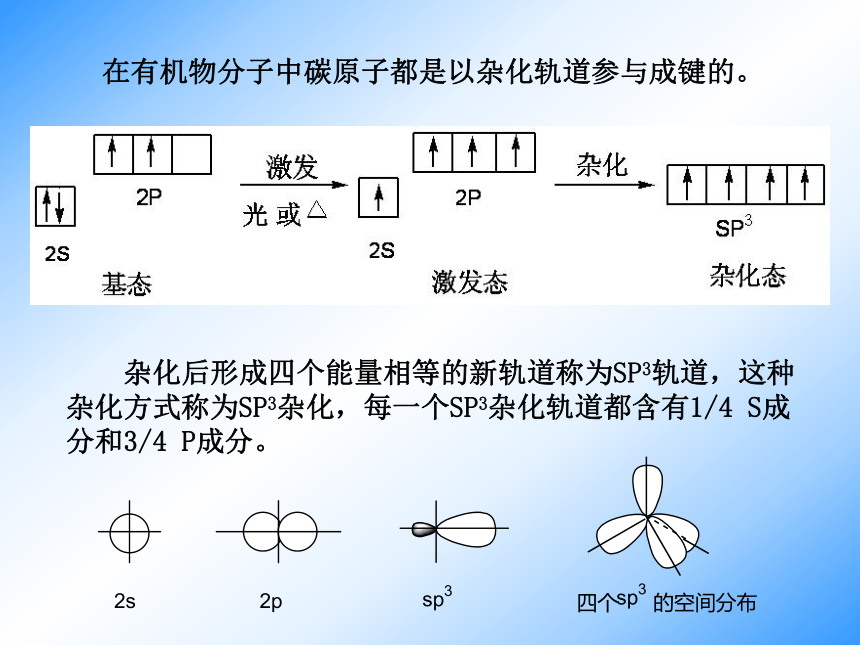
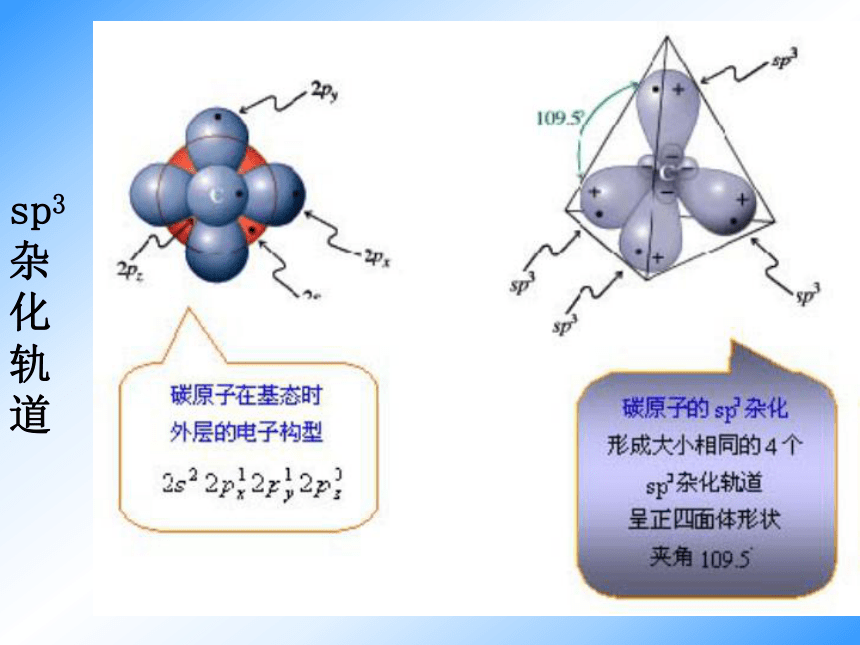
课件14张PPT。第二节 有机化合物的结构特点(第一课时)一、有机物中碳原子的成键特点在有机物分子中碳呈 价。 碳原子既可与其他原子形成 共价键,碳原子之间也可相互成键,也可以形成 或 ;碳碳之间可以形成长长的 ,也可以形成 。——形成4个共价键四碳链碳环问题:有机物种类繁多的主要原因是什么?四个答:碳原子既可与其他原子形成4个共价键,碳原子之间也可相互成键。键长分子中两个成键的原子的核间距离叫做键长一般说来,键长越短,键越牢固。键能气态原子形成一摩共价单键所释放的能量(破坏一摩单键所吸收的能量)叫做键能。键能越大,键越牢固。键角在分子中键和键之间的夹角叫做键角1.共价键的三个参数 键能 键长 键角 判断分子的稳定性 确定分子在空间的几何构型电子式结构式正四面体结构示意图 杂化后形成四个能量相等的新轨道称为SP3轨道,这种杂化方式称为SP3杂化,每一个SP3杂化轨道都含有1/4 S成分和3/4 P成分。 在有机物分子中碳原子都是以杂化轨道参与成键的。sp3杂化轨道 sp2杂化轨道 sp杂化轨道 烷烃分子中的碳都是sp3杂化。
甲烷具有正四面体的结构特征。
当烷烃中的碳原子数大于3的时候,碳链就形成锯齿形状。
烷烃中的碳氢键和碳碳键都是σ键。3.烷烃的结构特征:在化学中,将两个轨道沿着轨道对称轴方向重叠形成的键叫σ键。σ键的定义1、电子云可以达到最大程度的重叠,所以比较牢固。
2、σ键旋转时不会破坏电子云的重叠,所以σ键可以自由旋转。σ键的特点练习:1、有四种物质①金刚石;②白磷;③甲烷;④四氯化碳,其中分子具有正四面体构型的是:( )
A、①②③ B、①③④ C、②③④ D、①②③④C2、对制冷剂氟里昂—12(CF2Cl2)的叙述正确的是:( )
A、只有一种结构 B、有两种不同结构
C、有四种不同结构 D、是非极性分子A
甲烷具有正四面体的结构特征。
当烷烃中的碳原子数大于3的时候,碳链就形成锯齿形状。
烷烃中的碳氢键和碳碳键都是σ键。3.烷烃的结构特征:在化学中,将两个轨道沿着轨道对称轴方向重叠形成的键叫σ键。σ键的定义1、电子云可以达到最大程度的重叠,所以比较牢固。
2、σ键旋转时不会破坏电子云的重叠,所以σ键可以自由旋转。σ键的特点练习:1、有四种物质①金刚石;②白磷;③甲烷;④四氯化碳,其中分子具有正四面体构型的是:( )
A、①②③ B、①③④ C、②③④ D、①②③④C2、对制冷剂氟里昂—12(CF2Cl2)的叙述正确的是:( )
A、只有一种结构 B、有两种不同结构
C、有四种不同结构 D、是非极性分子A
