质量守恒定律[上学期]
图片预览







文档简介
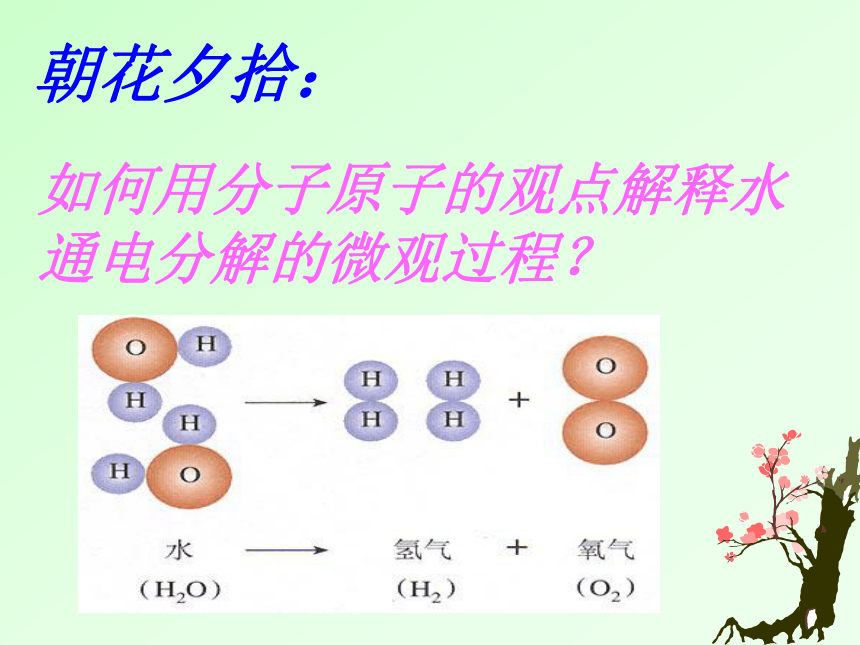
课件27张PPT。朝花夕拾:如何用分子原子的观点解释水通电分解的微观过程?想一想 物质在发生化学变化时,反应物的质量总和与生成物的质量总和之间存在什么关系呢?
1.可能是变大的
2.可能是不变的
3.可能是变小的教学目标:
1、能够完成对反应物和生成物质量的测定并总结出质量守衡定律
2、培养辨证唯物主义观点和定量研究、分析能力
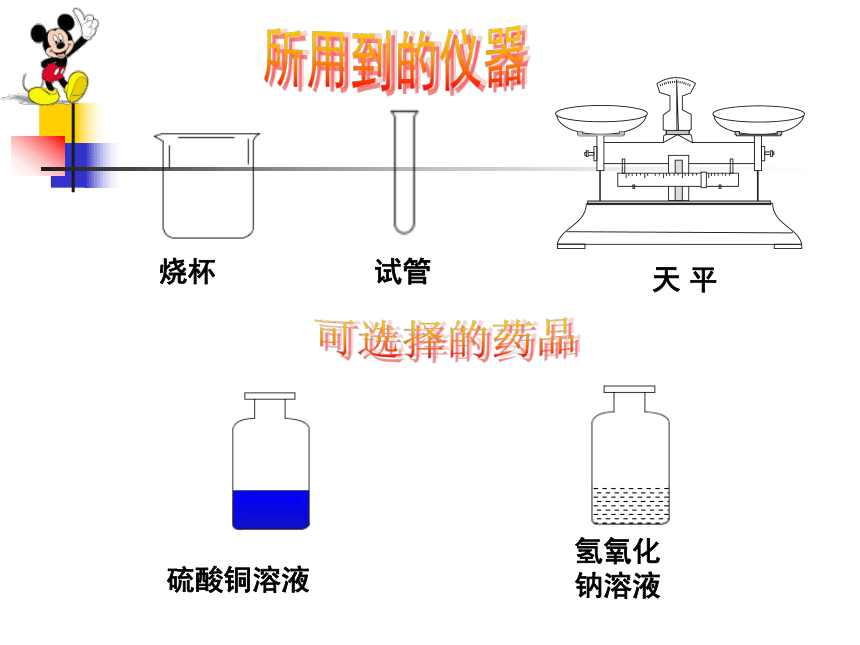
3、在探究学习中学会协作、交流(如果反应物是两种液体,应如何称量其总质量?)注意:如需倾倒液体需小心操作,不要将液体倒在外面,以免影响实验结果探究活动一:氢氧化钠和硫酸铜混和后,质量是如何变化的?硫酸铜溶液氢氧化钠溶液烧杯试管天 平可选择的药品所用到的仪器现象:生成蓝色沉淀,天平仍保持平衡氢氧化钠+硫酸铜结论:反应前物质质量总和与生成物质量总和相等反应前后的质量测定想一想:反应前后天平是否平衡?为什么?解释:P+O2 P2O5
反应物质量守恒定律 参加化学反应的各物质的质量和,等于反应后生成的各物质的质量总和。同步练习:1、 克碳在32克氧气中充分燃烧生成44克二氧化碳。2、若电解18克水,可生成2克氢气和 克氧气。12163.6手脑并用探究活动二:比一比,赛一赛:用以下的仪器和药品试验,看质量有什么变化。提示:仔细观察实验现象。思考出现这种现象的原因。稀硫酸烧杯试管天 平可选择的药品所用到的仪器锌粒现象:锌的表面有气泡冒出,天平无法保持平衡锌+硫酸结论:反应前物质质量总和与生成物质量不相等?反应前后的质量测定想一想:为什么??参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。质量守恒定律2、“参加”意味着反应物中过量的剩余部分的质量不应算在内。如锌粒与稀硫酸的反应剩余的锌粒不算在内。1、“总和”意味着把各种状态的反应物和生成物都算在内。如肉眼看不见的气体也应考虑。3、初中化学中质量守恒定律仅适用于化学变化。1、氯酸钾受热分解后,剩余固体的质量比原反应物的质量轻。氯酸钾受热分解生成氯化钾和氧气。由质量守恒定律知,反应物氯酸钾的质量等于生成物氯化钾和氧气的质量,氧气散失到空气中,所以,剩余固体的质量必然比原反应物的质量轻练一练:化学反应的实质是什么?化学反应的实质是:
参加反应的各物质的分子分化成原子,原子再重新组合而生成其他物质的分子。 二、质量守恒的原因:
在化学反应中,反应前后
没改变, 没有改变,
也没有变化。所以,化学反应前后各物质的
必然相等。
原子的种类原子的数目原子的质量质量总和 原子的种类不变,所以元素的种类也不变。推测一些物质的组成进行有关计算如果将燃着的镁条上方罩上罩,使生成物全部收集起称量,会出现什么样的实验结果?想一想元素种类变了吗?元素质量变了吗?物质的总质量呢?化学反应前后物质种类呢?分子种类呢?动动脑不变改变巩固练习:1、根据质量守恒定律知,铁丝在氧气中燃烧生成物的质量( )2、现有m克氯酸钾和2克二氧化锰混合加热,完全反应后,留下残余物n克,则生成氧气的质量为( )A、(m-n)克 B 、(m-n-2)克
C、 (m-n+2)克 D、(n-2)克 A、大于铁丝的质量 B、小于铁丝的质量
C、等于铁丝的质量 D、无法比较
AC3、在化学反应前后肯定没有变化的是( )①原子的数目②元素的种类③分子的种类④原子的种类⑤物质的质量A、①②③④⑤ B、 ①②③④
C、 ①②④⑤ D、 ①④⑤4、某化合物在纯氧中燃烧生成二氧化碳和二氧化硫,则在化合物中一定含有 元素和 元素。 C碳硫评估:通过本节课的学习,你有哪些启发?内乡县夏馆初中认真 勤奋 拼搏 进取 欢迎您提出宝贵意见
1.可能是变大的
2.可能是不变的
3.可能是变小的教学目标:
1、能够完成对反应物和生成物质量的测定并总结出质量守衡定律
2、培养辨证唯物主义观点和定量研究、分析能力
3、在探究学习中学会协作、交流(如果反应物是两种液体,应如何称量其总质量?)注意:如需倾倒液体需小心操作,不要将液体倒在外面,以免影响实验结果探究活动一:氢氧化钠和硫酸铜混和后,质量是如何变化的?硫酸铜溶液氢氧化钠溶液烧杯试管天 平可选择的药品所用到的仪器现象:生成蓝色沉淀,天平仍保持平衡氢氧化钠+硫酸铜结论:反应前物质质量总和与生成物质量总和相等反应前后的质量测定想一想:反应前后天平是否平衡?为什么?解释:P+O2 P2O5
反应物质量守恒定律 参加化学反应的各物质的质量和,等于反应后生成的各物质的质量总和。同步练习:1、 克碳在32克氧气中充分燃烧生成44克二氧化碳。2、若电解18克水,可生成2克氢气和 克氧气。12163.6手脑并用探究活动二:比一比,赛一赛:用以下的仪器和药品试验,看质量有什么变化。提示:仔细观察实验现象。思考出现这种现象的原因。稀硫酸烧杯试管天 平可选择的药品所用到的仪器锌粒现象:锌的表面有气泡冒出,天平无法保持平衡锌+硫酸结论:反应前物质质量总和与生成物质量不相等?反应前后的质量测定想一想:为什么??参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。质量守恒定律2、“参加”意味着反应物中过量的剩余部分的质量不应算在内。如锌粒与稀硫酸的反应剩余的锌粒不算在内。1、“总和”意味着把各种状态的反应物和生成物都算在内。如肉眼看不见的气体也应考虑。3、初中化学中质量守恒定律仅适用于化学变化。1、氯酸钾受热分解后,剩余固体的质量比原反应物的质量轻。氯酸钾受热分解生成氯化钾和氧气。由质量守恒定律知,反应物氯酸钾的质量等于生成物氯化钾和氧气的质量,氧气散失到空气中,所以,剩余固体的质量必然比原反应物的质量轻练一练:化学反应的实质是什么?化学反应的实质是:
参加反应的各物质的分子分化成原子,原子再重新组合而生成其他物质的分子。 二、质量守恒的原因:
在化学反应中,反应前后
没改变, 没有改变,
也没有变化。所以,化学反应前后各物质的
必然相等。
原子的种类原子的数目原子的质量质量总和 原子的种类不变,所以元素的种类也不变。推测一些物质的组成进行有关计算如果将燃着的镁条上方罩上罩,使生成物全部收集起称量,会出现什么样的实验结果?想一想元素种类变了吗?元素质量变了吗?物质的总质量呢?化学反应前后物质种类呢?分子种类呢?动动脑不变改变巩固练习:1、根据质量守恒定律知,铁丝在氧气中燃烧生成物的质量( )2、现有m克氯酸钾和2克二氧化锰混合加热,完全反应后,留下残余物n克,则生成氧气的质量为( )A、(m-n)克 B 、(m-n-2)克
C、 (m-n+2)克 D、(n-2)克 A、大于铁丝的质量 B、小于铁丝的质量
C、等于铁丝的质量 D、无法比较
AC3、在化学反应前后肯定没有变化的是( )①原子的数目②元素的种类③分子的种类④原子的种类⑤物质的质量A、①②③④⑤ B、 ①②③④
C、 ①②④⑤ D、 ①④⑤4、某化合物在纯氧中燃烧生成二氧化碳和二氧化硫,则在化合物中一定含有 元素和 元素。 C碳硫评估:通过本节课的学习,你有哪些启发?内乡县夏馆初中认真 勤奋 拼搏 进取 欢迎您提出宝贵意见
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
