质量守恒定律[上学期]
图片预览







文档简介
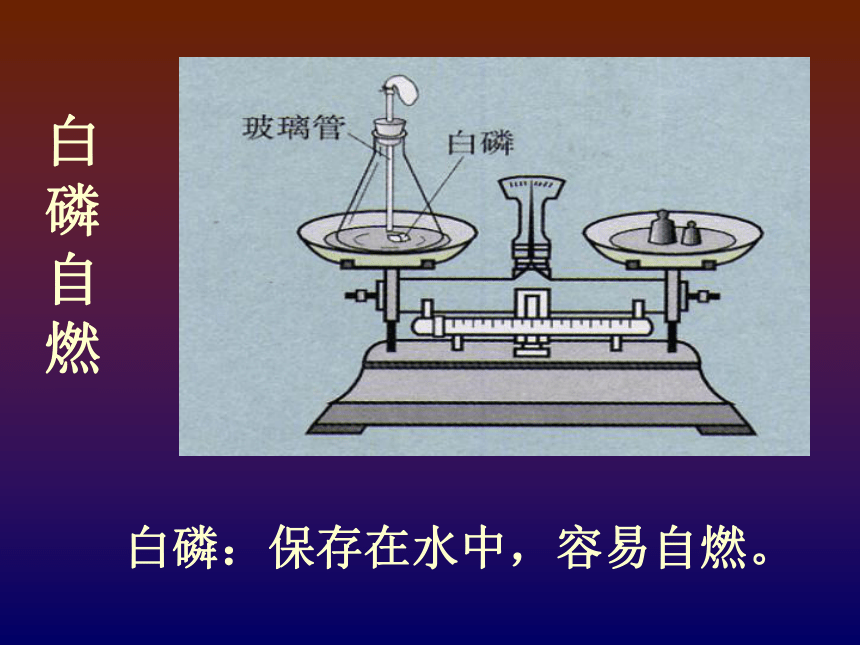
课件20张PPT。课题1 质量守恒定律凤城佳联国际学校 毕兴华白磷自燃白磷:保存在水中,容易自燃。Fe + CuSO4 =Cu + FeSO4银白色蓝色红色浅绿色一、质量守恒定律参加化学反应的各物质的质量总和,
等于生成物的各物质质量的总和。参加。(化学反应是按一定的质量比进行的,
不一定所有的物质都参加了反应)质量守恒。(不是体积和分子个数的守恒)总和。(不能忽略反应物或生成物中的气体)质量守恒定律的实质:在化学反应中,反应前后原子的种类,数目,原子的质量都没有改变。例1. 在化学反应前后,肯定没有发生变化的是( )
①原子数目②分子数目③元素种类④物质的总质量⑤物质的种类⑥原子的种类例2 铁燃烧后的黑色固体的质量比反应前的铁的质量要大,为什么??例3,下列 变化可用质量守恒定律进行解释的是( )
10g水变成10g冰
物质升华时要吸收热量
9g水完全电解成1g氢气和8g氧气
5g糖放入25g水总得到30g糖水练习:
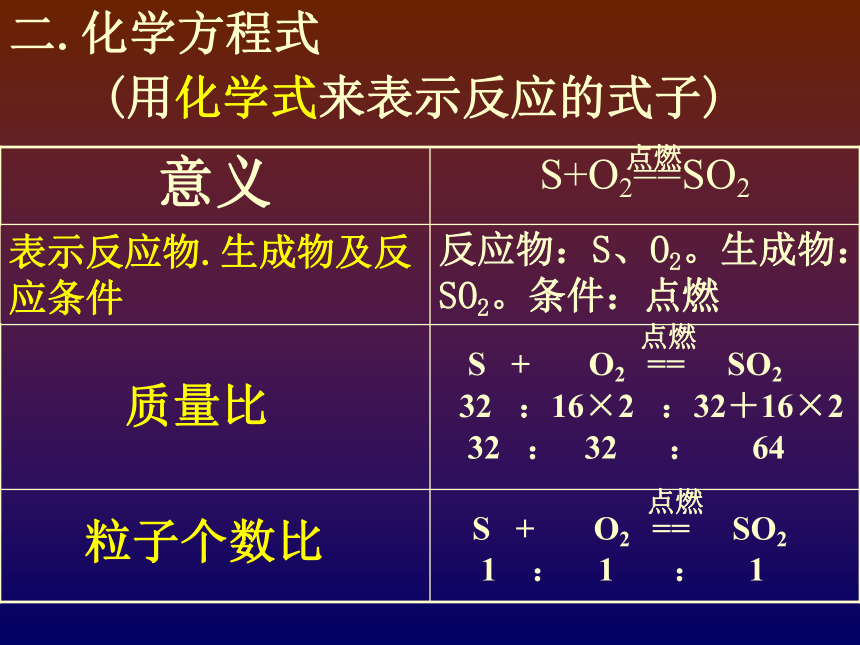
在化学反应A+B=C中,1.5g的A于足量的B充分反应后生成9.5gC,则参加反应的B的质量为 。二.化学方程式(用化学式来表示反应的式子)粒子个数比质量比反应物:S、O2。生成物:SO2。条件:点燃表示反应物.生成物及反应条件32 :16×2 :32+16×232 : 32 : 641 : 1 : 1化学方程式的读法:1)本质:硫和氧气在点燃条件下反应生成二氧化硫。和条件生成32 : 32 : 642)质量方面:每32份质量的硫和32份质量的氧气完全反应生成64份质量的二氧化硫。1 : 1 : 13)粒子个数方面:1个硫原子和1个氧分子反应生成1个二氧化硫分子。这个化学方程式给我们提供了哪些重要的信息?化学方程式的意义。将4.6g某化合物在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水,问:这种化合物含有哪几种元素?4.6g该化合物中各元素的质量分别是?化学反映的前后元素的质量不变。 已知48g镁于32g氧气恰好完全反应,生成氧化镁80g,则下列说法正确的是( )
5g镁和5g氧气生成10g氧化镁
6g镁和4g氧气生成10g氧化镁
3g镁和7g氧气生成10g氧化镁
4g镁和6g氧气生成10g氧化镁化学反应是按照一定质量比进行的。在化学方程式aC2H6+bO2==mCO2+nH2O中,各化学式前后的系数之间的关系正确的是( )
A、2m=a B、3a=n
C、3m=2n D、2b=m+n化学变化前后的原子的个数不变某化合物在空气中完全燃烧,生成二氧化碳和水。已知:每个该化合物分子和3个氧分子,生成2个二氧化碳分子和3个水分子,则这种化合物中应包含哪些元素?化合物分子中的各原子的个数比?CxHyOz+3O2=2CO2+3H2O“法轮功”邪教组织头目李洪志说,他发功能使铝发生化学变化,变成铜和金,“使铝分子变成铜分子和金分子”。请根据你所学的化学知识,指出这种说法违反科学之处。化学变化前后原子种类(元素种类)不变
等于生成物的各物质质量的总和。参加。(化学反应是按一定的质量比进行的,
不一定所有的物质都参加了反应)质量守恒。(不是体积和分子个数的守恒)总和。(不能忽略反应物或生成物中的气体)质量守恒定律的实质:在化学反应中,反应前后原子的种类,数目,原子的质量都没有改变。例1. 在化学反应前后,肯定没有发生变化的是( )
①原子数目②分子数目③元素种类④物质的总质量⑤物质的种类⑥原子的种类例2 铁燃烧后的黑色固体的质量比反应前的铁的质量要大,为什么??例3,下列 变化可用质量守恒定律进行解释的是( )
10g水变成10g冰
物质升华时要吸收热量
9g水完全电解成1g氢气和8g氧气
5g糖放入25g水总得到30g糖水练习:
在化学反应A+B=C中,1.5g的A于足量的B充分反应后生成9.5gC,则参加反应的B的质量为 。二.化学方程式(用化学式来表示反应的式子)粒子个数比质量比反应物:S、O2。生成物:SO2。条件:点燃表示反应物.生成物及反应条件32 :16×2 :32+16×232 : 32 : 641 : 1 : 1化学方程式的读法:1)本质:硫和氧气在点燃条件下反应生成二氧化硫。和条件生成32 : 32 : 642)质量方面:每32份质量的硫和32份质量的氧气完全反应生成64份质量的二氧化硫。1 : 1 : 13)粒子个数方面:1个硫原子和1个氧分子反应生成1个二氧化硫分子。这个化学方程式给我们提供了哪些重要的信息?化学方程式的意义。将4.6g某化合物在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水,问:这种化合物含有哪几种元素?4.6g该化合物中各元素的质量分别是?化学反映的前后元素的质量不变。 已知48g镁于32g氧气恰好完全反应,生成氧化镁80g,则下列说法正确的是( )
5g镁和5g氧气生成10g氧化镁
6g镁和4g氧气生成10g氧化镁
3g镁和7g氧气生成10g氧化镁
4g镁和6g氧气生成10g氧化镁化学反应是按照一定质量比进行的。在化学方程式aC2H6+bO2==mCO2+nH2O中,各化学式前后的系数之间的关系正确的是( )
A、2m=a B、3a=n
C、3m=2n D、2b=m+n化学变化前后的原子的个数不变某化合物在空气中完全燃烧,生成二氧化碳和水。已知:每个该化合物分子和3个氧分子,生成2个二氧化碳分子和3个水分子,则这种化合物中应包含哪些元素?化合物分子中的各原子的个数比?CxHyOz+3O2=2CO2+3H2O“法轮功”邪教组织头目李洪志说,他发功能使铝发生化学变化,变成铜和金,“使铝分子变成铜分子和金分子”。请根据你所学的化学知识,指出这种说法违反科学之处。化学变化前后原子种类(元素种类)不变
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
