Cu 与HNO3[下学期]
文档属性
| 名称 | Cu 与HNO3[下学期] |  | |
| 格式 | rar | ||
| 文件大小 | 219.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2005-12-21 07:49:00 | ||
图片预览






文档简介
课件22张PPT。铜与硝酸反应——化学实验习题
题的设计和解法示例学习重点:
考察化学基本操作:以化学反应为素材考查化学实验;通过实验设计考查对化学实验原理和操作过程的理解。
学习难点:
装置气密性的检查,装置的连接,实验的设计和分析,准确的化学语言的运用等。例1(1999年全国高考试题)图<1>装置可用于( )
A. 加热NaHCO3制CO2
B. 用Cu与稀HNO3反应
制NO
C. 用NH4Cl与浓NaOH
溶液反应制NH3
D. 用NaCl与浓H2SO4反
应制HCl
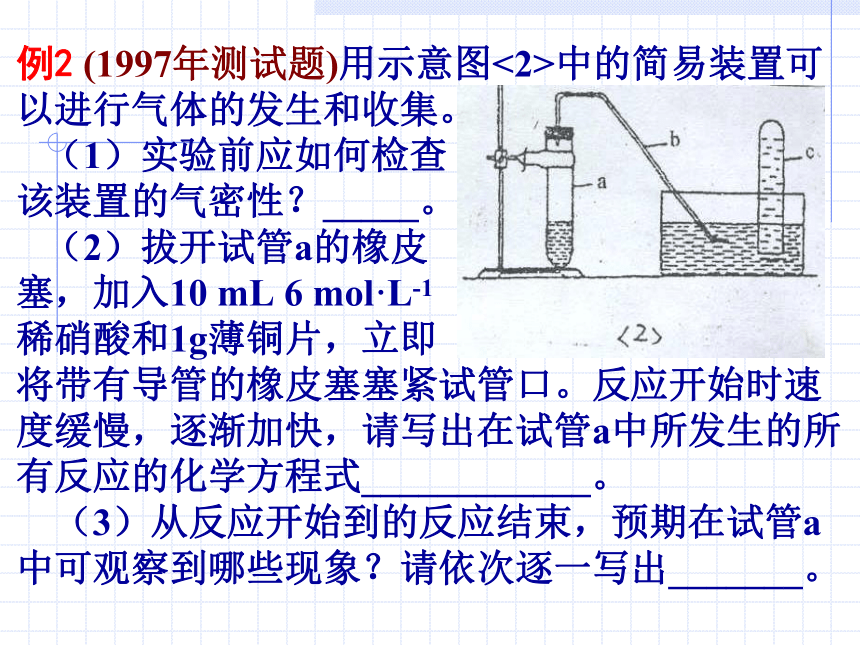
点评: 综合考查学生对常见气体的制备原理和收集方法的掌握,以及灵活运用知识的能力。实验室制备气体要遵循以下原则:①操作简便可行;②容易分离提纯;③经济实惠防毒。例2 (1997年测试题)用示意图<2>中的简易装置可以进行气体的发生和收集。
(1)实验前应如何检查
该装置的气密性?_____。
(2)拔开试管a的橡皮
塞,加入10 mL 6 mol·L-1
稀硝酸和1g薄铜片,立即
将带有导管的橡皮塞塞紧试管口。反应开始时速度缓慢,逐渐加快,请写出在试管a中所发生的所有反应的化学方程式____________。
(3)从反应开始到的反应结束,预期在试管a中可观察到哪些现象?请依次逐一写出_______。 (4)在反应开始时,可观察到导管b中的水面先沿导管b慢慢上升到一定高度,此后又回落,然后有气泡从管口冒出。试说明反应开始时,导管口水面上升的原因_________。
(5)试管c收集满气体后,用拇指堵住管口,取出水槽。将管口向上,松开拇指,片刻后,再次堵住管口,将试管再倒置于水槽中,松开拇指。此时可观察到什么现象?
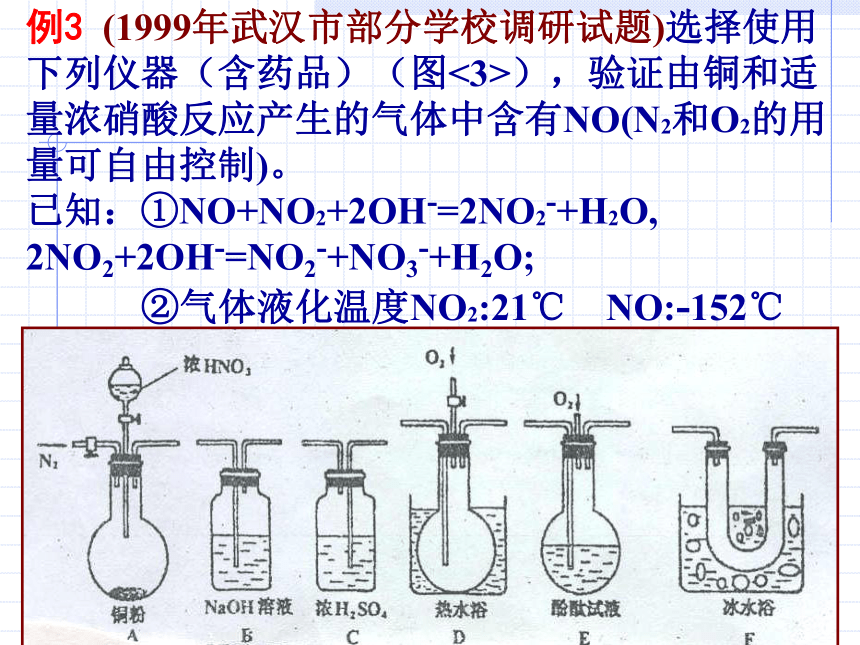
点评 : 本题是信息迁移式的实验简答题,意在考查学生的观察能力,实验能力和思维能力。解题时依据试题信息,细心观察实验装置图。联系已有基础知识,直接迁移,发散思维,用准确的化学语言解答实际问题。例3 (1999年武汉市部分学校调研试题)选择使用下列仪器(含药品)(图<3>),验证由铜和适量浓硝酸反应产生的气体中含有NO(N2和O2的用量可自由控制)。
已知:①NO+NO2+2OH-=2NO2-+H2O, 2NO2+2OH-=NO2-+NO3-+H2O;
②气体液化温度NO2:21℃ NO:-152℃ (1)甲乙丙三学生设计实验方案(用仪器的连接顺序表示)如下:
甲:A→C→F→D→B
乙:A→B→C→E
丙:A→F→D→B
讨论这些同学提出的实验方案是否能验证Cu与适量浓硝酸反应产生的气体中含有NO(填“能”或“不能”)?
甲________;乙_______;丙_______。
具体说明不能验证的主要原因(若3个实验方案都能验证,则此小题不用回答)___________。(2)反应前应先通入足量的N2,其目的是_______________。
(3)确认气体中含有NO的现象是_________。
(4)如果O2过量,则装置B中发生反应的化学方程式是:__________________。
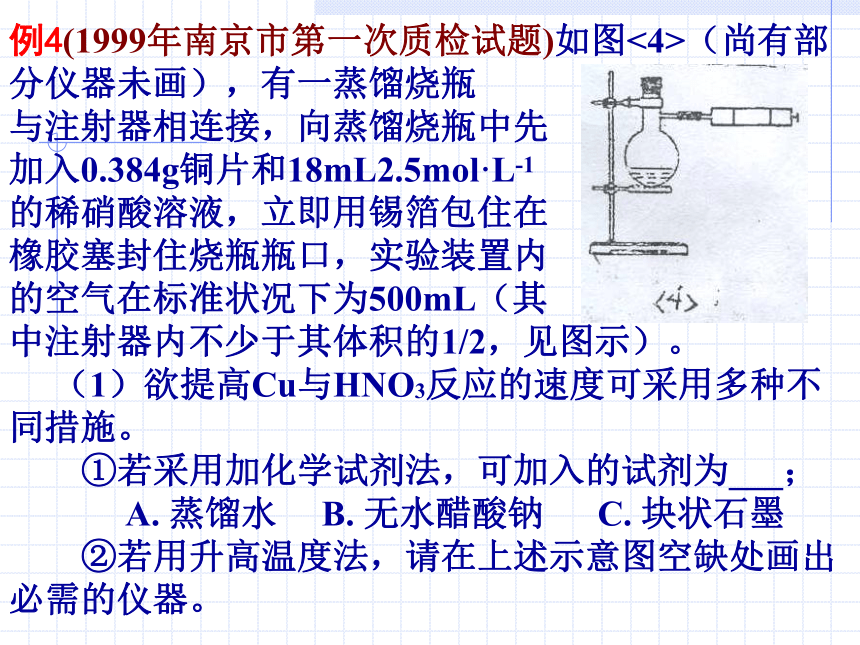
点评: 本题为信息迁移式综合实验题,其考查内容包括:最佳实验方案的设计,仪器(包括接口)的连接顺序,实验结果的分析等,从而达到从多个角度考查学生实验能力的目的,同时也考查学生的敏捷性和整体性。例4(1999年南京市第一次质检试题)如图<4>(尚有部分仪器未画),有一蒸馏烧瓶
与注射器相连接,向蒸馏烧瓶中先
加入0.384g铜片和18mL2.5mol·L-1
的稀硝酸溶液,立即用锡箔包住在
橡胶塞封住烧瓶瓶口,实验装置内
的空气在标准状况下为500mL(其
中注射器内不少于其体积的1/2,见图示)。
(1)欲提高Cu与HNO3反应的速度可采用多种不同措施。
①若采用加化学试剂法,可加入的试剂为___;
A. 蒸馏水 B. 无水醋酸钠 C. 块状石墨
②若用升高温度法,请在上述示意图空缺处画出必需的仪器。 (2)当烧瓶中的Cu和HNO3反应开始后,可观察到的现象有___________。
(3)待Cu与HNO3反应停止后,通过轻轻推拉注射器活塞,使装置内气体与气体、气体与液体之间充分反应,若忽略液体的体积变化,最终溶液中NO3-的物质的量浓度与开始时相比是否有变化________(填有变化或不变)。
(4)在上述反应过程中,曾经被还原的硝酸为________。 点评: 该题为典型的综合实验题,它取材于中学教学大纲中要求的铜与稀HNO3反应的演示实验和学生实验内容,通过一个比较新颖的装置图设问,考查考生综合运用化学反应速度和化学平衡等知识解决实际问题的能力;观察、记录实验现象,分析、处理实验结果和数据,从而得出正确结论的能力;识别和绘制典型的实验仪器装置图的能力。本题包容有选择、填空和简答,灵活多变,思考容量大。分析、解答此题运用了联想、推理、迁移、重组等思维方法。[相关练习题]
[1] 用下图(I)装置加入稀硝酸和铜片,在实验室里制备NO,在烧瓶中实际见到的气体是___色的,这就使人怀疑稀硝酸与铜反应是否真的能生成NO。即使可用排水取气法收集到NO,也可以认为是NO2与水反应生成NO而无法证实。现用U形管、分液漏斗、酒精灯、胶塞等仪器,设计下图(II)装置,来证实稀硝酸与铜反应的确生成了NO而不是NO2。 (1)补充完成实验步骤:
a. 检验装置的气密性_______________________。
b. 将活塞打开,以U形管长管口注入稀硝酸,一直到____________________________时为止。
c. 关闭活塞,用酒精灯在_____________加热,当观察到_____________________时,立即关闭酒精灯。
(2)观察现象:
(I)可以在何处观察到无色的NO气体?______。
反应在什么情况下可以自动停止?(铜丝与稀硝酸均未反应完)________________________________。
(II)如果再将活塞慢慢打开,可立即观察到明显现象有______________________。通过以上两个过程可以获得NO与NO2鲜明对照的实验效果。
(3)若用装置II制取并收集NO,应对装置作何简单的改动__________________________。 [1-1] 为了测定足量的铜与适量一定浓度的浓硝酸反应生成的NO气体和NO2气体的物质的量之比(用m表示),请从下图中选用适当的实验装置,设计一个合理而简单的实验,用于测定m的值。
其中E装置由甲、乙两根玻璃管组成,用橡皮管连通,并装入适量的水,甲管有刻度(0~50mL),供量气用,乙管可以上下移动,用来调节液面的高低。 (1)装置在连接顺序是(填各接口的编号,连接胶管及支持装置均省略):____。
(2)连接好装置并检验气密性后,应打开___通入N2;然后打开___,从乙管注水至充满甲、乙两管,关上ab。通入N2的原因是:________。
(3)实验后,若量气管中气体的体积(换算成标准状况下的体积)为V(mL),要测定m的值,还要将_____中的溶液中_____实验,假设测得其中溶质的物质的量为n,用含V和n的式子表示m:________。 (4)下列操作中能够造成m的值偏小的是(填序号)______________
(A)反应前E中甲管所装水里的气泡没赶尽,而最后读数时气泡消失。
(B)实验前,甲、乙两管液面在同一水平面上,最后读数时乙管的液面高于甲管的液面。
(C)实验前没有先通入足量N2。
(D)实验过程中,E装置乙管的水溢出。[2] 有人设计了一个特殊装置(如图),来制备NO并检验其有关性质。操作步骤如下:
①将干燥管细口端用塞有玻璃
球的胶管封好;
②从粗口端投入铜丝球,并在
如图位置固定好有孔塑料片;
③快速向干燥管中尽可能满的
加入稀硝酸(插入胶塞后,液面与
胶塞接触);
④迅速插好带玻璃管的单孔胶
塞,并倒置于一个大烧杯上(如图,烧杯略);
⑤待液面降至隔板以下,制气反应停止;
⑥用手挤压胶管中的玻璃球,空气自动进入干燥管发生反应。试回答下列问题: (1)硝酸尽可能加满的原因是:_________。
(2)⑤中液面降至隔板以下的原因是:__________(填序号):
A、生成气体的压力作用
B、液体自身的重力作用
从这一点看其原理类似于______(填一种实验仪器的名称)
(3)操作⑥中若进入一定量空气后停止挤压,能看到的明显现象有:
A,_________反应方程式为:__________。
B,_________反应方程式为:__________。
空气能自动进入干燥管的原因是:__________。
(4)该装置的最大优点是:______________。[3]为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。 (1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为_______. (2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为________________________; 装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧并E内气体颜色加深,产生上述现象的原因是___________________________。
一段时间后,C中白色沉淀溶解,其原因是______________________;
(3)装置D的作用是_____________________.
题的设计和解法示例学习重点:
考察化学基本操作:以化学反应为素材考查化学实验;通过实验设计考查对化学实验原理和操作过程的理解。
学习难点:
装置气密性的检查,装置的连接,实验的设计和分析,准确的化学语言的运用等。例1(1999年全国高考试题)图<1>装置可用于( )
A. 加热NaHCO3制CO2
B. 用Cu与稀HNO3反应
制NO
C. 用NH4Cl与浓NaOH
溶液反应制NH3
D. 用NaCl与浓H2SO4反
应制HCl
点评: 综合考查学生对常见气体的制备原理和收集方法的掌握,以及灵活运用知识的能力。实验室制备气体要遵循以下原则:①操作简便可行;②容易分离提纯;③经济实惠防毒。例2 (1997年测试题)用示意图<2>中的简易装置可以进行气体的发生和收集。
(1)实验前应如何检查
该装置的气密性?_____。
(2)拔开试管a的橡皮
塞,加入10 mL 6 mol·L-1
稀硝酸和1g薄铜片,立即
将带有导管的橡皮塞塞紧试管口。反应开始时速度缓慢,逐渐加快,请写出在试管a中所发生的所有反应的化学方程式____________。
(3)从反应开始到的反应结束,预期在试管a中可观察到哪些现象?请依次逐一写出_______。 (4)在反应开始时,可观察到导管b中的水面先沿导管b慢慢上升到一定高度,此后又回落,然后有气泡从管口冒出。试说明反应开始时,导管口水面上升的原因_________。
(5)试管c收集满气体后,用拇指堵住管口,取出水槽。将管口向上,松开拇指,片刻后,再次堵住管口,将试管再倒置于水槽中,松开拇指。此时可观察到什么现象?
点评 : 本题是信息迁移式的实验简答题,意在考查学生的观察能力,实验能力和思维能力。解题时依据试题信息,细心观察实验装置图。联系已有基础知识,直接迁移,发散思维,用准确的化学语言解答实际问题。例3 (1999年武汉市部分学校调研试题)选择使用下列仪器(含药品)(图<3>),验证由铜和适量浓硝酸反应产生的气体中含有NO(N2和O2的用量可自由控制)。
已知:①NO+NO2+2OH-=2NO2-+H2O, 2NO2+2OH-=NO2-+NO3-+H2O;
②气体液化温度NO2:21℃ NO:-152℃ (1)甲乙丙三学生设计实验方案(用仪器的连接顺序表示)如下:
甲:A→C→F→D→B
乙:A→B→C→E
丙:A→F→D→B
讨论这些同学提出的实验方案是否能验证Cu与适量浓硝酸反应产生的气体中含有NO(填“能”或“不能”)?
甲________;乙_______;丙_______。
具体说明不能验证的主要原因(若3个实验方案都能验证,则此小题不用回答)___________。(2)反应前应先通入足量的N2,其目的是_______________。
(3)确认气体中含有NO的现象是_________。
(4)如果O2过量,则装置B中发生反应的化学方程式是:__________________。
点评: 本题为信息迁移式综合实验题,其考查内容包括:最佳实验方案的设计,仪器(包括接口)的连接顺序,实验结果的分析等,从而达到从多个角度考查学生实验能力的目的,同时也考查学生的敏捷性和整体性。例4(1999年南京市第一次质检试题)如图<4>(尚有部分仪器未画),有一蒸馏烧瓶
与注射器相连接,向蒸馏烧瓶中先
加入0.384g铜片和18mL2.5mol·L-1
的稀硝酸溶液,立即用锡箔包住在
橡胶塞封住烧瓶瓶口,实验装置内
的空气在标准状况下为500mL(其
中注射器内不少于其体积的1/2,见图示)。
(1)欲提高Cu与HNO3反应的速度可采用多种不同措施。
①若采用加化学试剂法,可加入的试剂为___;
A. 蒸馏水 B. 无水醋酸钠 C. 块状石墨
②若用升高温度法,请在上述示意图空缺处画出必需的仪器。 (2)当烧瓶中的Cu和HNO3反应开始后,可观察到的现象有___________。
(3)待Cu与HNO3反应停止后,通过轻轻推拉注射器活塞,使装置内气体与气体、气体与液体之间充分反应,若忽略液体的体积变化,最终溶液中NO3-的物质的量浓度与开始时相比是否有变化________(填有变化或不变)。
(4)在上述反应过程中,曾经被还原的硝酸为________。 点评: 该题为典型的综合实验题,它取材于中学教学大纲中要求的铜与稀HNO3反应的演示实验和学生实验内容,通过一个比较新颖的装置图设问,考查考生综合运用化学反应速度和化学平衡等知识解决实际问题的能力;观察、记录实验现象,分析、处理实验结果和数据,从而得出正确结论的能力;识别和绘制典型的实验仪器装置图的能力。本题包容有选择、填空和简答,灵活多变,思考容量大。分析、解答此题运用了联想、推理、迁移、重组等思维方法。[相关练习题]
[1] 用下图(I)装置加入稀硝酸和铜片,在实验室里制备NO,在烧瓶中实际见到的气体是___色的,这就使人怀疑稀硝酸与铜反应是否真的能生成NO。即使可用排水取气法收集到NO,也可以认为是NO2与水反应生成NO而无法证实。现用U形管、分液漏斗、酒精灯、胶塞等仪器,设计下图(II)装置,来证实稀硝酸与铜反应的确生成了NO而不是NO2。 (1)补充完成实验步骤:
a. 检验装置的气密性_______________________。
b. 将活塞打开,以U形管长管口注入稀硝酸,一直到____________________________时为止。
c. 关闭活塞,用酒精灯在_____________加热,当观察到_____________________时,立即关闭酒精灯。
(2)观察现象:
(I)可以在何处观察到无色的NO气体?______。
反应在什么情况下可以自动停止?(铜丝与稀硝酸均未反应完)________________________________。
(II)如果再将活塞慢慢打开,可立即观察到明显现象有______________________。通过以上两个过程可以获得NO与NO2鲜明对照的实验效果。
(3)若用装置II制取并收集NO,应对装置作何简单的改动__________________________。 [1-1] 为了测定足量的铜与适量一定浓度的浓硝酸反应生成的NO气体和NO2气体的物质的量之比(用m表示),请从下图中选用适当的实验装置,设计一个合理而简单的实验,用于测定m的值。
其中E装置由甲、乙两根玻璃管组成,用橡皮管连通,并装入适量的水,甲管有刻度(0~50mL),供量气用,乙管可以上下移动,用来调节液面的高低。 (1)装置在连接顺序是(填各接口的编号,连接胶管及支持装置均省略):____。
(2)连接好装置并检验气密性后,应打开___通入N2;然后打开___,从乙管注水至充满甲、乙两管,关上ab。通入N2的原因是:________。
(3)实验后,若量气管中气体的体积(换算成标准状况下的体积)为V(mL),要测定m的值,还要将_____中的溶液中_____实验,假设测得其中溶质的物质的量为n,用含V和n的式子表示m:________。 (4)下列操作中能够造成m的值偏小的是(填序号)______________
(A)反应前E中甲管所装水里的气泡没赶尽,而最后读数时气泡消失。
(B)实验前,甲、乙两管液面在同一水平面上,最后读数时乙管的液面高于甲管的液面。
(C)实验前没有先通入足量N2。
(D)实验过程中,E装置乙管的水溢出。[2] 有人设计了一个特殊装置(如图),来制备NO并检验其有关性质。操作步骤如下:
①将干燥管细口端用塞有玻璃
球的胶管封好;
②从粗口端投入铜丝球,并在
如图位置固定好有孔塑料片;
③快速向干燥管中尽可能满的
加入稀硝酸(插入胶塞后,液面与
胶塞接触);
④迅速插好带玻璃管的单孔胶
塞,并倒置于一个大烧杯上(如图,烧杯略);
⑤待液面降至隔板以下,制气反应停止;
⑥用手挤压胶管中的玻璃球,空气自动进入干燥管发生反应。试回答下列问题: (1)硝酸尽可能加满的原因是:_________。
(2)⑤中液面降至隔板以下的原因是:__________(填序号):
A、生成气体的压力作用
B、液体自身的重力作用
从这一点看其原理类似于______(填一种实验仪器的名称)
(3)操作⑥中若进入一定量空气后停止挤压,能看到的明显现象有:
A,_________反应方程式为:__________。
B,_________反应方程式为:__________。
空气能自动进入干燥管的原因是:__________。
(4)该装置的最大优点是:______________。[3]为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。 (1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为_______. (2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为________________________; 装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧并E内气体颜色加深,产生上述现象的原因是___________________________。
一段时间后,C中白色沉淀溶解,其原因是______________________;
(3)装置D的作用是_____________________.
同课章节目录
