氢氧化物[上学期]
图片预览








文档简介
课件25张PPT。2
几种重要的金属化合物 第2课时 氢氧化物第三章 金属及其化合物汕头市潮阳西元中学 陈文丰『知识链接』 请把你认识的金属氢氧化物写出来,同时回忆物质分类的知识,并应用于对金属氢氧化物进行分类?(请打开课本93页,了解部分碱的溶解性。)比如你写出来了
没有?可 溶于水:KOH、NaOH、Ba(OH)2、
Ca(OH)2
不可溶于水:Cu(OH)2、Fe(OH)2、
Fe(OH)3、Al(OH)3、Mg(OH)2进行分类
若从溶解性这角度{『新课导入』二、氢氧化物Fe(OH)2 、Fe(OH)3(1)Fe(OH)2 、Fe(OH)3制取Fe(OH)2 、
Fe(OH)3
该如何制取?1. 铁的氢氧化物——制取的原理:可溶性铁盐、亚铁盐
与碱溶液反应反 应 本 质:Fe3+---→Fe(OH)3
Fe2+---→ Fe(OH)2 OH-OH-实验3-6大家请看教材:… … … … … … … … … 在两支试管里分别加入少量FeCl3和FeSO4溶液,
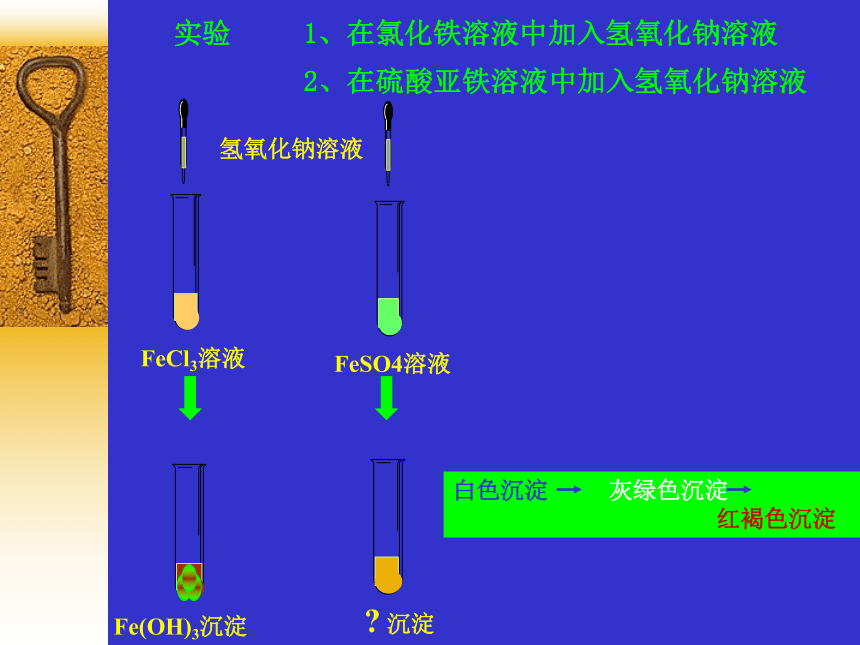
然后滴入NaOH溶液。观察并描述发生的现象实验 1、在氯化铁溶液中加入氢氧化钠溶液
2、在硫酸亚铁溶液中加入氢氧化钠溶液有红褐色沉淀生成有白色沉淀生成,迅速变为灰白色、灰绿色,FeCl3+3NaOH ==
Fe(OH)3↓+3NaClFeSO4+2NaOH ==
Fe(OH)2↓+Na2SO44Fe(OH)2+O2+2H2O==4 Fe(OH)3 在制取Fe(OH)2时,为什么很快会颜色的变化?最后变成红褐色
Fe3++3OH-== Fe(OH)3↓Fe2++2OH- == Fe(OH)2↓【讨论】为了观察Fe(OH)2的本来面目,你认为哪些方法可以制取氢氧化亚铁呢?请设计实验证明你的想法 (提示:O2存在溶液和空气中) 用煮沸冷却后的蒸
馏水配制所需溶液除去水中溶解的氧气在硫酸亚铁溶液中
滴加煤油等防止O2进一步溶解
在溶液中滴加碱时,滴管
伸入溶液内滴加避免与空气接触得到白色氢氧化亚铁沉淀
学 与 问 Fe(OH)2与Fe(OH)3都是不溶性碱,你能写出它们与酸反应的化学方程式吗?
[实验] 向(1)中制取的Fe(OH)2、Fe(OH)3试管分别滴入盐酸,观察现象。Fe(OH)2+2HCl=FeCl2+2H2O?????
Fe(OH)3+3HCl=FeCl3+3H2O沉淀逐渐溶解,发生如下反应:Fe(OH)2+H2SO4=FeSO4+2H2O??????
2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O这说明
什么? 加热Fe(OH)3时,它能失去水生成红棕色的Fe2O3粉末2Fe(OH)3===Fe2O3+3H2O↑△假如对Fe(OH)3加热,将会发生什么变化呢?这说明了Fe(OH)3的什么性质呢?2.氢氧化铝实验3-7… … … … … … … … … 在试管里加入10mL 0.5mol/LAl2(SO4)3溶液,滴加氨水,生成白色胶状物质,继续滴加氨水,直到不再产生沉淀为止【讨论】 Al(OH)3应该如何制取?(1)Al(OH)3的制取 【实验探究】 向两只盛有约5mL 0.5mol/L的Al2(SO4)3溶液中分别滴加氨水和2mol/L的NaOH 溶液,并振荡观察现象
白色胶状沉淀
继而沉淀消失白色胶状物质Al3+ + 3NH3· H2O == Al(OH) 3↓+ 3NH4+??
(氢氧化铝不溶于氨水)① Al3+ + 3OH- == Al(OH)3↓
② Al(OH)3 + OH- == AlO2-
+ 2H2O
Al(OH)3能与NaOH溶液反应,而Fe(OH)3呢? 根据以上探究实验,我们可知Al(OH)3能与强碱(如 NaOH)反应,不与弱碱NH3· H2O等反应 ,哪它能否与酸(如HCl)反应呢?(2)Al(OH)3的两性Al(OH)3+3HCl==AlCl3 +3H2OAl(OH)3+NaOH==NaAlO2+2H2O【讨论】:若将Al2(SO4)3溶液滴加入NaOH
溶液,其现象是否相同?(3)Al(OH)3受热易分解Fe(OH)3受热能分解,而Al(OH)3呢?2Al(OH)3=== Al2O3+3H2O△(4)Al(OH)3的用途(请参阅教材49页)你!
知道吗?(1)用Fe(OH)3、Al(OH)3制成的胶体
具有净水作用?『课外探究』
设计实验,除去FeCl3溶液中少量的AlCl3,
写出实验步骤和可能观察到的实验现象及有关
化学方程式、离子方程式。(2)Al(OH)3可用于治疗胃酸过多,其
原理是什么?
(3)人体应尽可能避免摄入过多的含铝食 物,如油条。
【小结】 1、掌握几种重要氢氧化物的性质 3、理解两性氢氧化物概念 2、掌握Fe(OH)2氧化成Fe(OH)3的过程4、了解Al(OH)3的用途板书设计二、氢氧化物
1.铁的氢氧化物——Fe(OH)2、Fe(OH)3
(1)Fe(OH)2、Fe(OH)3制取
(2)Fe(OH)2、Fe(OH)3与盐酸反应
(3)Fe(OH)3 受热易分解
2.氢氧化铝——Al(OH)3
(1)Al(OH)3 的制取
(2)Al(OH)3 的两性
(3)Al(OH)3 受热易分解
(4)Al(OH)3 的用途思考与练习 1、在含有1molFeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀得到的固体物质是( )
A、Fe B、FeO C、Fe(OH)3 D、Fe2O3 2、实验室中,要使AlCl3溶液中的Al3+离子全部沉淀出来,最佳用的试剂是( )
A、NaOH溶液 B、Ba(OH)2溶液 C、氨水D、盐酸 ☆3、(2000年高考题)把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为( )
A.70% B.52.4% C.47.6% D.30% 4、1mol/L AlCl3溶液中滴入1mol/L NaOH溶液,请画出生成
Al(OH)3的沉淀量随加入NaOH 的量的变化图。
n Al(OH)3(mol) n NaOH(mol)课外作业谢谢指导!!!『新课导入』二、氢氧化物1、铁的氢氧化物——Fe(OH)2 、Fe(OH)3(1)Fe(OH)2 、Fe(OH)3制取(2)Fe(OH)2、Fe(OH)3与盐酸反应『新课导入』二、氢氧化物1、铁的氢氧化物——Fe(OH)2 、Fe(OH)3(1)Fe(OH)2 、Fe(OH)3制取(2)Fe(OH)2、Fe(OH)3与盐酸反应(3)Fe(OH)3受热易分解 氢氧化铁和氢氧化亚铁的生成Al(OH)3吸附色素铝盐可能导致记忆力丧失 广泛使用铝盐[如:KAl(SO4)2·12H2O]净化水可能导致脑损伤,造成严重的记忆力丧失,这是老年性痴呆症特有的症状。参与这项工作的研究人员说,对老鼠的实验表明,混在饮用水中的微量铝进入老鼠的脑中并在那里逐渐积累。研究人员认为,如果随时间推移,铝在脑中逐渐积累,就会杀死神经原,使人的记忆力丧失。一位科学家说:我们一生都在喝铝盐净化过的水,吃含铝盐的食品,因此到我们很老时,我们体内已经积累了很多铝。他指出,过去70年早老性痴呆症发病率在世界范围内普遍上升。他说,铝也被用在食品乳化剂中。
对老鼠的研究发现,仅给它们喝下一杯经铝盐处理的水后,它们脑中的铝含量就达到可测量水平。铝制品为什么不能盛放含盐食品 铝制品的表面虽然有致密的保护膜,不易被氧化,但是当有较活泼的元素(如卤素)的离子存在时,氧化膜将这些离子吸附在表面,取代了膜中氧形成新的化合物。例如,有氯离子存在时,就会使一部分保护膜变成氯化铝,氯化铝易溶于水,因而使保护膜的结构遭到破坏,产生了孔隙,有害物质就可能渗入内部,加速铝制品的腐蚀。
???? 食盐的成分是氯化钠,其中还含有少量氯化镁,在水中溶解后能电离生成氯离子,因此会破坏保护膜。氯化镁在溶解时会发生水解,使溶液呈酸性,使铝制品腐蚀的更快。因此不能用铝制品盛含盐的蔬菜及食品。
摘自《生活与化学》铝锅会变黑吗?
有时候会碰到这样的怪事:一个新买回来的银光闪闪的铝锅,只用来煮了几次开水,铝锅中凡是有水浸到的地方,竟都变成了灰黑色。乍一看来,事情的确有些奇怪,铝锅是新的,除水以外还没有煮过其他东西,难道水会使铝锅变黑吗?
???? 通常的水,表面看来挺干净,实际上,它里面已溶解了不少东西,最常见的是钙盐、镁盐,其次是铁盐。不同来源的水所含的铁盐有多有少,这些铁盐就是使铝锅变黑的“祸首”。 由于铝比铁更活泼,铝锅碰上了含有铁盐的水,铝就能替换出铁,替换出来的铁附属在铝锅上,铝锅就变黑了。不过,这场化学戏法要变得成功必须有三个条件:
??? ?第一,水中含有的铁盐较多,
??? ?第二,煮水的时间要较长,
???? 第三,铝锅必须是新的,
??? ?因为旧的铝锅表面,有一层薄薄的氧化铝,这层氧化铝使得里面的铝没有机会“抛头露面”,戏法当然变不成了。既然黑色的物质是铁,因此用已变黑的铝锅来煮东西,并没有关系。用醋可以将这些黑色除去,有时煮几次番茄等酸性食物,也能使铁溶解,使铝锅重新回复光亮。不过这层黑色的物质可以不必除去,因为除掉后再烧开水又会发黑了,而且每除去一次,会使铝锅壁变薄一些,减少铝锅的使用寿命。
几种重要的金属化合物 第2课时 氢氧化物第三章 金属及其化合物汕头市潮阳西元中学 陈文丰『知识链接』 请把你认识的金属氢氧化物写出来,同时回忆物质分类的知识,并应用于对金属氢氧化物进行分类?(请打开课本93页,了解部分碱的溶解性。)比如你写出来了
没有?可 溶于水:KOH、NaOH、Ba(OH)2、
Ca(OH)2
不可溶于水:Cu(OH)2、Fe(OH)2、
Fe(OH)3、Al(OH)3、Mg(OH)2进行分类
若从溶解性这角度{『新课导入』二、氢氧化物Fe(OH)2 、Fe(OH)3(1)Fe(OH)2 、Fe(OH)3制取Fe(OH)2 、
Fe(OH)3
该如何制取?1. 铁的氢氧化物——制取的原理:可溶性铁盐、亚铁盐
与碱溶液反应反 应 本 质:Fe3+---→Fe(OH)3
Fe2+---→ Fe(OH)2 OH-OH-实验3-6大家请看教材:… … … … … … … … … 在两支试管里分别加入少量FeCl3和FeSO4溶液,
然后滴入NaOH溶液。观察并描述发生的现象实验 1、在氯化铁溶液中加入氢氧化钠溶液
2、在硫酸亚铁溶液中加入氢氧化钠溶液有红褐色沉淀生成有白色沉淀生成,迅速变为灰白色、灰绿色,FeCl3+3NaOH ==
Fe(OH)3↓+3NaClFeSO4+2NaOH ==
Fe(OH)2↓+Na2SO44Fe(OH)2+O2+2H2O==4 Fe(OH)3 在制取Fe(OH)2时,为什么很快会颜色的变化?最后变成红褐色
Fe3++3OH-== Fe(OH)3↓Fe2++2OH- == Fe(OH)2↓【讨论】为了观察Fe(OH)2的本来面目,你认为哪些方法可以制取氢氧化亚铁呢?请设计实验证明你的想法 (提示:O2存在溶液和空气中) 用煮沸冷却后的蒸
馏水配制所需溶液除去水中溶解的氧气在硫酸亚铁溶液中
滴加煤油等防止O2进一步溶解
在溶液中滴加碱时,滴管
伸入溶液内滴加避免与空气接触得到白色氢氧化亚铁沉淀
学 与 问 Fe(OH)2与Fe(OH)3都是不溶性碱,你能写出它们与酸反应的化学方程式吗?
[实验] 向(1)中制取的Fe(OH)2、Fe(OH)3试管分别滴入盐酸,观察现象。Fe(OH)2+2HCl=FeCl2+2H2O?????
Fe(OH)3+3HCl=FeCl3+3H2O沉淀逐渐溶解,发生如下反应:Fe(OH)2+H2SO4=FeSO4+2H2O??????
2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O这说明
什么? 加热Fe(OH)3时,它能失去水生成红棕色的Fe2O3粉末2Fe(OH)3===Fe2O3+3H2O↑△假如对Fe(OH)3加热,将会发生什么变化呢?这说明了Fe(OH)3的什么性质呢?2.氢氧化铝实验3-7… … … … … … … … … 在试管里加入10mL 0.5mol/LAl2(SO4)3溶液,滴加氨水,生成白色胶状物质,继续滴加氨水,直到不再产生沉淀为止【讨论】 Al(OH)3应该如何制取?(1)Al(OH)3的制取 【实验探究】 向两只盛有约5mL 0.5mol/L的Al2(SO4)3溶液中分别滴加氨水和2mol/L的NaOH 溶液,并振荡观察现象
白色胶状沉淀
继而沉淀消失白色胶状物质Al3+ + 3NH3· H2O == Al(OH) 3↓+ 3NH4+??
(氢氧化铝不溶于氨水)① Al3+ + 3OH- == Al(OH)3↓
② Al(OH)3 + OH- == AlO2-
+ 2H2O
Al(OH)3能与NaOH溶液反应,而Fe(OH)3呢? 根据以上探究实验,我们可知Al(OH)3能与强碱(如 NaOH)反应,不与弱碱NH3· H2O等反应 ,哪它能否与酸(如HCl)反应呢?(2)Al(OH)3的两性Al(OH)3+3HCl==AlCl3 +3H2OAl(OH)3+NaOH==NaAlO2+2H2O【讨论】:若将Al2(SO4)3溶液滴加入NaOH
溶液,其现象是否相同?(3)Al(OH)3受热易分解Fe(OH)3受热能分解,而Al(OH)3呢?2Al(OH)3=== Al2O3+3H2O△(4)Al(OH)3的用途(请参阅教材49页)你!
知道吗?(1)用Fe(OH)3、Al(OH)3制成的胶体
具有净水作用?『课外探究』
设计实验,除去FeCl3溶液中少量的AlCl3,
写出实验步骤和可能观察到的实验现象及有关
化学方程式、离子方程式。(2)Al(OH)3可用于治疗胃酸过多,其
原理是什么?
(3)人体应尽可能避免摄入过多的含铝食 物,如油条。
【小结】 1、掌握几种重要氢氧化物的性质 3、理解两性氢氧化物概念 2、掌握Fe(OH)2氧化成Fe(OH)3的过程4、了解Al(OH)3的用途板书设计二、氢氧化物
1.铁的氢氧化物——Fe(OH)2、Fe(OH)3
(1)Fe(OH)2、Fe(OH)3制取
(2)Fe(OH)2、Fe(OH)3与盐酸反应
(3)Fe(OH)3 受热易分解
2.氢氧化铝——Al(OH)3
(1)Al(OH)3 的制取
(2)Al(OH)3 的两性
(3)Al(OH)3 受热易分解
(4)Al(OH)3 的用途思考与练习 1、在含有1molFeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀得到的固体物质是( )
A、Fe B、FeO C、Fe(OH)3 D、Fe2O3 2、实验室中,要使AlCl3溶液中的Al3+离子全部沉淀出来,最佳用的试剂是( )
A、NaOH溶液 B、Ba(OH)2溶液 C、氨水D、盐酸 ☆3、(2000年高考题)把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为( )
A.70% B.52.4% C.47.6% D.30% 4、1mol/L AlCl3溶液中滴入1mol/L NaOH溶液,请画出生成
Al(OH)3的沉淀量随加入NaOH 的量的变化图。
n Al(OH)3(mol) n NaOH(mol)课外作业谢谢指导!!!『新课导入』二、氢氧化物1、铁的氢氧化物——Fe(OH)2 、Fe(OH)3(1)Fe(OH)2 、Fe(OH)3制取(2)Fe(OH)2、Fe(OH)3与盐酸反应『新课导入』二、氢氧化物1、铁的氢氧化物——Fe(OH)2 、Fe(OH)3(1)Fe(OH)2 、Fe(OH)3制取(2)Fe(OH)2、Fe(OH)3与盐酸反应(3)Fe(OH)3受热易分解 氢氧化铁和氢氧化亚铁的生成Al(OH)3吸附色素铝盐可能导致记忆力丧失 广泛使用铝盐[如:KAl(SO4)2·12H2O]净化水可能导致脑损伤,造成严重的记忆力丧失,这是老年性痴呆症特有的症状。参与这项工作的研究人员说,对老鼠的实验表明,混在饮用水中的微量铝进入老鼠的脑中并在那里逐渐积累。研究人员认为,如果随时间推移,铝在脑中逐渐积累,就会杀死神经原,使人的记忆力丧失。一位科学家说:我们一生都在喝铝盐净化过的水,吃含铝盐的食品,因此到我们很老时,我们体内已经积累了很多铝。他指出,过去70年早老性痴呆症发病率在世界范围内普遍上升。他说,铝也被用在食品乳化剂中。
对老鼠的研究发现,仅给它们喝下一杯经铝盐处理的水后,它们脑中的铝含量就达到可测量水平。铝制品为什么不能盛放含盐食品 铝制品的表面虽然有致密的保护膜,不易被氧化,但是当有较活泼的元素(如卤素)的离子存在时,氧化膜将这些离子吸附在表面,取代了膜中氧形成新的化合物。例如,有氯离子存在时,就会使一部分保护膜变成氯化铝,氯化铝易溶于水,因而使保护膜的结构遭到破坏,产生了孔隙,有害物质就可能渗入内部,加速铝制品的腐蚀。
???? 食盐的成分是氯化钠,其中还含有少量氯化镁,在水中溶解后能电离生成氯离子,因此会破坏保护膜。氯化镁在溶解时会发生水解,使溶液呈酸性,使铝制品腐蚀的更快。因此不能用铝制品盛含盐的蔬菜及食品。
摘自《生活与化学》铝锅会变黑吗?
有时候会碰到这样的怪事:一个新买回来的银光闪闪的铝锅,只用来煮了几次开水,铝锅中凡是有水浸到的地方,竟都变成了灰黑色。乍一看来,事情的确有些奇怪,铝锅是新的,除水以外还没有煮过其他东西,难道水会使铝锅变黑吗?
???? 通常的水,表面看来挺干净,实际上,它里面已溶解了不少东西,最常见的是钙盐、镁盐,其次是铁盐。不同来源的水所含的铁盐有多有少,这些铁盐就是使铝锅变黑的“祸首”。 由于铝比铁更活泼,铝锅碰上了含有铁盐的水,铝就能替换出铁,替换出来的铁附属在铝锅上,铝锅就变黑了。不过,这场化学戏法要变得成功必须有三个条件:
??? ?第一,水中含有的铁盐较多,
??? ?第二,煮水的时间要较长,
???? 第三,铝锅必须是新的,
??? ?因为旧的铝锅表面,有一层薄薄的氧化铝,这层氧化铝使得里面的铝没有机会“抛头露面”,戏法当然变不成了。既然黑色的物质是铁,因此用已变黑的铝锅来煮东西,并没有关系。用醋可以将这些黑色除去,有时煮几次番茄等酸性食物,也能使铁溶解,使铝锅重新回复光亮。不过这层黑色的物质可以不必除去,因为除掉后再烧开水又会发黑了,而且每除去一次,会使铝锅壁变薄一些,减少铝锅的使用寿命。
