高一上期末复习2[上学期]
图片预览



文档简介
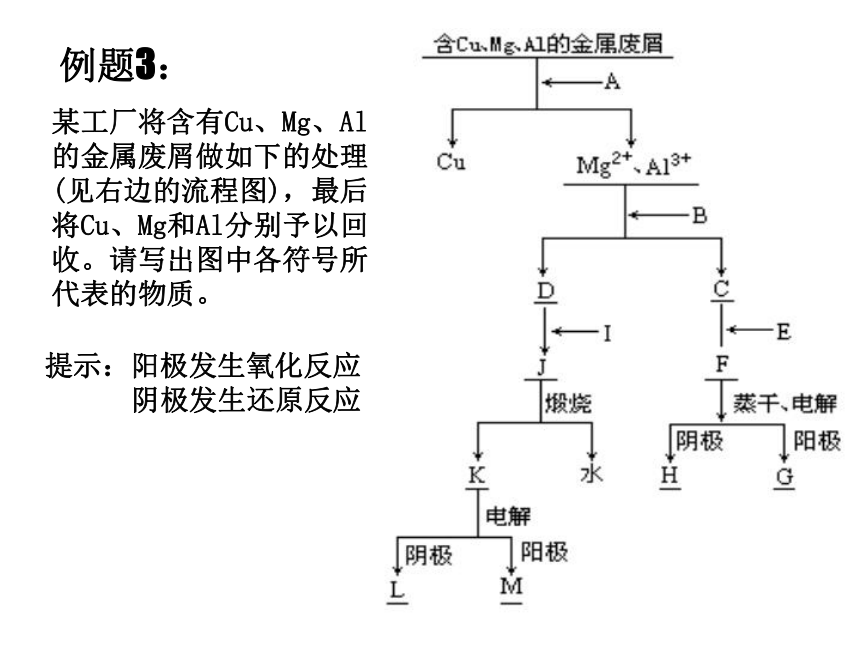
课件8张PPT。复习二 几种重要的金属例题1: 煤油中隔绝空气银白色金属通性变暗被氧化游,浮,响,熔,红密度小,反应剧烈,放热,产生气体,生成碱性物质例题2:请写出下列反应的离子方程式:A:碳酸氢钠溶液分别与盐酸和氢氧 化钠溶液的反应B:少量的碳酸钠与足量的盐酸反应C:少量的盐酸与足量的碳酸钠反应例题3:某工厂将含有Cu、Mg、Al的金属废屑做如下的处理(见右边的流程图),最后将Cu、Mg和Al分别予以回收。请写出图中各符号所代表的物质。提示:阳极发生氧化反应
阴极发生还原反应例题4:在含有0.02molMgCl2和0.02molAlCl3的混合溶液中,主要存在有______离子,向此混合液中加入100mL1mol/L的NaOH溶液后,混合液中增加了_____离子,______离子减少;继续加入1mol/LNaOH溶液50毫升后,混合液中主要存在______离子。 例题5:下列离子方程式中,不正确的是A、在氯化亚铁溶液中通入氯气
Fe2+ + Cl2 = Fe3+ + 2Clˉ
B、三氯化铁溶液跟过量氨水反应
Fe3+ + 3NH3?H2O = Fe(OH)3↓ + 3NH4+
C、氢氧化亚铁接触空气
4Fe(OH)2+2H2O+O2=4Fe(OH)3
D、铁粉投入氯化铜溶液
Fe + Cu2+ = Fe2+ + Cu己知①②是两性化合物,⑥的水溶液呈浅绿色。试写出①至⑧物质的化学式。 例题7:海水粗盐母液精盐Mg(OH)2MgCl26H2OMgCl2Mg贝壳CaO石灰乳蒸发水,重结晶盐酸
浓缩脱水 煅烧水问1:请写出上述过程中发生的化学反应方程式问2:上述没有涉及到四大基本反应类型中的哪些类型?问3:已知海水中镁的含量为1.10 mg/L,若有一工厂每天生产1.00t镁,则每天至少需要多少体积的海水?
阴极发生还原反应例题4:在含有0.02molMgCl2和0.02molAlCl3的混合溶液中,主要存在有______离子,向此混合液中加入100mL1mol/L的NaOH溶液后,混合液中增加了_____离子,______离子减少;继续加入1mol/LNaOH溶液50毫升后,混合液中主要存在______离子。 例题5:下列离子方程式中,不正确的是A、在氯化亚铁溶液中通入氯气
Fe2+ + Cl2 = Fe3+ + 2Clˉ
B、三氯化铁溶液跟过量氨水反应
Fe3+ + 3NH3?H2O = Fe(OH)3↓ + 3NH4+
C、氢氧化亚铁接触空气
4Fe(OH)2+2H2O+O2=4Fe(OH)3
D、铁粉投入氯化铜溶液
Fe + Cu2+ = Fe2+ + Cu己知①②是两性化合物,⑥的水溶液呈浅绿色。试写出①至⑧物质的化学式。 例题7:海水粗盐母液精盐Mg(OH)2MgCl26H2OMgCl2Mg贝壳CaO石灰乳蒸发水,重结晶盐酸
浓缩脱水 煅烧水问1:请写出上述过程中发生的化学反应方程式问2:上述没有涉及到四大基本反应类型中的哪些类型?问3:已知海水中镁的含量为1.10 mg/L,若有一工厂每天生产1.00t镁,则每天至少需要多少体积的海水?
