几种重要金属化合物(第一课时)[上学期]
文档属性
| 名称 | 几种重要金属化合物(第一课时)[上学期] |  | |
| 格式 | rar | ||
| 文件大小 | 360.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-05-16 14:05:00 | ||
图片预览

文档简介
课件11张PPT。课题:《几种重要的金属化合物》
(第一课时)授 课 人: 袁 文 清
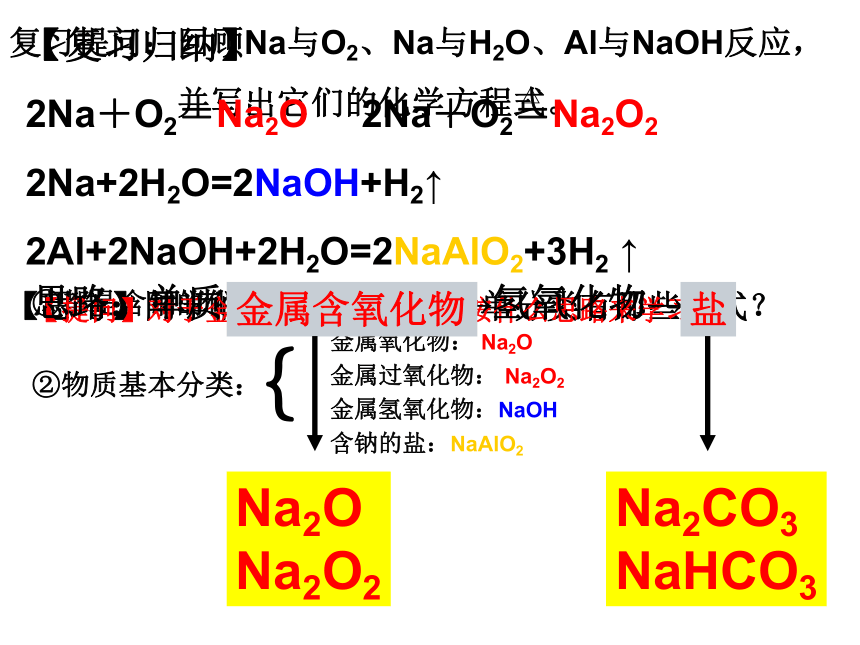
联系方式:ywq9195@126.com(4933605)敬请各位专家指教!同学们的收获是我们的共同快乐!复习提问:回顾Na与O2、Na与H2O、Al与NaOH反应,
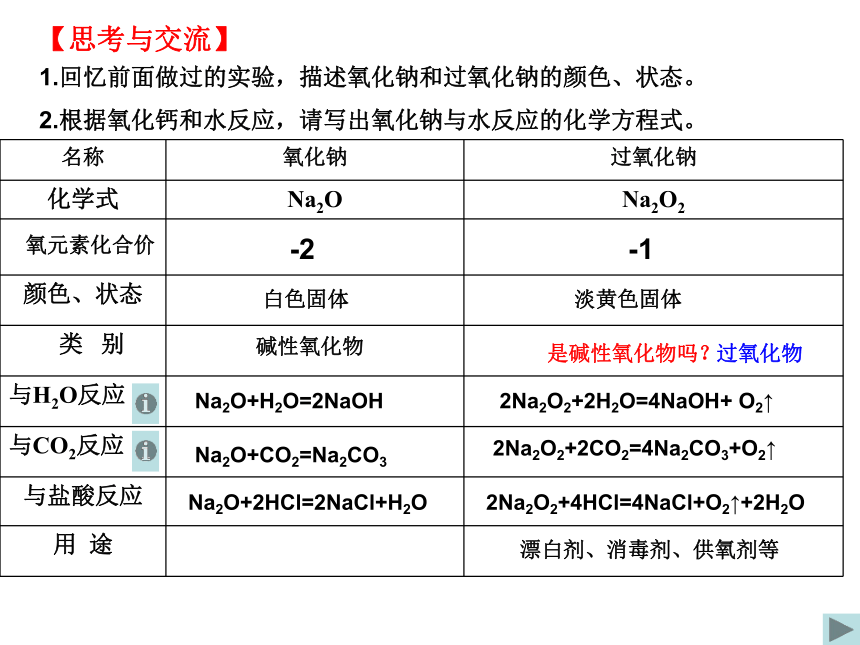
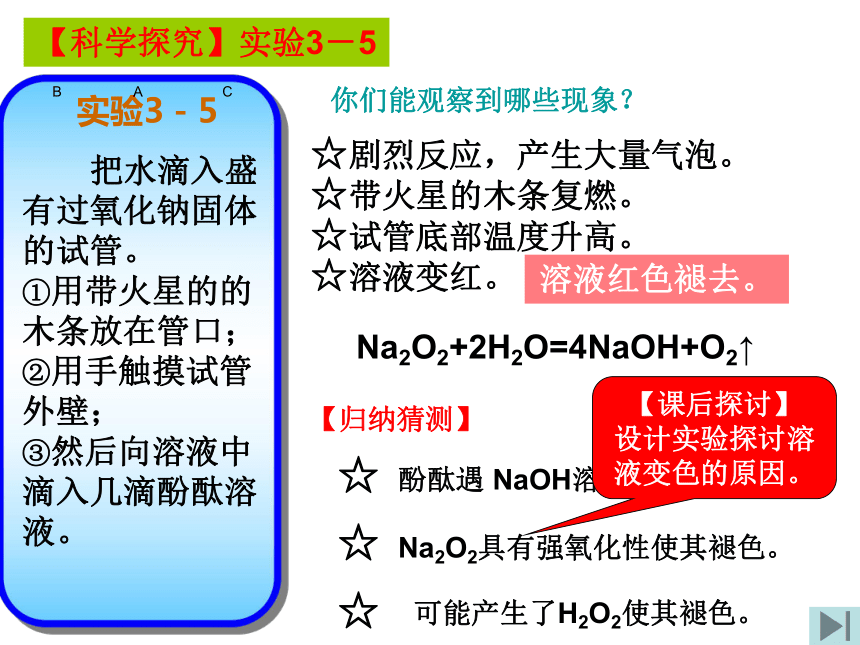
并写出它们的化学方程式。【思考】同学们对生成物进行简单分类有那些方式?【提问】对于金属元素学习,我们按什么思路来学习?思路:单质→金属氧化物→氢氧化物→盐金属含氧化物盐-2-1白色固体淡黄色固体碱性氧化物过氧化物Na2O+H2O=2NaOH2Na2O2+2H2O=4NaOH+ O2↑Na2O+CO2=Na2CO32Na2O2+2CO2=4Na2CO3+O2↑氧元素化合价漂白剂、消毒剂、供氧剂等Na2O+2HCl=2NaCl+H2O2Na2O2+4HCl=4NaCl+O2↑+2H2O是碱性氧化物吗?【科学探究】实验3-5你们能观察到哪些现象?☆剧烈反应,产生大量气泡。☆试管底部温度升高。☆溶液变红。溶液红色褪去。☆带火星的木条复燃。【归纳猜测】☆☆☆可能产生了H2O2使其褪色。 酚酞遇 NaOH溶液变红。Na2O2具有强氧化性使其褪色。Na2O2+2H2O=4NaOH+O2↑【课后探讨】
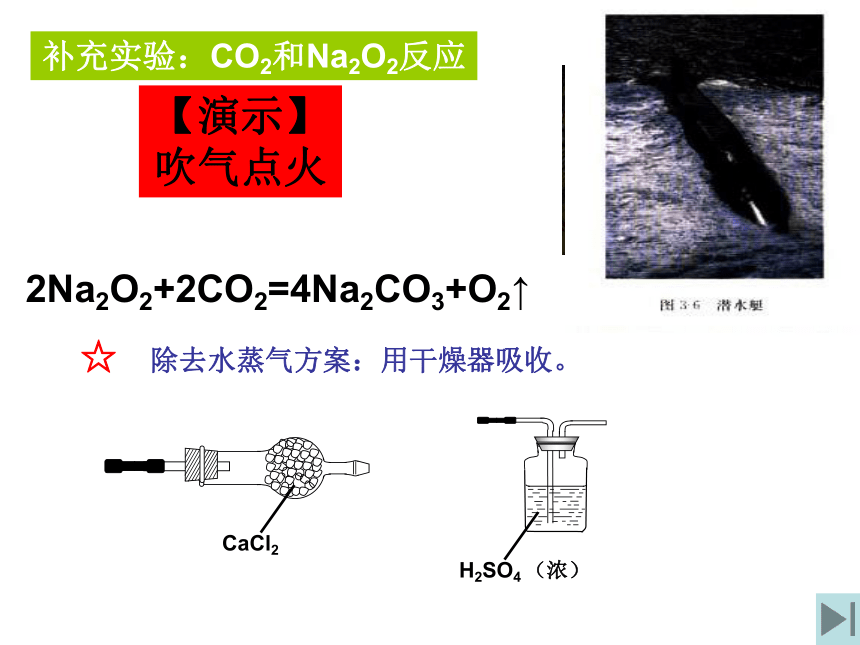
设计实验探讨溶液变色的原因。补充实验:CO2和Na2O2反应【演示】吹气点火2Na2O2+2CO2=4Na2CO3+O2↑☆ 除去水蒸气方案:用干燥器吸收。2.碳酸钠和碳酸氢钠鉴别相互转化热稳定性与酚酞作用水溶性色态俗名NaHCO3Na2CO3物质小苏打纯碱、苏打白色粉末细小白色晶体易溶溶液变红,显碱性稳定,加热不分解易溶Na2CO3>NaHCO3溶液变浅红,显碱性不稳定,加热不分解科学探究实
验实
验酸:H2CO3 、H+碱:NaOH、OH-谢谢同学们合作!溶解性比Na2CO3小,溶液碱性比Na2CO3弱。加水先变成含结晶水的晶体,溶液比NaHCO3碱性强。初步结论溶液变微红色溶液变红(较深)③加2滴酚酞固体量减少震荡时间长可溶解②加10mL 水细小白色粉末,加水部分溶解,感受不到热量变化白色粉末,加水结块成晶体,放热。①加1mL水NaHCO3Na2CO3实验步骤师生共同探究一(1)Na2CO3和NaHCO3的溶解性师生共同探究二(2)Na2CO3和NaHCO3的热稳定性澄清石灰水不变浑浊。澄清石灰水变浑浊。碳酸钠和碳酸氢钠的相互转变怎样鉴别碳酸钠和碳酸氢钠 ⑴ 加热固体。产生能使石灰水变浑浊的无色气体
的是碳酸氢钠。2NaHCO3 = Na2CO3 + H2O + CO2△ ⑶ 在固体中加入相同浓度的盐酸,反应剧烈的是碳酸氢钠。Na2CO3 + CaCl2 = 2NaCl + CaCO3 ⑵ 溶解,加入氯化钙溶液,产生沉淀的是碳酸钠。
(第一课时)授 课 人: 袁 文 清
联系方式:ywq9195@126.com(4933605)敬请各位专家指教!同学们的收获是我们的共同快乐!复习提问:回顾Na与O2、Na与H2O、Al与NaOH反应,
并写出它们的化学方程式。【思考】同学们对生成物进行简单分类有那些方式?【提问】对于金属元素学习,我们按什么思路来学习?思路:单质→金属氧化物→氢氧化物→盐金属含氧化物盐-2-1白色固体淡黄色固体碱性氧化物过氧化物Na2O+H2O=2NaOH2Na2O2+2H2O=4NaOH+ O2↑Na2O+CO2=Na2CO32Na2O2+2CO2=4Na2CO3+O2↑氧元素化合价漂白剂、消毒剂、供氧剂等Na2O+2HCl=2NaCl+H2O2Na2O2+4HCl=4NaCl+O2↑+2H2O是碱性氧化物吗?【科学探究】实验3-5你们能观察到哪些现象?☆剧烈反应,产生大量气泡。☆试管底部温度升高。☆溶液变红。溶液红色褪去。☆带火星的木条复燃。【归纳猜测】☆☆☆可能产生了H2O2使其褪色。 酚酞遇 NaOH溶液变红。Na2O2具有强氧化性使其褪色。Na2O2+2H2O=4NaOH+O2↑【课后探讨】
设计实验探讨溶液变色的原因。补充实验:CO2和Na2O2反应【演示】吹气点火2Na2O2+2CO2=4Na2CO3+O2↑☆ 除去水蒸气方案:用干燥器吸收。2.碳酸钠和碳酸氢钠鉴别相互转化热稳定性与酚酞作用水溶性色态俗名NaHCO3Na2CO3物质小苏打纯碱、苏打白色粉末细小白色晶体易溶溶液变红,显碱性稳定,加热不分解易溶Na2CO3>NaHCO3溶液变浅红,显碱性不稳定,加热不分解科学探究实
验实
验酸:H2CO3 、H+碱:NaOH、OH-谢谢同学们合作!溶解性比Na2CO3小,溶液碱性比Na2CO3弱。加水先变成含结晶水的晶体,溶液比NaHCO3碱性强。初步结论溶液变微红色溶液变红(较深)③加2滴酚酞固体量减少震荡时间长可溶解②加10mL 水细小白色粉末,加水部分溶解,感受不到热量变化白色粉末,加水结块成晶体,放热。①加1mL水NaHCO3Na2CO3实验步骤师生共同探究一(1)Na2CO3和NaHCO3的溶解性师生共同探究二(2)Na2CO3和NaHCO3的热稳定性澄清石灰水不变浑浊。澄清石灰水变浑浊。碳酸钠和碳酸氢钠的相互转变怎样鉴别碳酸钠和碳酸氢钠 ⑴ 加热固体。产生能使石灰水变浑浊的无色气体
的是碳酸氢钠。2NaHCO3 = Na2CO3 + H2O + CO2△ ⑶ 在固体中加入相同浓度的盐酸,反应剧烈的是碳酸氢钠。Na2CO3 + CaCl2 = 2NaCl + CaCO3 ⑵ 溶解,加入氯化钙溶液,产生沉淀的是碳酸钠。
