从海水获取化学物质 必修I
图片预览










文档简介
课件43张PPT。
2、根据上述实验现象和分析结果,写出电解氯化钠溶液的化学方程式:
2NaCl+2H2O===2NaOH+ H2↑+ Cl2↑通电2、氯气的实验室制法(1)实验原理:MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O
(2)发生装置:
粉末状固体或液体+液体 气体(3)除杂装置:饱和食盐水(4)干燥装置:浓硫酸(5)收集装置:向上排空气法或排饱和食 盐水法(6)尾气处理:用氢氧化钠溶液吸收氯 气?
重
庆
天
原
化
工
总
厂 氯气重庆氯气泄漏抢险纪实:
命悬一线 15万人大转移
新华网重庆4月17日(记者黄豁 张琴)16日凌晨,当繁华的山城已沉入梦乡的时候,一场意想不到的危险却悄然降临了。“嘭!”重庆天原化工总厂在寂静的黑夜中发出一声闷响,厂里2号氯冷凝器发生爆炸,黄绿色的氯气如同从瓶中释放的魔鬼弥漫开来。下午17时57分,正在抢险的化工厂再次发生爆炸,当即造成死亡和失踪9人……
不同浓度的氯气对人体的危害 大气中氯气的浓度不得超过0.1mg/m3,生产车间不超过1mg/m3 居民区不超过0.03mg/m3。
如果中毒,保持安静,注意保温,吸入少量乙醇和乙醚蒸汽或氨气。氯 气一、物理性质二、化学性质三 、氯气的用途一、物理性质颜色:
状态:
气味:
密度:
溶解性:
(水中)黄绿色刺激气味气体比空气大能溶于水(1:2) 易液化 : 黄色油状液体 ( 液氯)
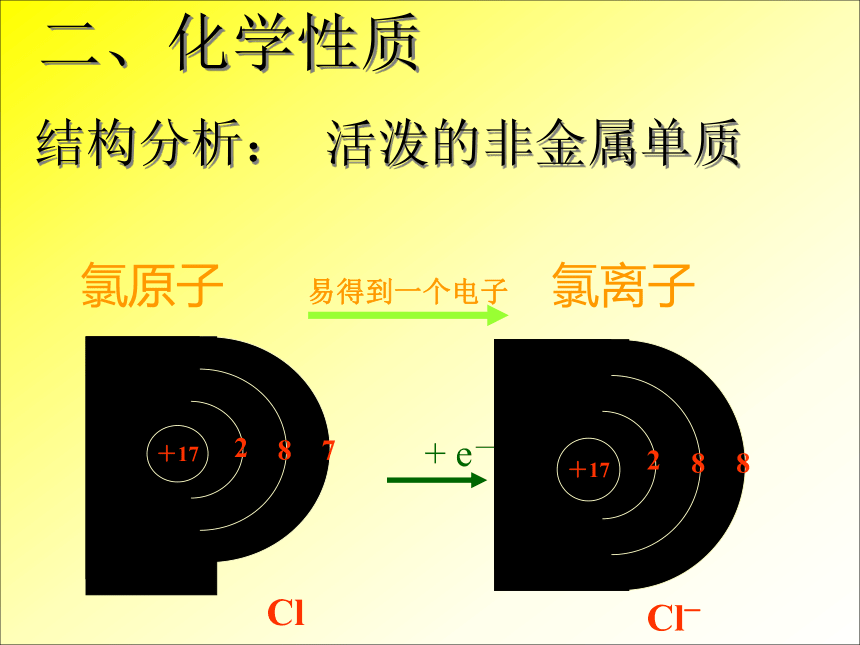
(闻?)二、化学性质结构分析:活泼的非金属单质ClCl_+ e-(1)铜与氯气的反应 现象:剧烈燃烧,生成棕黄色的烟。 反应方程式 : 加水后,溶液 呈蓝绿色(浓)或蓝色(稀)(棕黄色)(2)铁与氯气的反应 现象:剧烈燃烧,生成褐色的烟。 加水后,溶液呈
反应方程式 : 黄色。练一练写出氯气与下列金属反应的化学方程式Mg + Cl2
Al + Cl2
(1)氯气与氢气的反应 现象:安静的燃烧,火焰呈苍白色,
瓶口有白雾产生2、与非金属单质反应① 氢气在氯气中燃烧 反应方程式 : 工业制盐酸② 氢气与氯气的混合气体在强光下 现象:释放大量的热,发生爆炸。讨论1、工业制盐酸条件?2、左图是工业制盐酸使
用的燃烧管:A处通何种气体?
B处通何种气体?
先通谁? 如何防止Cl2溢出?工业用氯气和氢气化合制盐酸概念拓展:——任何发光发热的剧烈的化学反应燃烧常见助燃剂:O2 、 Cl2小结:Cl2是很活泼的非金属单质:
能与多种金属单质、非金属单质化合
表现强氧化性 氯气的水溶液叫氯水。请仔细观察,并根据已学的知识推测氯水中可能含有的分子和离子?氯 水3.与水反应:氯 水 水分子、含有的分子:
含有的离子: 氯气分子H+ Cl-、 如何检验可能含有的Cl-和H+呢?请设计最合理的实验方案。请思考:推测:氯 水检验Cl-离子的实验设计: 往氯水中滴加AgNO3溶液和稀HNO3溶液,如果有白色浑浊或沉淀出现,则说明氯水中含有Cl-离子。实验现象:有白色的浑浊出现实验结论:氯水中含有Cl-离子氯 水 将氯水加入紫色石蕊试液中,如紫色石蕊试液变红,则说明氯水中含有H+离子。检验H+离子的实验设计:实验现象:实验结论:紫色石蕊试液先变红,后马上褪色。先变红说明氯水中含有H+,后褪色说明在氯水中存在着具有漂白性的物质。氯 水说明在氯水中存在着具有漂白性的物质石蕊试液为什么会褪色呢?氯 水想一想 思考:该漂白性物质是Cl2本身,还是Cl2与H2O反应的生成的新物质?请设计合理的实验方案检验之。氯 水漂白性实验设计:1.在干燥的氯气瓶中放入一干燥的有色纸条。2.在干燥的氯气瓶中放入一湿润的有色纸条。实验现象:干燥的有色纸条未褪色,而湿润的有色纸条褪色。实验结论:具有漂白性的物质不是Cl2本身,而是Cl2与H2O反应的生成物HClO。 次氯酸 1、 次氯酸是一元弱酸,属于电解质,酸性弱于碳酸。 2、次氯酸不稳定,容易分解放出氧气。当氯水受到日光照射时,次氯酸的分解速率加快。 3、次氯酸具有强氧化性,因此可用来杀菌消毒和漂白有色物质。2.新制氯水中含有的粒子:3.久置氯水中含有的粒子:H2O 、H+、Cl-分子:Cl2、H2O、HClO
离子:Cl-、 H+、 ClO- 、OH -1.氯气与水的反应的方程式及离子方程式:小结:完成下列表格:气态液态液态Cl2分子 纯净物纯净物混合物Cl2分子 无无有H2O、 Cl2、HClOCl-、 H+、 ClO- 、OH -练习:混合物液态H2O、 Cl-、 H+无思考: 氯气和水反应生成HCl和HClO,试分析氯气和碱溶液会不会反应?如果能反应,则反应的生成物将会是什么? 4.与碱反应: 氯气与碱溶液反应生成
次氯酸盐,金属氯化物和水1.请写出Cl2和NaOH溶液反应的化学方程式:2.请写出Cl2和石灰乳反应的化学方程式:Cl2+2NaOH====NaCl+NaClO+H2O练习:【其有效成分是Ca(ClO)2 】 4.与碱反应: :
(1)用于自来水的杀菌消毒,1升水里约通人0.002克氯气;
(2)用于工业上制盐酸和漂白粉;
(3)用于制造多种农药,制造氯仿等有机溶剂
所以,氯气是一种重要的化工原料。
氯气的用途总结一、物理性质
氯气是一种黄绿色有刺激性气味的气体,有毒,密度比空气大,能溶于水,易液化。
二、化学性质1、与金属单质反应Cu + Cl2 = CuCl2点燃2、与非金属单质反应3.与水反应:4.与碱反应巩固练习:1.下列物质不具有漂白作用的是( )
A. 氯水 B. Ca(ClO)2
C. NaClO溶液 D. 过氧化钠
E. 活性炭 F. 液氯BF巩固练习:2.氯水可用来消毒、杀菌,又可作为漂白剂,其中起主要作用的是( )
A.Cl2 B.HClO C.HCl D.H2OB3.下列关于氯水的说法正确的是( )
A.新制的氯水只含有氯气分子和水分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.光照氯水有气泡逸出,该气体主要是氯气
D.新制氯水久置后酸性增强,几乎无漂白性 BD4.下列物质中含有Cl-的是( )
A.液氯 B.氯水
C.KClO溶液 D.CuCl2溶液
E.KClO3溶液 BD巩固练习:5.用自来水养鱼时,将氯水注入鱼缸前需在阳光 下曝晒一段时间,主要目的是( )
A.起杀菌作用 B.使水中的HClO分解
C.提高水温 D.增加水中O2的含量B巩固练习:6.漂白粉制取原理的反应方程式是 ;
漂白粉的成分是 ;有效成分是 ;漂白粉放置在空气中失效的方程是 。Ca(ClO)2+CO2+H2O====CaCO3↓+2HClO2Cl2+2Ca(OH)2=====CaCl2+Ca(ClO)2+2H2OCaCl2和Ca(ClO)2Ca(ClO)2久置氯水还有漂白性吗?思考: Cl-离子和Ag+离子反应生成难溶于酸白色AgCl沉淀,根据这一特性来检验Cl-离子。 与碱反应;与碱性氧化物反应;与活泼的金属反应;与碳酸盐或碳酸氢盐反应;用酸碱指示剂。Cl-离子的特性:H+离子的性质:再见!
2、根据上述实验现象和分析结果,写出电解氯化钠溶液的化学方程式:
2NaCl+2H2O===2NaOH+ H2↑+ Cl2↑通电2、氯气的实验室制法(1)实验原理:MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O
(2)发生装置:
粉末状固体或液体+液体 气体(3)除杂装置:饱和食盐水(4)干燥装置:浓硫酸(5)收集装置:向上排空气法或排饱和食 盐水法(6)尾气处理:用氢氧化钠溶液吸收氯 气?
重
庆
天
原
化
工
总
厂 氯气重庆氯气泄漏抢险纪实:
命悬一线 15万人大转移
新华网重庆4月17日(记者黄豁 张琴)16日凌晨,当繁华的山城已沉入梦乡的时候,一场意想不到的危险却悄然降临了。“嘭!”重庆天原化工总厂在寂静的黑夜中发出一声闷响,厂里2号氯冷凝器发生爆炸,黄绿色的氯气如同从瓶中释放的魔鬼弥漫开来。下午17时57分,正在抢险的化工厂再次发生爆炸,当即造成死亡和失踪9人……
不同浓度的氯气对人体的危害 大气中氯气的浓度不得超过0.1mg/m3,生产车间不超过1mg/m3 居民区不超过0.03mg/m3。
如果中毒,保持安静,注意保温,吸入少量乙醇和乙醚蒸汽或氨气。氯 气一、物理性质二、化学性质三 、氯气的用途一、物理性质颜色:
状态:
气味:
密度:
溶解性:
(水中)黄绿色刺激气味气体比空气大能溶于水(1:2) 易液化 : 黄色油状液体 ( 液氯)
(闻?)二、化学性质结构分析:活泼的非金属单质ClCl_+ e-(1)铜与氯气的反应 现象:剧烈燃烧,生成棕黄色的烟。 反应方程式 : 加水后,溶液 呈蓝绿色(浓)或蓝色(稀)(棕黄色)(2)铁与氯气的反应 现象:剧烈燃烧,生成褐色的烟。 加水后,溶液呈
反应方程式 : 黄色。练一练写出氯气与下列金属反应的化学方程式Mg + Cl2
Al + Cl2
(1)氯气与氢气的反应 现象:安静的燃烧,火焰呈苍白色,
瓶口有白雾产生2、与非金属单质反应① 氢气在氯气中燃烧 反应方程式 : 工业制盐酸② 氢气与氯气的混合气体在强光下 现象:释放大量的热,发生爆炸。讨论1、工业制盐酸条件?2、左图是工业制盐酸使
用的燃烧管:A处通何种气体?
B处通何种气体?
先通谁? 如何防止Cl2溢出?工业用氯气和氢气化合制盐酸概念拓展:——任何发光发热的剧烈的化学反应燃烧常见助燃剂:O2 、 Cl2小结:Cl2是很活泼的非金属单质:
能与多种金属单质、非金属单质化合
表现强氧化性 氯气的水溶液叫氯水。请仔细观察,并根据已学的知识推测氯水中可能含有的分子和离子?氯 水3.与水反应:氯 水 水分子、含有的分子:
含有的离子: 氯气分子H+ Cl-、 如何检验可能含有的Cl-和H+呢?请设计最合理的实验方案。请思考:推测:氯 水检验Cl-离子的实验设计: 往氯水中滴加AgNO3溶液和稀HNO3溶液,如果有白色浑浊或沉淀出现,则说明氯水中含有Cl-离子。实验现象:有白色的浑浊出现实验结论:氯水中含有Cl-离子氯 水 将氯水加入紫色石蕊试液中,如紫色石蕊试液变红,则说明氯水中含有H+离子。检验H+离子的实验设计:实验现象:实验结论:紫色石蕊试液先变红,后马上褪色。先变红说明氯水中含有H+,后褪色说明在氯水中存在着具有漂白性的物质。氯 水说明在氯水中存在着具有漂白性的物质石蕊试液为什么会褪色呢?氯 水想一想 思考:该漂白性物质是Cl2本身,还是Cl2与H2O反应的生成的新物质?请设计合理的实验方案检验之。氯 水漂白性实验设计:1.在干燥的氯气瓶中放入一干燥的有色纸条。2.在干燥的氯气瓶中放入一湿润的有色纸条。实验现象:干燥的有色纸条未褪色,而湿润的有色纸条褪色。实验结论:具有漂白性的物质不是Cl2本身,而是Cl2与H2O反应的生成物HClO。 次氯酸 1、 次氯酸是一元弱酸,属于电解质,酸性弱于碳酸。 2、次氯酸不稳定,容易分解放出氧气。当氯水受到日光照射时,次氯酸的分解速率加快。 3、次氯酸具有强氧化性,因此可用来杀菌消毒和漂白有色物质。2.新制氯水中含有的粒子:3.久置氯水中含有的粒子:H2O 、H+、Cl-分子:Cl2、H2O、HClO
离子:Cl-、 H+、 ClO- 、OH -1.氯气与水的反应的方程式及离子方程式:小结:完成下列表格:气态液态液态Cl2分子 纯净物纯净物混合物Cl2分子 无无有H2O、 Cl2、HClOCl-、 H+、 ClO- 、OH -练习:混合物液态H2O、 Cl-、 H+无思考: 氯气和水反应生成HCl和HClO,试分析氯气和碱溶液会不会反应?如果能反应,则反应的生成物将会是什么? 4.与碱反应: 氯气与碱溶液反应生成
次氯酸盐,金属氯化物和水1.请写出Cl2和NaOH溶液反应的化学方程式:2.请写出Cl2和石灰乳反应的化学方程式:Cl2+2NaOH====NaCl+NaClO+H2O练习:【其有效成分是Ca(ClO)2 】 4.与碱反应: :
(1)用于自来水的杀菌消毒,1升水里约通人0.002克氯气;
(2)用于工业上制盐酸和漂白粉;
(3)用于制造多种农药,制造氯仿等有机溶剂
所以,氯气是一种重要的化工原料。
氯气的用途总结一、物理性质
氯气是一种黄绿色有刺激性气味的气体,有毒,密度比空气大,能溶于水,易液化。
二、化学性质1、与金属单质反应Cu + Cl2 = CuCl2点燃2、与非金属单质反应3.与水反应:4.与碱反应巩固练习:1.下列物质不具有漂白作用的是( )
A. 氯水 B. Ca(ClO)2
C. NaClO溶液 D. 过氧化钠
E. 活性炭 F. 液氯BF巩固练习:2.氯水可用来消毒、杀菌,又可作为漂白剂,其中起主要作用的是( )
A.Cl2 B.HClO C.HCl D.H2OB3.下列关于氯水的说法正确的是( )
A.新制的氯水只含有氯气分子和水分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.光照氯水有气泡逸出,该气体主要是氯气
D.新制氯水久置后酸性增强,几乎无漂白性 BD4.下列物质中含有Cl-的是( )
A.液氯 B.氯水
C.KClO溶液 D.CuCl2溶液
E.KClO3溶液 BD巩固练习:5.用自来水养鱼时,将氯水注入鱼缸前需在阳光 下曝晒一段时间,主要目的是( )
A.起杀菌作用 B.使水中的HClO分解
C.提高水温 D.增加水中O2的含量B巩固练习:6.漂白粉制取原理的反应方程式是 ;
漂白粉的成分是 ;有效成分是 ;漂白粉放置在空气中失效的方程是 。Ca(ClO)2+CO2+H2O====CaCO3↓+2HClO2Cl2+2Ca(OH)2=====CaCl2+Ca(ClO)2+2H2OCaCl2和Ca(ClO)2Ca(ClO)2久置氯水还有漂白性吗?思考: Cl-离子和Ag+离子反应生成难溶于酸白色AgCl沉淀,根据这一特性来检验Cl-离子。 与碱反应;与碱性氧化物反应;与活泼的金属反应;与碳酸盐或碳酸氢盐反应;用酸碱指示剂。Cl-离子的特性:H+离子的性质:再见!
