必修I-人类对原子结构的认识
图片预览






文档简介
课件14张PPT。原子结构模型的演变 (1)人类对原子结构的认识经历了哪几个阶段?(2)道尔顿、汤姆生、卢瑟福、玻尔的原子结构模型有哪些错误或不足?(3)我们从原子结构的认识历程中受到哪些启迪?阅读思考道尔顿原子模型
1803 汤姆生原子模型
1904 卢瑟福原子模型
1911 玻尔原子模型
1913 道尔顿原子模型 (实心球) 19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。 汤姆生原子模型 (葡萄干面包) 1897年,英国科学家汤姆生发现了电子,认识到原子是由更小的微粒构成. 卢瑟福原子模型 (空心球) 1911年,英国物理学家卢瑟福根据α粒子散射现象认识到原子是由原子核和核外电子 构成. 玻尔原子模型 1913年丹麦物理学家玻尔提出,原子核外,电子在一系列稳定的轨道上运动。 排 布 规 律 能量最低原理
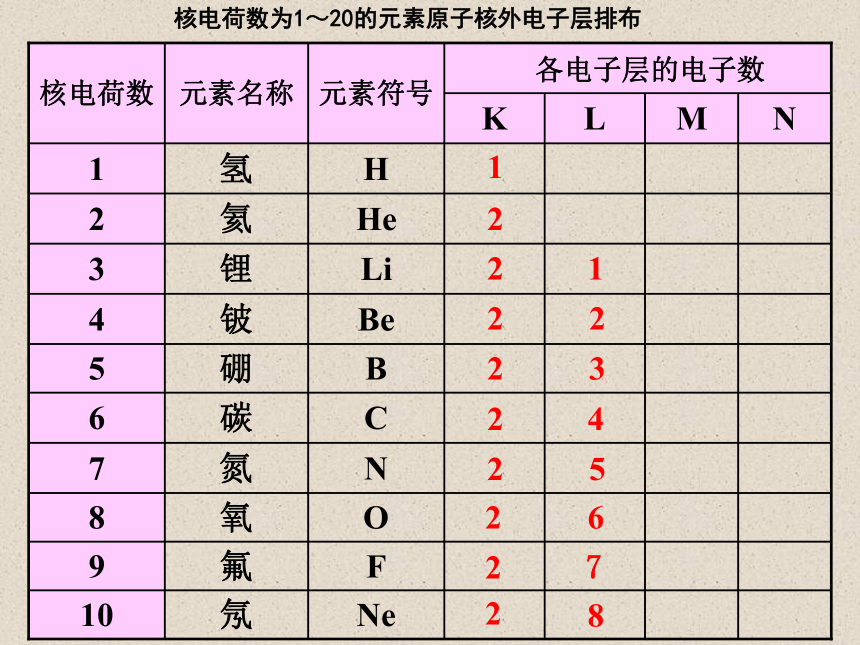
每个电子层最多只能排布2n2个电子。
K层为最外层时,最多只能容纳2个电子。
其它各层为最外层时,最多只能容纳8个电子。
次外层最多不超过18个电子。倒数第 三层不超过32个。
上述规律相互制约,相互联系
K→L → M→N → O → P2→ 8 →18→32→50→ 2n21→ 2 → 3→ 4→ 5 → 6
失一个电子钠原子钠离子+NaNa+钠离子的形成 氯离子的形成
得一个电子氯原子氯离子-
—+Na Cle Na+ Cl-
②⑧①⑧⑦②原子结构简图不稳定 3、元素性质与元素的原子核外电子排布的关系
稀有气体的不活泼性:稀有气体元素的原子最外层有8个电子(He为2)处于稳定
结构,因此化学性质稳定,一般不跟其它物质发生化学反应。
非金属性与金属性(一般规律):
金属元素 非金属元素
最外层电子数:
<4 >4
得失电子趋势:
易失 易得
元素性质:
金属性 非金属性
1803 汤姆生原子模型
1904 卢瑟福原子模型
1911 玻尔原子模型
1913 道尔顿原子模型 (实心球) 19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。 汤姆生原子模型 (葡萄干面包) 1897年,英国科学家汤姆生发现了电子,认识到原子是由更小的微粒构成. 卢瑟福原子模型 (空心球) 1911年,英国物理学家卢瑟福根据α粒子散射现象认识到原子是由原子核和核外电子 构成. 玻尔原子模型 1913年丹麦物理学家玻尔提出,原子核外,电子在一系列稳定的轨道上运动。 排 布 规 律 能量最低原理
每个电子层最多只能排布2n2个电子。
K层为最外层时,最多只能容纳2个电子。
其它各层为最外层时,最多只能容纳8个电子。
次外层最多不超过18个电子。倒数第 三层不超过32个。
上述规律相互制约,相互联系
K→L → M→N → O → P2→ 8 →18→32→50→ 2n21→ 2 → 3→ 4→ 5 → 6
失一个电子钠原子钠离子+NaNa+钠离子的形成 氯离子的形成
得一个电子氯原子氯离子-
—+Na Cle Na+ Cl-
②⑧①⑧⑦②原子结构简图不稳定 3、元素性质与元素的原子核外电子排布的关系
稀有气体的不活泼性:稀有气体元素的原子最外层有8个电子(He为2)处于稳定
结构,因此化学性质稳定,一般不跟其它物质发生化学反应。
非金属性与金属性(一般规律):
金属元素 非金属元素
最外层电子数:
<4 >4
得失电子趋势:
易失 易得
元素性质:
金属性 非金属性
